- Учителю
- Образовательный веб-квест по теме: Опасные химические вещества и объекты.
Образовательный веб-квест по теме: Опасные химические вещества и объекты.
Образовательный веб-квест по теме:
Опасные химические вещества и объекты.
Учитель: Маркина Римма Фарисовна, высшая квалификационная категория.
МОУ ИРМО «Усть-Кудинская СОШ»
Класс: 8
Тип урока: комбинированный.
Цели:
- дать знания об АХОВ и ХОО;
- довести до учащихся основные понятия об АХОВ и ХОО и их опасности;
- классифицировать крупнейших потребителей АХОВ
Оборудование: яркий воздушный шарик, компьютер, презентация урока, интерактивный кроссворд: «АХОВ», валеологические аудиозаписи, листы бумаги, фломастеры.
План урока:
1. Организационный этап - (2 мин.)
2. Основной этап.
Актуализация первичного опыта учащихся (5 мин.)
Совместное целеполагание. Задание «Билет в химическую
лабораторию»
Изучение нового материала. Работа в группах. Представление и
трансляция своего материала: АХОВ или презентация работ
учащихся.
3. Физкультурная пауза.
4. Закрепление нового материала: интерактивный кроссворд «АХОВ».
5. Подведение итогов, оценивание учащихся.
6. Домашнее задание.
7. Рефлексия
Ход урока
На перемене перед уроком звучит валеологическая мелодия. Класс проветрен. Учащиеся рассаживаются по группам.
1. Организационный этап.
Приветствие учащихся. Создание благоприятной психоэмоциональной обстановки на уроке. Передавая воздушный шар по цепочке ребята друг другу говорят один любой комплимент: «Ты замечательный человечек, хороший друг, очень умный, талантливый и т.д.
2. Основной этап.
Актуализация первичного опыта учащихся (5 мин.)
Прежде чем, перейти к изучению новой темы, мы должны с Вами вспомнить материал предыдущих уроков, разгадав кроссворд. Кроссворд «Радиация», его нужно выполнить на компьютере (буквы заглавные). Кроссворд на доске.
1
2
3
4
1. Неконтролируемый процесс горения, сопровождающийся уничтожением материальных ценностей и создающий опасность для жизни и здоровья людей. (Пожар)
2. Характер аварии, связанный с технической, производственной сферой деятельности человека.(Техногенный)
3. Самопроизвольный распад ядер нестабильных химических элементов, сопровождающийся выделением потока элементарных частиц и электромагнитным излучением. (Радиоактивность)
4. Реакция горения, при которой скорость выделения теплоты превышает скорость ее рассеивания. (Взрыв)
Учитель: - Что получилось у нас в вертикальном столбце? (АХОВ)
Кто знает, что означает эта аббревиатура АХОВ? (аварийно химически опасные вещества, верно.
Задание «Билет».
Учитель вручает каждому участнику входной билет в химическую лабораторию. Билет состоит из двух частей. На одной части участники урока пишут свои ожидания от предстоящей работы, а на другой (зона контроля) - свои опасения. (Подсказки для учеников: - С какими еще понятиями ассоциируется у вас понятие химически опасные вещества. Запишите несколько словосочетаний «Что я знаю». У вас есть какой-то личный опыт взаимодействия с химически опасными веществами? Что вы хотите узнать по этой теме?- Афишируйте, что вас интересует по этой теме? (Нужно знать свойства вещества, характер их влияния на организм? Нужно знать, где они используются? А какие крупнейшие аварии случались на химических объектах - это вас интересует? А как обстоят дела в Иркутской области?)
Учитель-модератор отрывает область контроля (опасения) и забирает себе, а часть билета, на которой написаны ожидания, остается у участника. Все участники прикрепляют свои ожидания на планшет своей группы. После этого учитель обобщает полученный результат.
- Сегодня мы подробно поговорим об опасных химических веществах, их характеристиках, поражающих факторах.
Запишем определение химически опасных веществ в тетрадь: Опасное химическое вещество - химическое вещество, прямое или опосредованное воздействие которого на человека может вызвать острые и хронические заболевания людей или их гибель.
Все опасные химические вещества делятся на 3 группы (учащиеся оформляют таблицу в тетради):
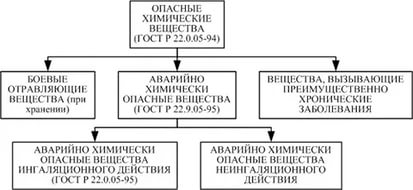
Учитель: А сейчас поработаем в группах. Ваша задача - донести до населения информацию о конкретном химическом веществе. Вы должны по своему материалу «Характеристика некоторых наиболее распространенных АХОВ», который готовили в течение недели, подготовиться к публичному выступлению, указав характеристики вещества, его влияние на человеческий организм, при этом транслируя вы переходите по ссылкам на ваш продукт: теория, опыты, интересные факты, полезное, картинки и др.
Прежде, чем вы приступите к работе, сделайте в тетради таблицу, заполняем её, слушая докладчиков.
Для ознакомления приведём характеристики наиболее распространённых АХОВ.Группа 1.
Аммиак (международный код - 1005)
Аммиак - бесцветный газ (международный код - 1005) с резким запахом, легче воздуха, температура плавления -80° С, температура кипения - 36° С, хорошо растворяется в воде, спирте и ряде других органических растворителей. Синтезируют из азота и водорода. В природе образуется при разложении азотсодержащих органических соединений.
Газ горюч, с воздухом образует взрывоопасную смесь. Ёмкости с газом при нагревании могут взрываться. Перевозится в сжиженном состоянии под давлением в железнодорожных цистернах с надписью «Аммиак».
Аммиак обладает удушающим действием, возбуждает центральную нервную систему и вызывает судороги. При высоких концентрациях возможен смертельный исход.
Интересные факты:
*От аммиака голубые и синие лепестки цветов становятся зелеными, ярко красные - черными.
*А некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать (например, астры).
Применение аммиака:
В основном используется для производства азотных удобрений (нитрат и сульфат аммония), взрывчатых веществ и полимеров, азотной кислоты, соды (по аммиачному методу) и других продуктов химической промышленности. Жидкий аммиак используют в качестве растворителя.
Опыты с аммиаком:
https://www.youtube.com/watch?v=P8334vJZlds
https://www.youtube.com/watch?v=WH27wEk5wB8
Группа 2.
Хлор.
Хлор - при нормальных условиях газ жёлто-зелёного цвета с резким раздражающим специфическим запахом, тяжелее воздуха примерно в 2,5 раза, вследствие чего стелется по земле, скапливаясь в низинах, подвалах, колодцах, переходах, туннелях. Хранится и перевозится под давлением в стальных баллонах и железнодорожных цистернах жёлтого цвета с красной полосой. При выходе в атмосферу дымит, заражает водоёмы. Мало растворим в воде, не горюч. При испарении образует с водяными парами белый туман. 1 кг жидкого газа образует 316 л газа. Международный код - 1017.
Физические и химические свойства хлора.
tgko.ru/spravka/gaz/hlor
Простые опыты с хлором.
www.h2o.u-sonic.ru/exp/cl.htm
Опыты с хлором, видео.
https://www.youtube.com/watch?v=Osp4yA3uL50
Группа 3.
Ртуть.
Опасна для жизни и здоровья также ртуть - серебристый жидкий металл плотностью 13,5 г/см3. Применяется в термометрах, манометрах, приборах, при производстве хлора и едкого натра (в качестве катода). Ртуть и её соединения ядовиты. Она легко испаряется даже при низкой температуре. При разливе равномерно распространяется по всему объёму. При температуре выше +28 0С пары ртути снова попадают в воздух. Они характеризуются ярко выраженной токсичностью, что пагубно сказывается на эндокринной системе человека: вначале появляются повышенная утомляемость, слабость, сонливость и головная боль. Позже начинают дрожать руки, веки, а в тяжёлых случаях - ноги. Меры спасения: быстро покинуть опасное место и срочно вызвать специалистов; постараться сменить одежду; принять душ; прополоскать рот 0,25%-ным раствором марганцовки; обязательно почистить зубы.
Физические и химические свойства ртути:
chemhelper.ru/dir.php?id_dir=218
Чем ртуть опасна для человека:
fb.ru/article/160913/rtut-opasnost-dlya-cheloveka-chem-opasna-rtut
Отравление ртутью из градусника:
www.ja-zdorov.ru/blog/otravlenie-rtutyu-iz-gradusnika-ugroza-zdorovyu-cheloveka/
Группа 4. Серная кислота.
Се́рная кислота́ H2SO4 - сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота - тяжёлая маслянистая жидкость без цвета и запаха, с кислым «медным» вкусом.
Серная кислота является более сильной кислотой чем соляная, концентрированная обугливает сахар, дерево, хлопок, шерсть и вызывает очень глубокие ожоги кожи. При приготовлении раствора серной кислоты необходимо следовать следующему правилу: Кислоту льют в воду тонкой струйкой по стенке стеклянной посуды, но не наоборот. Серную кислоту, за счет ее свойства поглощать большие количества воды, использую для осушения в зимнее время окон, предварительно поставив между рамами концентрированную серную кислоту в стакане, заполнив на 1/5 объема. Серная кислота также применяется для приготовления аккумуляторной кислоты.
Химические свойства и промышленное производство:
himege.ru/sernaya-kislota-ximicheskie-svojstva-i-promyshlennoe-proizvodstvo/
Опыт с серной кислотой-https://www.youtube.com/watch?v=B38zQz7i57A
Группа 5. Соляная кислота.
Соляная кислота - раствор хлористого водорода в воде.
Интересные факты:
-
Желудок человека вынужден ежедневно обновлять свою поверхность взамен пострадавшей от желудочного сока, то есть соляной кислоты
-
Желудочный сок человека достаточно агрессивен для того, чтобы полностью растворить бритвенное лезвие за неделю
Применение:
Соляная кислота хорошо растворяет металлы, в том числе цинк, олово, железо, но не взаимодействует с золотом, серебром и медью. Соляную кислоту можно смешивать с водой в любых соотношениях. Применяется для очистки от известкового налета раковины эмалированные и фаянсовые, унитазы, умывальники. Можно применять для очистки тканей от ржавых пятен, чернил (готовится слабый раствор кислоты). Соляная кислота разрушает ткани, изготовленные льна, хлопка, искусственного шелка. При попадании на кожу вызывает химические ожоги
Физические и химические свойства chemhelper.ru/dir.php?id_dir=209
Опыты:
https://www.youtube.com/watch?v=5B6tm2fMADg
https://www.youtube.com/watch?v=UKeykk9oB4w
Группа 6. Сернистый ангидрид
Сернистый ангидрид при атмосферном давлении и температуре 0°С представляет собой бесцветный газ с удушливым запахом. Он тяжелее воздуха в 2,264 раза (плотность 2,9263 кг/м3). Температура плавления сернистого ангидрида - минус 75,5° С, температура кипения- минус 10°С (под атмосферным давлением).
Сернистый ангидрид не горит и не поддерживает горения, в связи с чем является безопасным в пожарном отношении.
Газообразный сернистый ангидрид очень вредно действует на дыхательные органы человека, вызывая воспаление слизистых оболочек. Высокие концентрации сернистого ангидрида в атмосфере чрезвычайно опасны.
Растворимость сернистого ангидрида в воде с повышением температуры уменьшается. При температуре 0°С насыщенный раствор содержит 23% SO2 при 20° С - 11,5%, при 30° С - 7,8%.
Источник: www.activestudy.info/svojstva-sernistogo-angidrida/ ©
Применение сернистого ангидрида
sernistyj-angidrid.ru/primenenie-sernistogo-angidrida
Группа 7. Сероводород.
Сероводоро́д (серни́стый водоро́д, сульфид водорода, дигидросульфид) - бесцветный газ с запахом протухших яиц и сладковатым вкусом. Химическая формула - H2S. Плохо растворим в воде, хорошо - в этаноле. Ядовит. При больших концентрациях разъедает многие металлы. Концентрационные пределы воспламенения с воздухом составляют 4,5 - 45 % сероводорода.
В природе встречается очень редко в виде смешанных веществ нефти и газа. Входит в состав вулканических газов. Образуется при гниении белков. Сероводород используют в лечебных целях, например в сероводородных ваннах.
Свойства и применение
allrefs.net/c26/41xfq/p24/
fizterapia.ru/pokazaniya-i-protivopokazaniya-k-primeneniyu-serovodorodnyih-vann/
Группа 8.
Синильная кислота - бесцветная быстро испаряющаяся жидкость с запахом горького миндаля. На открытой местности быстро улетучивается (через 10-15 мин), не заражает местность и технику. Дегазация помещений, убежищ и закрытых машин производится проветриванием. В полевых условиях возможно значительное сорбирование синильной кислоты обмундированием.
Обеззараживание достигается также проветриванием. Температура замерзания синильной кислоты минус 14°С, поэтому в холодное время применяется в смеси с хлорцианом или другими 0В. Синильная кислота может применяться химическими авиабомбами крупного калибра. Поражение наступает при вдыхании зараженного воздуха (возможно поражение через кожу при длительном действии очень высоких концентраций).
Средствами защиты от синильной кислоты являются противогаз, убежища и техника, оснащенные фильтровентиляционными установками. При поражении синильной кислотой появляются неприятный металлический привкус и жжение во рту, онемение кончика языка, покалывание в области глаз, царапанье в горле, состояние беспокойства, слабость и головокружение. кислота кумулятивным действием не обладает.
armyman.info/sinilnaya-kislota-ac-i-cianidy.html
воздействие на человека:
otravleniya.net/ximicheskie-otravleniya/otravlenie-sinilnoj-kislotoj.html
синильная кислота в косточках фруктов: otravleniya.net/fakty-ob-otravleniyax/sinilnaya-kislota-v-kostochkax.html
На территории Российской Федерации насчитывается более 3300 химически опасных объектов.
- Какие химически опасные объекты существуют в Иркутской области? (ж/д, автозаправки, водозабор)
- Были ли у нас аварии на этих объектах?
- Хорошо, что серьезных катастроф не было, но знать о них и быть готовыми к ним нужно всегда.
- В каком регионе России больше всего ХОО? Как вы думаете, почему? (в центральном и северокавказском, здесь больше численность населения)
- В каком регионе живём мы? Какое количество ХОО находится в нашем регионе? (Поволжский регион занимает третье место по числу химически опасных объектов после Центрального и Северо-Кавказского)
- Зависит ли количество ХОО от плотности населения региона? (чем более густонаселенная территория, тем больше таких предприятий)
В зонах возможного химического поражения проживает около 53 миллионов человек.
3. Физкультурная пауза.
Гимнастика для глаз
Движения выполняются легко, без напряжения, с удовольствием, не щурясь.
а) горизонтальные движения: влево и вправо; влево - вперед и
вправо - вперед.
б) вертикальные движения: вверх и вниз; вверх - прямо перед собой и
вниз - прямо перед собой.
в) движения по диагонали в двух направлениях: лево верх - право низ
и право верх - лево низ.
г) «Конверт» или «Бабочка» в двух направлениях.
д) «Восьмерка» в двух направлениях: лежащая горизонтально на уровне
глаз, вертикальная и лежащая у ног.
е) Взгляд на: кончик носа - вперед вдаль; переносицу - вперед
вдаль; межбровье - вперед вдаль.
ж) «Циферблат» перед собой по часовой стрелке и против часовой
стрелки.
з) «Циферблат» на потолке в двух направлениях.
и) «Циферблат» с закрытыми глазами: голова в положении прямо;
голова запрокинута вверх.
4. Закрепление нового материала: интерактивный кроссворд «АХОВ».

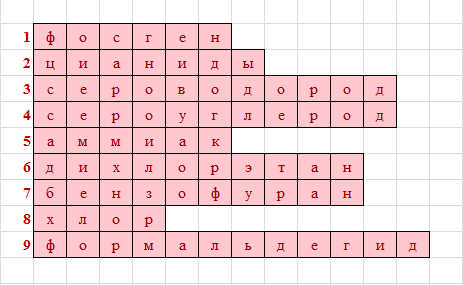
5. Подведение итогов, оценивание учащихся.
6. Домашнее задание. 1 группа: Подготовить сообщение о химически опасных объектах Иркутской области. 2 группа: Внимательно изучите рекомендации специалистов МЧС России по правилам безопасного поведения в условиях химической аварии. Сформулируйте свои действия, направленные на обеспечение химической безопасности в месте вашего проживания. Согласуйте основные моменты своего поведения с родителями. Запишите порядок действий в различных ситуациях в дневник безопасности. Разработать памятку для населения.
7. Рефлексия.
Используемые материалы для урока:
-
Рабочая программа по курсу «Основы безопасности жизнедеятельности» составлена на основе программы для общеобразовательных учреждений: Основы безопасности жизнедеятельности: 5-11 классы/ А.Т. Смирнов, Л.П. Анастасов, Б.О. Хренников и др.; Под общ. ред. А.Т. Смирнова. М.: Просвещение, 2011 - 112с. в соответствии с учебником для общеобразовательных учреждений «Основы безопасности жизнедеятельности: 8 класс», Смирнов А.Т., Хренников Б.О. М.: Просвещение, 2010 год
-
«Основы безопасности жизнедеятельности: 8 класс», Смирнов А.Т., Хренников Б.О. М.: Просвещение, 2010 год
-
Кроссворд «Радиация»,nsportal.ru/shkola/osnovy-bezopasnosti-zhiznedeyatelnosti/library/2013/08/20/urok-opasnye-khimicheskie.
-
Презентация из коллекции «videouroki.net.»: «Опасные химические вещества и объекты».
-
Материалы обучающихся: Группа 1. Аммиак (международный код - 1005). Группа 2. Хлор. Группа 3. Ртуть. Группа 4. Серная кислота. Группа 5. Соляная кислота. Группа 6. Сернистый ангидрид. Группа 7. Сероводород. Группа 8.
-
Физкультминутка. Гимнастика для глаз: festival.1september.ru/articles/515569/</</p>
-
Собственный интерактивный кроссворд по АХОВ.
-
Учебник по ОБЖ, 8 класс