- Учителю
- Конспект урока 'Основания' (на ошибках учимся) 8 класс
Конспект урока 'Основания' (на ошибках учимся) 8 класс
Конспект урока
За участие в конкурсе на Сайте Школьник ру я получила Диплом I степени. (№1224 стр. 13)
Тема. Основания (на ошибках учимся).
Класс. Предмет. 8 класс, химия, учебник «Химия» О.С. Габриелян.
Автор. Антонова Ольга Викторовна, учитель химии, МБОУ СОШ №9 г. Амурска, Хабаровского края
Тип урока. Комбинированный урок, коррекция знаний, умений и навыков.
Вид урока. Изучение нового материала. Технологический прием «На ошибках учимся»
Тема урока: Основания.
Цель урока: создание условий для того, чтобы, познакомить учащихся с составом, названиями, классификацией и отдельными представителями оснований; дать представление о качественных реакциях на примере щелочей; выяснить основой для получения каких соединений используют основания; продолжить знакомство с основными правилами техники безопасности при проведении лабораторных опытов, показать значение важнейших представителей гидроксидов в природе и жизни человека.
Задачи:
-
Образовательная - сформировать новое понятие «основания». Научить учащихся пользоваться таблицей «Растворимости», проводить лабораторные опыты, соблюдая правила Т.Б.
-
Развивающая - развивать:
- способность различать формулы оснований.
- выделять главное, сопоставлять факты, анализировать, высказывать свою точку зрения и отстаивать её по проблеме урока.
- находить пути и способы решения экспериментальных задач, используя химические вещества.
-
Воспитательная - продолжить формирование мировоззренческих понятий о познаваемости природы, причинно следственной зависимости между строением и свойствами простых веществ.
План урока.
1. Организационный момент -1 минута.
2. Актуализация знаний - 5 минут
3. Изучение нового материала - 30 минут
4. Физминутка- 1 минута
5. Закрепление новой темы - 6 минут
6. Подведение итогов - 1 минуты
7. Рефлексия - 1 минута.
Оборудование и реактивы:
на столах учащихся - пробирки №1 - соляная кислота, №2- гидроксид натрия, №3 - вода, стеклянная трубочка, салфетка, стакан с водой, метилоранж, чашка Петри, пробирка №4 - молоко, 2 ватные палочки, фарфоровая чашечка с жидким мылом;
на столе учителя - кристаллические вещества: гидроксид натрия, гидроксид калия, гидроксид бария, пробирки с пробками, вода, индикаторы.
Список использованных источников информации.
1. Габриелян о.С. Химия 8 класс: учебник для общеобразовательных учреждений/ О.С. Габриелян. - 13-е издание. Исправленное - М.: Дрофа. 2008. -270
2. Габриелян О.С. Методика преподавания химии
3. Чернобельская Г.М. Методика обучения химии в средней школе / Г.М. Чернобельская Г.М. -М.: Владос, 2000, 336 с.
4. Иванова Р.Г. Общая методика обучения химии в школе/ Р.Г.Иванова, Городилова Н.А., Добротин Д.Ю.и др.; под ред. Р.Г. Ивановой. - М.: Дрофа, 2008 - 319 с.
5.Единая коллекция ЦОР- Анимация «Правила Т.б. при работе со щелочами»-
6.Занимательная химия -
Ход урока
(фотографии размещены с согласия родителей учащихся)
-
Организационный момент.
Учитель настраивает учащихся на урок и сообщает, что урок пройдет под девизом: «На ошибках учимся». Желаю вам работать в атмосфере сотрудничества, взаимопомощи и добра. Каждый из вас сам оценит свой труд, а для этого у вас на столах лежат «Рабочие листы», который вы дополните нужными записями. После проверки он останется у вас как пособие-памятка. («Рабочий лист». Приложение 1).

II. Актуализация знаний (фронтальная работа).
Устный опрос:
-
Что такое бинарные соединения?
-
Что такое оксиды?
Учитель приглашает одного ученика для выполнения задания на доске.
Задание. Из предложенного списка выбрать и подчеркнуть оксиды. ZnO Fe(OH)2 SO3 LiOH MgO KOH Cl2O7 Ag2O NaOH.
Все остальные выполняют задание №1 в «Рабочем листе». Задание: в схеме «Классификация оксидов» найдите ошибки и исправьте их. Дайте названия оксидам по международной номенклатуре.
Оксиды металлов Оксиды неметаллов
Na2O SО2
H2О ВаО
CuO СаО
N2O5 Fe2O3.
После выполнения задания учитель организует проверку выполненной работы, заслушивает ответы учащихся, корректирует их и открывает слайд 1 с ответами (Презентация к уроку).
Учащиеся проверяют выполненное задание на доске. Учитель делает вывод и переходит к изучению новой темы.
-
Изучение нового материала.
Учитель вводит учащихся в тему урока, говоря о том, что им сегодня предстоит еще раз убедиться, что химия многолика.
Учитель. Знаете ли вы, чем мыли волосы женщины в Древней Руси? И сам же отвечает: "Раствором золы". А рецепт был такой: взять ковш золы, да не простой, а еловой или от подсолнечника, замочить в дубовом ведре ключевой или дождевой водой. Постоит такая смесь сутки, потом ее надо процедить или просто слить верхний слой, развести фильтрат чистой водой, подогреть на камельке в рубленой бане и вымыть косы. Потому, что полученный раствор, мыльный на ощупь - это средство под названием "щелок". Я вспомнила о нем потому, что реакция среды раствора щелока такая же, как и растворов веществ, которые мы начинаем изучать.
Сегодня мы будем изучать третий класс неорганических соединений. Попробуйте назвать тему урока. Учитель корректирует ответы учеников и объявляет тему урока.
Тема. Основания.
Домашнее задание §19 №.1,2
Учитель. Какие ассоциации возникают у вас со словом «основания»?
Ответы учеников: основа, основание подо что-то, фундамент.
Учитель. Верно. Беря за основу эти слова, попробуйте сформулировать цель урока.
Цель урока. Изучение свойств оснований и выявление основой чего они служат (учащиеся записывают тему, цель и домашнее задание в «Рабочем листе», учитель открывает слайд 2).
Учитель. Обратите внимание на формулы, которые остались не подчеркнутыми на доске и у вас в «Рабочих листах». Что в них общего?
Данные вещества состоят из трех химических элементов. Кроме бинарных соединений, существуют сложные вещества, состоящие из 3 элементов. К таким соединениям относятся основания.
Основой жизни на Земле является вода. Слово основание - однокоренное слово со словом основа. И наверно не случайно вода является основой для образования класса неорганических соединений - основания.
Молекулы оснований содержат атомы металла и атомы кислорода и водорода в виде гидроксогруппы ОН- (учащиеся записывают определение в тетрадь). Этот ион ОН- всегда пишется вместе, кислород и водород в гидроксогруппе не разъединяются. Гидроксогруппа - имеет постоянную валентность равную единице или С.О. -1.
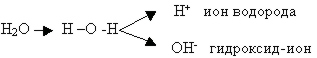
Помогите мне выразить общую формулу оснований. (После обсуждения учащихся). Учитель записывает на доске М(ОН)n, где М - металл, п - число гидроксогрупп, и одновременно валентность металла.
У нас есть вещества, есть их молекулярные формулы. А как же называется каждое из них? Каждый человек имеет свою фамилию, имя, отчество. Так и химические соединения имеют свое название в «Рабочих листах» есть схема образования названий оснований.
Название оснований.
слово "гидроксид"
+
название металла в родительном падеже
+
(римская цифра, обозначающая числовое значение степени окисления металла) для металлов с переменной степенью окисления.
Учитель организует работу с учебником. На странице 98 учебника записаны примеры оснований, назовите их: NaOH-гидроксид натрия, Са(ОН)2-гидроксид кальция, Fe(OH)3-гидроксид железа (III).
А теперь я дам названия основаниям, вы их видите в задании №2, ваша задача найти ошибку в названиях оснований (формулы на доске и в «Рабочем листе»).
Задание №2 «Лови ошибку»
Формула
Название с ошибкой
Ответы учеников
Fe(OH)2
гидроксид железа
гидроксид железа (II)
LiOH
гидроксид лития (I)
гидроксид лития
KOH
основание калия
гидроксид калия
NiOH
гидроксид натрия
гидроксид никеля
Учитель. Выполните задание из коллекции ЦОР для этого откройте презентацию слайд 3и перейдите ссылке
Задание №3. Составьте формулы оснований (учитель оказывает помощь ученикам).
Учитель. А теперь познакомимся с физическими свойствами оснований (учитель демонстрирует растворение гидроксида калия и натрия в воде). Рассуждает вместе с учениками: основания - это белые, твердые, гигроскопичные вещества, они жадно поглощают воду из воздуха, расплываясь постепенно в сиропообразную массу. Растворимые в воде основания называются щелочами. Щелочи - едкие вещества они разъедают кожу и ткани. Поэтому технические названия некоторых из них указывают на это свойство. Например: NаОН - едкий натр, КОН - едкий кали. Однако большинство оснований в воде не растворяются. Обращаться со щелочами нужно очень осторожно.
Прослушайте правила техники безопасности при работе со щелочами, а затем выполните задание №4 «Найди ошибки в тексте».
Единая коллекция ЦОР. Правила Т.Б. при работе со щелочами
Учитель организует проверку выполненного задания №4.
 Чтобы выяснить растворимость оснований в воде ребята сейчас вы проведете лабораторный опыт. Задание №5 Лабораторный опыт №1 «Получение гидроксидов меди (II) и железа (III)».
Чтобы выяснить растворимость оснований в воде ребята сейчас вы проведете лабораторный опыт. Задание №5 Лабораторный опыт №1 «Получение гидроксидов меди (II) и железа (III)».
После выполнения и обсуждения задания №5.
Учитель. Опытным путем мы определили отношение оснований к воде. На основании полученных данных выполните задание №6, предложите классификацию оснований, составьте схему и приведите примеры.
Учитель заслушивает учащихся, корректирует ответы, составляет схему на доске.
Задание № 6
Классификация оснований (по растворимости в воде)

Растворимые (щелочи)
Малорастворимые
Нерастворимые
Правильность ваших рассуждений можно проверить по таблице (учитель просит открыть таблицу растворимости в учебнике и рассказывает учащимся, как ей пользоваться).
Учитель. Существует еще две классификации оснований, в основе одной лежит основность (количество гидроксогрупп), а другой отношение к электрическому току (сильные и слабые).
Как же отличить щелочи от воды или кислоты, если эти вещества бесцветны и не имеют запаха?
Учитель просит учащихся открыть учебник, рассмотреть таблицу «Изменение окраски индикаторов» объясняет, как можно применять её для определения веществ.
Далее предлагает выполнить задание №7. Лабораторный опыт №2 «Проверьте утверждение». Проверить верно, ли указаны номера пробирок, в которых содержатся кислота, щелочь и вода используя только один реактив.
Учитель после обсуждения ответов учащихся помогает сформулировать вывод.
 Учитель рассказывает, что для определения щелочей, есть еще одна качественная реакция и приглашает 2 учеников, помочь провести опыт. (Взаимодействие оксида углерода (IV) с гидроксидом кальция в двух вариантах). Учитель записывает схему уравнения реакции на доске, а учащиеся в «Рабочих листах».
Учитель рассказывает, что для определения щелочей, есть еще одна качественная реакция и приглашает 2 учеников, помочь провести опыт. (Взаимодействие оксида углерода (IV) с гидроксидом кальция в двух вариантах). Учитель записывает схему уравнения реакции на доске, а учащиеся в «Рабочих листах».
Са(ОН)2 + СО2 = СаСО3 + Н2О
известковая вода соль
Вывод: Растворимые в воде основания изменяют окраску индикаторов. Под действием углекислого газа известковая вода (гидроксид кальция) мутнеет - это качественная реакция на CO2 и Ca(OH)2.
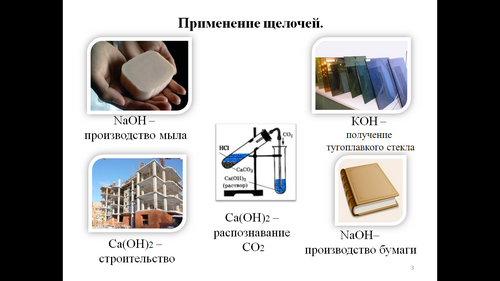
Учитель. Мы познакомились еще с одним классом сложных веществ - основаниями. Как вы думаете, имеют ли основания практическое значение? Конечно же, да Внимательно послушайте сообщение о применение щелочей и выполните задание №8 «Установите соответствие», исправив ошибки.
Сообщение ученицы (слайд 3). Гидроксид натрия применяют в производстве мыла, в кожевенной промышленности, в фармацевтике и в производстве бумаги. Гидроксид калия используется при "варке" тугоплавкого стекла, производстве бумаги и жидкого мыла. Гидроксид кальция в смеси с медным купоросом для борьбы с возбудителями грибковых заболеваний плодовых, овощных и декоративных культур. Он применяется для распознавания углекислого газа.
Заполненную схему, учитель проверяет после сдачи «Рабочего листа».
Учитель. Сейчас вам предстоит провести небольшое исследование и объяснить наблюдаемое явление. Это эвристическое задание, оно поможет определить, как вы можете применять полученные знания не в стандартной ситуации.
Задание №9. На каком свойстве основано применение щелочей в качестве жидкого мыла?
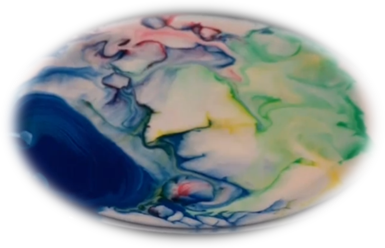
Тема. Рисуем на молоке.
Учитель. Откройте слайд в презентации
(после обсуждения ответов учитель объясняет суть опыта) при добавлении краски в молоко и жидкого мыла на поверхности образуются неожиданные рисунки, мыло, содержащее щелочь, растворяет жир, содержащийся в молоке. Т.к. капельки жира плавают в молоке хаотично, то и растворение его происходит неравномерно.
IV Закрепление.
Учитель. В начале урока мы сформулировали цель «Изучение свойств оснований и выявление основой для чего они служат», с какими свойствами оснований мы сегодня познакомились? (физическими и химическими)
Чтобы ответить на вторую часть вопроса обратите внимание на схемы уравнений реакций в задании №5 и №7, какие вещества образуются в реакциях со щелочами? (соли)
Вывод: основания являются основой для получения солей. Их мы будем изучать на следующем уроке.


Что бы проверить как вы усвоили материал урока, выполните задание №10 - тест. В тесте отмечены ответы, если ты не согласен исправь их.
Тест. «Исправьте ошибки»
1.При обычных условиях основания это
-
твердые вещества
-
жидкости
-
газообразные вещества
-
могут быть твердыми, жидкими и газообразными
2.В растворах щелочей лакмус меняет свой цвет соответственно на…
-
фиолетовый на красный
-
фиолетовый на синий
-
фиолетовый на желтый
3.Хорошо растворимы в воде все основания группы:
-
KOH, Ca(OH)2, NaOH
-
LiOH, KOH, Al(OH)3
-
NaOH, KOH, Ba(OH)2
4.Формула щелочи - это:
-
Zn(OH)2 b) KOH c) Cu(OH)2 d) Mg(OH)2
Ответ: 1 а 2 а 3 с 4 b
V Итог урока
В ходе сегодняшнего урока изучая новую тему, вы выполняли задания, находили и исправляли ошибки. Прочитайте цитату Хань Сян-цзы в «Рабочих листах», выскажите своё мнение: можно ли исправляя ошибки других, научится самому. После высказываний учеников учитель подводит итог урока, выставляет оценки за работу.
VI Рефлексия
Задание №11. Выберите предложение, которое отражает ваше настроение, и подчеркните его.
-
Урок полезен, все понятно.
-
Лишь кое-что чуть-чуть не ясно.
-
Еще придется потрудиться.
-
Да, трудно все-таки учится!
Приложение 1
Рабочий лист.
«Тот, кто правильно указывает на мои ошибки
- мой учитель.
Тот, кто помогает мне увидеть мои ошибки
- мой друг.
Тот, кто мне льстит - мой враг».
ХаньСян-цзы - китайский философ 760г.
Тема.________________________________
Цель.________________________________________________________________________
_____________________________________________________________________________Д.З. §_____№
Задание №1«Найди ошибку».
В схеме «Классификация оксидов» найдите ошибки и исправьте их. Дайте названия оксидам по международной номенклатуре.
Классификация оксидов
Оксиды металлов Оксиды неметаллов
1.Na2O _____________ А. SО2 ____________
2.H2О ______________ Б. ВаО ____________
3.CuO ______________ В. СаО ____________
Подчеркните оксиды: KOH N2O5 Fe(OH)2 Fe2O3 Al(OH)3 CO2
Основания - это______________________________________________________________
_____________________________________________________________________________
Общая формула оснований______________
Название оснований
слово "гидроксид"
+
название металла в родительном падеже
+
(римская цифра, обозначающая числовое значение степени окисления металла) для металлов с переменной степень окисления
Задание №2 «Лови ошибку». Найди ошибки и исправь их в названиях, которые будет давать приведенным ниже соединениям учитель.
-
Fe(OH)2-гидроксид железа____________________________
-
LiOH- гидроксид лития (I)____________________________
-
KOH - основание калия_____________________________
-
NiOH - гидроксид натрия _____________________________
Задание №3. Составьте формулы оснований.
Гидроксид меди_______________
гидроксид бария_______________
гидроксид алюминия___________
Задание №4 «Найдите ошибки в тексте»
Правила Т.Б. со щелочами.
Несоблюдение правил работы со щелочами не приводит к сильным химическим ожогам. При воздействии на кожу концентрированных растворов едких щелочей образуются светло-желтые пятна.
Твердые едкие щелочи, притягивая влагу, содержащуюся в воздухе, легко переходят в раствор, поэтому действие их не расценивается как действие щелочей.
Твердые щелочи можно брать незащищенными руками, для этого используются фарфоровые ложечки или шпатели. Большие куски едких щелочей раскалывать на мелкие кусочки могут ученики с применением защитных очков и перчаток.
Растворять щелочи следует в фарфоровой посуде путем медленного прибавления к воде небольших порций при постоянном помешивании.
Насыпать или наливать щелочи следует как обычные вещества.
Для нейтрализации пролитых на стол щелочей используйте заранее приготовленный 50% раствор уксусной кислоты.
При нагревании жидких щелочей можно заглянуть в пробирку, т.к. это не может привести к несчастному случаю.
Остатки щелочей и веществ после опытов сливают в раковину.
Задание №5. Лабораторный опыт №1
Тема. Получение гидроксидов меди (II) и железа (III)
Техника безопасности при работе со щелочами

![]()
![]()

-
На лабораторное стекло с помощью стеклянной трубочки нанесите 1-2 мл сульфата меди (CuSO4) из бутылочки.
-
С помощью стеклянной трубочки к сульфату меди добавьте 1-2 мл гидроксид натрия (NaOH) из бутылочки.
-
Что вы наблюдаете? По каким признакам можно судить, что произошла реакция? К полученному веществу добавьте 3мл воды.Что вы наблюдаете? Сделайте вывод о растворимости гидроксида меди.
-
На лабораторное стекло с помощью стеклянной трубочки нанесите 1-2 мл хлорида железа (FeCl3) добавьте 1-2 мл гидроксид натрия (NaOH) из бутылочки.
-
Что вы наблюдаете? По каким признакам можно судить, что произошла реакция?К полученному веществу добавьте 3мл воды.Что вы наблюдаете? Сделайте вывод о растворимости гидроксида железа.
CuSO4 + __NaOH =____________ + Na2SO4 _________________________________
соль + щелочь = основание + новая соль
FeCl3 _+ NaOH =____________ + 2NaCl
Задание №5. Составьте схему классификации оснований. На лепестках напишите примеры оснований.
Классификация оснований (по растворимости в воде)

_______________ ___________________ ______________
Задание № 7. «Проверьте утверждение»
Лабораторный опыт №2
Тема. Определение реакции среды растворов
-
В трех пронумерованных пробирках находятся вещества №1 вода, №2 щелочь, №3 кислота. Проверьте это утверждение, используя только один реактив. Что наблюдаете?
-
Объясните полученные результаты.
Вывод: пробирка №1 -_________, пробирка №2 -_________ пробирка №3 -_____________
Качественная реакция на гидроксид кальция с углекислым газом.
Реакции, с помощью которых распознают определенные вещества, называют качественными.
Са(ОН)2 + СО2 = СаСО3 + Н2О
известковая вода соль
Задание №8. «Установите соответствие», исправив ошибки.
Применение оснований
Вещества

Применение
А
 . Гидроксид натрия
. Гидроксид натрия
В . Гидроксид калия
. Гидроксид калия
С. Гидроксид кальция
-
В строительстве
-
В быту
-
Изготовление мыла
-
Производство бумаги
-
Распознавание углекислого газа
Ответ: А-_____________ В -__________ С - __________
Задание №9. Лабораторный опыт №3
Тема. Рисуем на молоке
1. В чашку Петри налейте молоко из пробирки №4.
2. Капните по несколько капель разноцветных красок в молоко по центру чашки Петри.
3. Обмакните две ватные палочки в жидкое мыло (фарфоровая чашечка) и погрузите их в молоко.
4. Что наблюдаете? На каком свойстве основано применение щелочей в качестве жидкого мыла?
Задание №10. Тест «Исправь ошибки». В тесте отмечены ответы, если ты не согласен исправь их и укажи свой ответ.
1.При обычных условиях основания
-
твердые вещества
-
жидкости
-
газообразные вещества
-
могут быть твердыми, жидкими и газообразными
2.В растворах щелочей лакмус меняет свой цвет соответственно на
-
фиолетовый на красный
-
фиолетовый на синий
-
фиолетовый на желтый
3.Хорошо растворимы в воде все основания группы:
-
KOH, Ca(OH)2, NaOH
-
LiOH, KOH, Al(OH)3
-
NaOH, KOH, Ba(OH)2
4.Формула щелочи - это:
-
Zn(OH)2 b)KOH c)Cu(OH)2 d)Mg(OH)2
Рефлексия.
Задание №11.Выбери предложение, которое отражает твое настроение.
Урок полезен, все понятно.
Лишь кое-что чуть-чуть не ясно.
Еще придется потрудиться.
Да, трудно все-таки учится!
Приложение 2
Презентация.

Слайд 2

Слайд 3
13