- Учителю
- Конспект по химии:состав и строение атома
Конспект по химии:состав и строение атома
Тема: состав и строение атома
Класс: 8 «Б»
Дата:
Цель: сформировать компетентность учащихся по теме на основе межпредметных связей (физика и химия) в умении применять знания.
Задачи:
-
Образовательные - изучить строение, состав атомных ядер, изотопы
-
Развивающие - развивать научное мышление при установлении причинно-следственных связей, сравнении химических объектов, применении знаний и умений в новых ситуациях, в том числе, для решения межпредметных проблем; развивать интерес и другие мотивы изучения химии при знакомстве с историей становления идеи о делимости атома в науке и научными работами ученых.
-
Воспитательная - формировать умение работать с книгой через групповую работу, воспитание чувства сотрудничества, сотворчества, создание условий для реальной самооценки учащихся.
Тип урока: урок изучения нового материала и первичного закрепления новых знаний.
Оборудование: периодическая система химических элементов Д.И.Менделеева, электронная презентация к уроку.
Ход урока
1. Мотивационно-ориетировочный этап.
Учитель:
-
Вспомните, что изучает химия?
-
Из чего состоят вещества?
-
Что такое химический элемент?
Итак, мы знаем, что мельчайшей частицей вещества является атом: одинаковые атомы, или атомы одного вида, называются химическим элементом (запись в разделе "Что мы знаем?" Приложение № 1)
Слово "атом" придумал очень давно, более 2500 лет назад, древнегреческий философ Демокрит. С греческого "атом" переводится как "неделимый". Так ли это?
Прочтите, пожалуйста, поэтические строчки:
(Информация № 1 в Приложении № 2, Слайды 1, 4, 5.)
Элементы встали вряд,
В ядрах их растет заряд.
Значит столько в нем протонов,
А в округе - электронов.
Есть в ядре еще нейтроны,
Что заряд иметь не склонны.
Ну а то, что в массе дробь,
В том виновен изотоп.
-
Что вы узнали из данной информации?
-
Смысл каких слов вам не понятен?
-
Как вы думаете, о чем пойдет речь на сегодняшнем уроке?
-
Найдите в информации в состав чего входят протоны, электроны, нейтроны?
-
Сформулируйте тему урока (запись темы на доске).
-
Каковы цели сегодняшнего урока? (Запись на доске в разделе "Что хотим узнать?" Приложение № 1, Слайды 1,2,3.)
2. Актуализация знаний по вопросу: История изучения состава атома.
Учитель: В истории развития физики одна из самых интересных и увлекательных страниц - это история открытия сложного строения атома. В конце ХI - начала ХII в. идеи о строении атома витали в воздухе, различные догадки ученых создавали духовную атмосферу, в которой, в конце концов, и рождалось открытие, ведь в это время ничего о внутреннем строении атома не было известно.
Какими же великими открытиями была доказана сложность строения атома?
Для этого вам предстоит прочесть материал учебника (с. 38-40) и осуществить описание по плану:
А) Открытие физика Д.Стони_________________________________
_____________________________________________________________
Б) Открытие физиков Д.Томсона и Ж.Перрена
(Дорисуй модель, укажи размеры.)
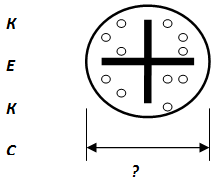
В) Открытие физика А.Беккереля_________________________________________________
Г) Схема опыта Э. Резерфорда.
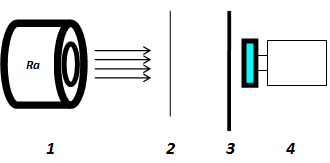
Заполни:
1. -_______________ ;
2. -_______________ ;
3. -_______________ ;
4. -_______________ .
(Дорисуй возможные дальнейшие направления движения ά- частиц.)
Д) Планетарная модель атома
1-________________________________
2-________________________________
(Укажи размеры атома.)
(Последующее обсуждение вопросов. Просмотр Слайдов 6, 7. Самооценка и выставление баллов в карту оценки участия в уроке по 3 бальной шкале.)
Учитель: Какой вывод можно сделать из полученной информации? (В начале 20 в. разрушились представления о неделимости атома. Атом - сложная частица.)
3. Операционно-исполнительский этап (работа в группах).
Учитель: Используя информацию № 2 в Приложении № 2 и наглядный материал " Как устроен атом" (из серии электронных учебных пособий), докажите сложность строения атома, для этого вставьте пропущенные слова в тексте:
-
Модель атома, предложенная Резерфордом, называется …
-
Атом - это частица, состоящая из …
-
В состав ядра атома входят … и …
-
Протон - элементарная частица, имеющая массу приблизительно … и заряд равный … Для протона принято обозначение…
-
Ядро атома имеет… заряд
-
Нейтрон - элементарная частица, имеющая массу приблизительно … и заряд равный … Для нейтрона принято обозначение…
-
Вокруг ядра постоянно движутся …, их заряд - …, а масса - …
-
Масса атома сосредоточена в …, т.к. массой … можно пренебречь.
-
Атом электронейтрален, т.к. …
-
По разности … определяют число нейтронов в атоме.
Учитель: Что у вас получилось? (Устные ответы учащихся. Запись на доске в разделе Что узнали? Выставление оценок в карту оценки участия в уроке по 3 бальной шкале. Просмотр Слайдов 8-10.)
Учитель: По полученному тексту попытайтесь составить схему строения атома (работа в группах).
(Учитель проходит по рядам и выясняет: какая из схем более полно и точно отражает строение атома. Более точная схема выносится на доску или показывается соответствующий слайд презентации.)
Учитель:
1. Как вы понимаете задание: определить состав атома?
2. Попытайтесь составить алгоритм, т.е. порядок действий, который
позволит определить состав атома. Я дам вам подсказки, а вы
расставьте их в нужном порядке (Что значит, определить состав
атомных ядер? Как можно определить число протонов, нейтронов? Как
найти количество электронов в атоме?)
Учитель: Какие последовательности у вас получились? (на слайде№11 выводится алгоритм, демонстрируется пример):
-
N = - см. ПСХЭ
-
N = Z = число р+
-
Число n0 = Ar - Z
-
Число е = числу р+
Учитель: Используя данный алгоритм, выполните задание: заполните таблицу. (Каждый участник команды выполняет одно задание и карточку передает другому ученику.)Подводится итог: за правильно выполненное задание выставляются баллы (взаимопроверка. Слайд 12).
Критерии оценки: без ошибок - молодец (3б.),1-2 ошибки - не все потеряно (1-2б.), 3-4 ошибки - стоит обратить на это особое внимание (0б.).
4. Формирование практических навыков.
Учитель: Нам известно, что свободные атомы - это одна из форм существования химического элемента.
Другого ничего в природе нет,
Ни здесь, ни там, в космических глубинах:
Все от песчинок малых до планет -
Из элементов состоит единых.
В настоящее время известно 114 химических элементов, получены первые атомы элемента с номером 116. Давайте обратимся к периодической системе химических элементов Д.И.Менделеева и посмотрим, какими числами представлены в ней относительные атомные массы элементов? Если масса атома определяется количеством протонов и нейтронов, массы которых выражены целыми числами, то почему относительные атомные массы представляют собой дробные величины? (Постановка учебной проблемы.) На эти вопросы мы будем искать ответы в ходе мысленного эксперимента с опорой на модели.
1) Изменение числа нейтронов в атоме водорода.
Решение задачи: Что произойдет с атомами одного и того же вида,
если в их ядра мысленно добавить по 1 нейтрону?
Для примера возьмем атом с самым простым строением - атом водорода.
-
Найдите среди моделей ядро этого атома. Сколько протонов он содержит? (Один.) Эта разновидность атома носит название протий (из-за простоты строения).
-
Мысленно добавьте в этот атом 1 нейтрон. Изменилась ли масса атома? (Да, она равна массе протона и нейтрона, массу электрона из-за ее очень малой величины не учитываем.)
-
Сравните модели ядра протия и полученного атома. Такой атом водорода называют дейтерием.
-
Мысленно добавьте теперь уже в ядро дейтерия один нейтрон. (Далее рассуждения аналогичны выше изложенным.)Полученный атом называют тритием.
Итак, мы имеем три модели, три разновидности атомов водорода с различными массами.
Как же называют разновидности атомов одного и того же вида (в нашем случае - атомов водорода), имеющие один и тот же заряд ядра атома, но разные массы? Посмотрите в периодической системе химических элементов. В ней всем разновидностям атома водорода отведено одно и то же место. Поэтому, они получили название изотопы ("изос" - равный, одинаковый, "топос" - место), т. е. занимающие одно и то же место.
2) Оформление результатов мысленного эксперимента в тетрадях и на доске (Совместное заполнение таблицы и формулировка понятия "изотопы".)
Оформим результаты наших рассуждений в тетрадях.Изотопы - это … (Продолжение записи на доске в разделе "Что узнали?")
Учитель: Давайте послушаем учащегося, который расскажет, какую интересную информацию он нашел об этих изотопах.
Учащийся (рассказывает и презентует материал "Знаете ли вы",который подготовил самостоятельно дома</<font face="Times New Roman, serif">). Приблизительный вариант:
-
Протий - обычный водород, дейтерий - тяжелый водород, тритий - сверхтяжелый водород
-
Тяжелый водород содержится в обычном водороде в небольших количествах: на 5 тыс. атомов обычного водорода приходится 1 атом тяжелого.
-
Вода, в которой протий заменен дейтерием, называется тяжелой. Тяжелая вода характеризуется особыми свойствами: температура замерзания +3,8 С0, температура кипения +101,4 С0, плотность 1,1г/мл.
-
В тяжелой воде невозможна жизнь.
-
Сверхтяжелый водород в природе встречается крайне редко. Доля его ничтожно мала: один атом трития приходится на миллиард миллиардов атомов обычного водорода.
-
Тритий является радиоактивным изотопом водорода.
-
Совсем недавно появилось сообщение о новом изотопе водорода с атомной массой равной 4. Насколько трудной была задача обнаружения нового "сверхтяжелого" водорода, говорит время его существования, равное 0, 000 000 000 01 доли секунды.
Учитель: Так почему же относительные атомные массы химических элементов, указанные в периодической системе Д.И.Менделеева, не целые, а дробные величины?
Учащийся: Это средняя арифметическая величина, в которой учтены не только массы всех изотопов, но еще и процентное содержание в природе. Поэтому получаемые при расчетах величины оказываются не целыми, а дробными.
Учитель: В ядре атома химического элемента А содержится 11 протонов и 12 нейтронов, а в ядре атома химического элемента В -12 протонов и 12 нейтронов.
Определите, являются ли они:
- изотопами одного элемента;
- атомами двух химических элементов, у которых одинаковое массовое
число;
- атомами двух разных элементов, находящихся в периодической
системе рядом. (Слайд 13)
Учитель:
Собрать, сколько надо, частиц всех сортов,
И атом - пожалуйста, - вот он, готов!
Но в общее дело их вклады неравны…
Так кто же из этих частиц самый главный?
Пузатый протон, флегматичный нейтрон,
А может быть, юркий малец - электрон?
Итак, предположите, какая же частица в атоме главная? (Постановка учебной проблемы.)
Решение учебной проблемы основывается на известной учащимся информации:
-
Нейтрон? Нет, их количество может быть разным
-
Электрон? Нет, они могут быть отданы или приняты в ходе химических превращений.
-
Относительная атомная масса? Нет, она может быть различной.
Учащийся: Главной характеристикой любого химического эксперимента является содержание в нем протонов, а точнее, значение положительного заряда ядра атома, определяемое числом протонов.
Учитель: Исходя из этого, дайте современное, новое определение понятия "химический элемент".
Учащийся: Химический элемент - это совокупность атомов с одинаковым зарядом ядра.
Учитель: Итак, подведем итог. Вспомни начала урока: Что мы знали? Что хотели узнать? А что же узнали?(анализ записей на доске, получившихся к концу урока. Приложение № 1. Слайд 14)
5. Домашнее задание.