- Учителю
- Урок по химии Типы химических реакций
Урок по химии Типы химических реакций
Урок по теме
«Химические реакции. Типы химических реакций»
«Мощь и сила науки - во множестве
фактов, цель - в обобщении этого множества»
Д. И. Менделеев
Цели урока:
- закрепить и обобщить знания учащихся по изученной теме, развивать умение применять полученные знания при составлении химических формул, при проведении вычислений по химическим формулам и составлении уравнений химических реакций;
- развивать речевые навыки учащихся, умение наблюдать, анализировать, сравнивать, обобщать, выделять главное, оценивать свои знания и знания своих товарищей;
- развивать стойкий позитивный интерес к предмету, чувство ответственности не только за свои знания, но и за знания одноклассников.
Оборудование: карточки с заданиями для команд и отдельных учащихся, посуда и реактивы для проведения практических заданий, набор атомов для моделирования.
Ход урока
1. В начале урока сообщается учащимся цель урока: обобщить, систематизировать и углубить знания, проверить качество знаний.
Затем представляю экспертов и гостей, знакомлю с последовательностью выполнения заданий.
В качестве разминки организуется беседу по вопросам:
1. Что изучает химия?
2. Что является предметом изучения химии?
3. Что такое вещество?
4. На какие две группы можно разделить все вещества?
5. Какие вещества называются простыми? Пример.
6. Какие вещества называются сложными? Пример.
7. Как можно классифицировать сложные вещества?
Далее следует конкурс № 1 «Классификация веществ» для представителей команд (у доски). В это же время команда работает над заданием «Установите соответствие». Команда из слабых учеников класса моделирует физические и химические явления.
КОНКУРС 1
«Классификация веществ»
Распределите вещества по соответствующим классам
(оксиды, основания, кислоты, соли)
HNO3, CuO, Na2SO4, NaOH, P2O5, HCl, Cu(OH)2, AlCl3
Назовите вещества
(каждый правильный ответ 1 балл, максимальный балл за это задание 8 баллов)
КОНКУРС 1
«Установите соответствие»
между записями 1 - 10 и формулами а - к
Формула
1. Многокислотное основание
а) Al(OH)3
2. Кислородсодержащая кислота
б) HCl
3. Средняя соль
в) NaHS
4. Одноосновная кислота
г) BaSO4
5. Нерастворимая соль
д) CO2
6. Газообразный, кислотный оксид
е) H2SO4
7. Бескислородная кислота
ж) CuOHCl
8. Растворимое основание (щелочь)
з) H2S
9. Кислая соль
и) H2O
10. Основная соль
к) KOH
Ответ: 1 _________, 2 ________, 3 _______, 4 ________, 5 _______, 6 ______,
7 _________, 8 ________, 9 _______, 10 _______.
(каждый правильный ответ 1 балл, максимальный балл за это задание 11 баллов)
Задание
«Моделирование физических и химических явлений»
Задание 1. Сделайте из шариков 4 модели двухатомных молекул вещества. Расположите эти модели так, как будто вещество находится в твёрдом состоянии. Отодвиньте теперь немного модели молекул друг от друга. Какое явление вы сейчас смоделировали? Это физическое или химическое явление? Почему вы так считаете? _________________________________________________________________________________________________________________________________________________________
Задание 2. Смоделируйте кипение жидкости. Какое это явление? Почему?______________________________________________________________________________________________________________________________________________________________________
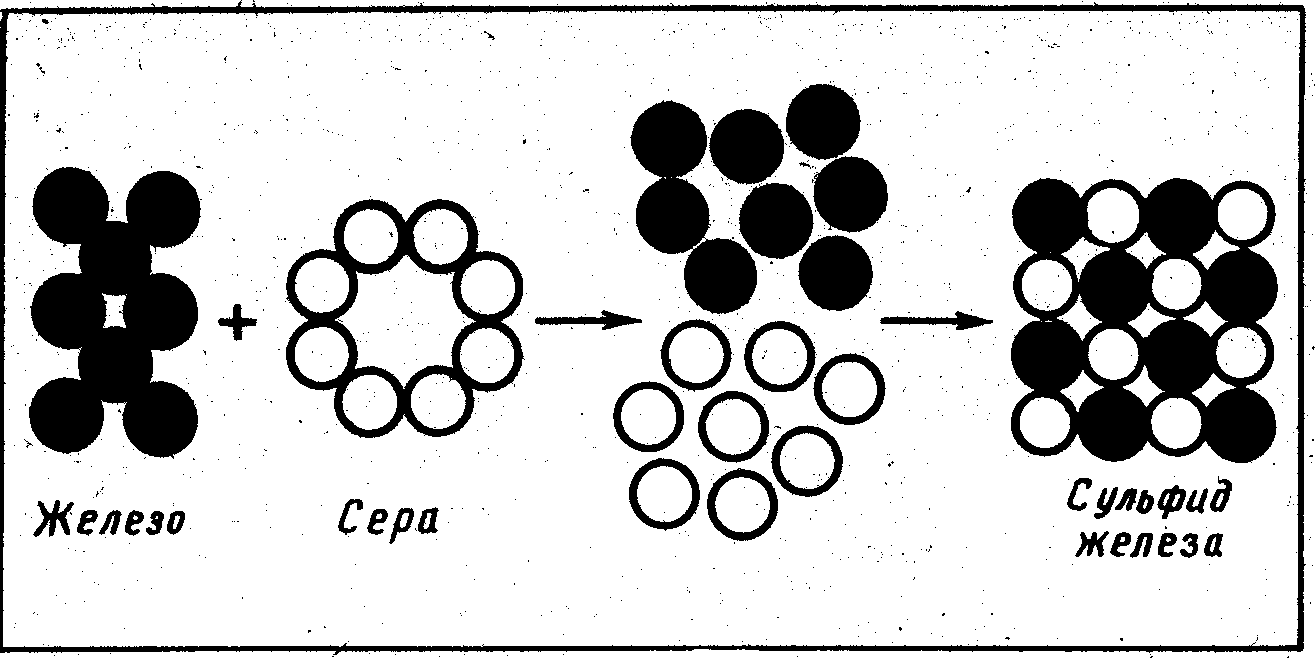
Задание 3. Изготовьте модели одного твёрдого вещества немолекулярного строения (железа) и двух восьмиатомных молекул другого вещества (серы). Смоделируйте разрушение обоих веществ до отдельных атомов (это происходит при нагревании) и соедините модели разных атомов вместе, правильно их, чередуя: атом железа, атом серы, атом железа, атом серы… Сколько новых веществ образовалось? Это простые или сложные вещества? Вы увидели сущность химической реакции между серой и железом, которую недавно проводили. Не остались ли у вас «лишние» модели каких-нибудь атомов? О чём это говорит?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Составьте уравнение химической реакции для задания № 4
_____________________________________________________________________________
Укажите тип химической реакции.
В чем сущность химических реакций?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________
По окончании выполнения работы, команды обмениваются листами с ответами и проверяют их правильность (я диктую правильные ответы), одновременно с этим от команд противников осуществляется проверка задания у доски. Подсчитываются балла.
- Что такое химическая формула?
- Что можно узнать по химической формуле?
- Что значит составить химическую формулу?
Следующий конкурс «Химическая формула» команда работает над составлением формул, для представителей команд (у доски) конкурс
«Математическая экспертиза»
КОНКУРС 2
«Химическая формула»
В конверте находятся «осколки» формул веществ, необходимо составить формулы веществ.
Al2+3, C+4, NO3 -, (NO3)3-, K+, O3-2, Al3+, O2-2
Назовите полученные вещества
(каждый правильный ответ 3 балла, максимальный балл за это задание 12 баллов)
КОНКУРС 2
«Математическая экспертиза»
Необходимо определить, какое из веществ тяжелее и во
сколько раз
KOH и KI
(максимальный балл за это задание 3 балла)
По окончании выполнения работы, команды называют, составленные формулы, дают им названия. Подсчитываются балла.
- Как можно классифицировать явления, которые происходят с веществами?
- Чем они отличаются друг от друга?
Далее следует практическое задание.
Практическое задание 3
«Физические и химические явления»
Задание. Посмотрите в своем лабораторном журнале описание лабораторной работы № ____ и практической работы № 1, 3 и ответьте на вопросы. Ответы занесите в таблицу.
Какое это явление?
Объяснение
1) Кипячение воды
2) Опускание мела в соляную кислоту
3) Нагревание парафина
4) Добавление к мылу фенолфталеина
5) Гашение негашеной извести
6) Добавление гидроксида натрия к р-ру медного купороса.
Сделайте вывод по результатам данной работы:
(каждый правильный ответ 2 балла, максимальный балл за это задание 12 баллов)
- Что такое химическое уравнение?
- Какие типы химических реакций вам известны?
Команда работает над творческим конкурсом «Выбери правильный ответ».
КОНКУРС 4
«Выбери правильный ответ»
А) SO2 + H2O = H2SO3
Б) CuSO4 + Fe = FeSO4 + Cu
В) CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Г) Ba(OH)2 + 2HCl = BaCl2 + 2H2O
Д) Na2O + H2O = 2NaOH
Е) Cu(OH)2 t= CuO + H2O
1) В результате какой реакции образуется нерастворимое вещество синего цвета?
2) В какой реакции продуктом является щелочь?
3) Какая реакция относится к реакциям замещения?
4) В уравнении какой реакции записаны формулы всех четырех классов неорганических веществ?
5) Какое уравнение соответствует схеме: сульфат меди(II) + гидроксид натрия → гидроксид меди(II) + сульфат натрия?
6) Какая реакция относится к эндотермическим реакциям?
Ответ: 1 _________, 2 ________, 3 _______, 4 ________, 5 _______, 6 ______.
(каждый правильный ответ 1 балл, максимальный балл за это задание 6 баллов)
КОНКУРС 4
«Допишите предложения» (у доски)
-
Число, показывающее количество атомов в молекуле, называют ….
-
Условная запись вещества, отражающая его количественный и качественный состав, называется ….
-
Вещества, состоящие из нескольких видов атомов, называются ….
-
Запись химической реакции с помощью химических формул - это ….
-
Явления, при которых происходит превращение одних веществ в другие, называются ….
-
Вещества, образованные одним видом атомов, называются ….
-
«Масса веществ, вступивших в реакцию, равна массе образующихся веществ» - это формулировка ….
-
Образование осадка, выделение газа, изменение окраски, выделение теплоты, появление запаха - всё это ….
-
Какие числа необходимо использовать, чтобы в уравнении реакции показать, что во взаимодействие вступают два моля вещества водорода: коэффициент, индекс?
(каждый правильный ответ 1 балл, максимальный балл за это задание 9 баллов)
По окончании выполнения работы, команды обмениваются листами с ответами и проверяют их правильность (я диктую правильные ответы), одновременно с этим представители команд осуществляют самопроверку по карточкам с ответами. Подсчитываются балла.
- Вы знаете, что вещества бывают опасными, и чтобы жизнь ваша не была в опасности, нужно знать правила безопасности.
ТЕСТ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ 5
1. Как ПОЛОЖЕНО себя вести в школьной химической лаборатории?
А. Можно перекусить.
Б.Можно смешивать реактивы, не пользуясь инструкцией.
В. Можно бегать и шуметь.
Г. Следует соблюдать на рабочем месте чистоту и порядок.
2. Когда можно приступать к работе в лаборатории?
А. Когда хочешь.
Б. С разрешения лаборанта.
В. С разрешения учителя.
Г. Когда будешь готов.
3. Какую посуду надо использовать при работе?
А. Чистую.
Б. Грязную.
В. С трещинами.
Г. Какая есть, ту и использовать.
4. При нагревании жидкости в пробирке отверстие надо направлять...
А. Вверх.
Б. В сторону от себя.
В. Вниз.
Г. В сторону от себя и от соседей.
5. Что надо сделать в случае попадания влаги на электроприбор?
А. Вытереть прибор тряпкой.
Б. Выключить прибор.
В. Позвать учителя.
Г. Работать дальше.
6. Чего нельзя делать при работе со спиртовкой?
А. тушить огонь колпачком.
Б. Зажигать спичками.
В. Заполнять этиловым спиртом.
Г. Зажигать от другой спиртовки.
(каждый правильный ответ 1 балла, максимальный балл за это задание 6 баллов)
Конкурс 5
Задание. Налейте раствор из сосуда в пробирку
Оборудование: раствор хлорида натрия в склянке с этикеткой; пробирка.
Критерии оценки
• Этикетка на склянке должна быть вверху (этикетка в руке).
• Последнюю каплю жидкости снять горлышком пробирки.
• Не наполнять пробирку более чем на одну треть.
Конкурс 5
Задание. Определите запах вещества.
Оборудование: химический стакан с 6%-ньтм раствором уксусной кислоты.
Критерий оценки
• Нюхать с предосторожностями.
Конкурс 5
Задание. Возьмите сыпучие реактивы из банки.
Оборудование: банка с порошком мела; пробирки, ложечки.
Критерий оценки
• Аккуратность при работе.
Конкурс 5
Задание. Зажгите и потушите спиртовку.
Оборудование: спиртовка, спички.
Критерий оценки
• Зажигать спичками, тушить колпачком.
Конкурс 5
Задание. Нагрейте воду в пробирке до кипения.
Оборудование: штатив с лапкой, пробирка, спиртовка, спички.
Критерии оценки
• Правильность зажима пробирки в лапке штатива.
• Правильность расположения отверстия пробирки (от себя и от соседей).
• Правильность нагревания жидкости в пробирке.
КОНКУРС 6
«Химическая экспертиза»
Самостоятельное исследование по проблеме: в какой пробирке (№ 1, № 2 или № 3) находится кислота и щелочь, если молекулярные формулы этих веществ соответственно НСl и NaOH.
1) Сформулировать проблему
2) Выявить объект и предмет исследования
Объект - сложное вещество, состоящее из ионов Н+ и кислотного остатка, сложное вещество, состоящее из гидроксид - ионов ОН- и ионов металла
Предмет - свойства этих веществ
3) Выдвинуть гипотезу
Если в молекуле вещества есть ионы ____________, то индикатор _________ должен менять цвет (становится ______________). Следовательно, выданное вещество в пробирке № ____ является _____________.
4) Провести экспериментальное исследование
5) Сделать вывод
С помощью химического эксперимента гипотеза подтверждена:
В пробирке № ____ находится соляная кислота, а в пробирке № ____ - гидроксид натрия.
Команды получают по 5 баллов за правильно выдвинутую и доказанную гипотезу.
На этом этапе проверяем работу пятой команды. Оцениваем их ответы.
Кроссворд 7
1) H2 + O2 → …
2) Fe + CuCl2 → … + FeCl2
3) Fe + … → FeS
4) … + O2 → MgO
1
2
3
4
(каждый правильный ответ 1 балла, максимальный балл за это задание 4 баллов)
Конкурс 7
«Химические процессы вокруг нас»
Расставьте коэффициенты, определите типы химических реакций
а) СrO3 + Al - А12O3 + Сr;
б) НI - Н2 + I2;
в) Al + S - Al2S3
г) Nа2O + НСI - NаС1 + Н2O
(каждый правильный ответ 2 балла, максимальный балл за это задание 8 баллов)
д) Сu + ? - СuО;
е) СuО +? - CuCl2 + Н2O
(каждый правильный ответ 3 балла, максимальный балл за это задание 6 баллов)
Конкурс
практиков и экспериментаторов
Ученик должен был взять для реакции 0,5 моль серы. Он взвесил на весах 8 г серы. Правильно ли он выполнил задание? Сколько грамм оксида серы (IV) образуется из 0,5 моль серы в результате этой реакции?
В ходе урока эксперты заполняют аттестационный лист каждой команды, подводят окончательные итоги. Команда, набравшая наибольшее количество баллов и занявшая первое место получает оценку «5», команда, занявшая второе место - «4»
Тест по теме
ХИМИЧЕСКИЕ РЕАКЦИИ
1. ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ ПРИ ХИМИЧЕСКИХ РЕАКЦИЯХ УСТАНОВИЛ
а) М. В. Ломоносов б) Д. Дальтон в) Д. И. Менделеев г) А. Беккерель
2. МАССА ПОРОШКА АЛЮМИНИЯ, СГОРАЮЩЕГО В КОЛБЕ С КИСЛОРОДОМ,
а) увеличится б) уменьшится в) не изменится
г) сначала увеличится, а потом уменьшится
3. СУММА КОЭФФИЦИЕНТОВ В УРАВНЕНИИ РЕАКЦИИ
NаОН + СuSO4 - Nа2SO4 + Сu(OН)2 РАВНА
а) 6 б) 4 в) 3 г)5
4. УРАВНЕНИЕ РЕАКЦИИ СОЕДИНЕНИЯ
а) 2NаOН + СuSO4 = Nа2SO4 + Сu(OН)2
б) СuSO4 + Fе = FеSO4 + Сu
в) 2Н2 + O2 = 2Н2O
г) Fе2O3 + 3Н2 = 2Fе + 3Н2O
5. ХИМИЧЕСКАЯ РЕАКЦИЯ, УРАВНЕНИЕ КОТОРОЙ
NаОН + СuSO4 - Nа2SO4 + Сu(OН)2, ОТНОСИТСЯ К РЕАКЦИЯМ
а) разложения б) соединения в) замещения г) обмена
6. РЕАКЦИИ, ПРИ КОТОРЫХ ИЗ НЕСКОЛЬКИХ ПРОСТЫХ ИЛИ СЛОЖНЫХ ВЕЩЕСТВ ОБРАЗУЕТСЯ ОДНО СЛОЖНОЕ ВЕЩЕСТВО, НАЗЫВАЮТСЯ РЕАКЦИЯМИ
а) разложения б) замещения в) соединения г) обмена
7. СХЕМЕ ОКСИД ЖЕЛЕЗА(III) + ВОДОРОД - ЖЕЛЕЗО + ВОДА СООТВЕТСТВУЕТ УРАВНЕНИЕ ХИМИЧЕСКОЙ РЕАКЦИИ
а) FеО + Н2 = Fе + Н2O
б) Fе3O2 + 2Н2 = ЗFe + 2Н2O
в) 2FеО + Н2 = 2Fе + Н2O
г) Fе2O3 + 3Н2 = 2Fе + 3Н2O
8. ПРИ ВЗАИМОДЕЙСТВИИ 1 моль СЕРНОЙ КИСЛОТЫ С ЦИНКОМ ПОЛУЧИТСЯ ВОДОРОД ОБЪЕМОМ
а) 1л б) 2л в) 44,8л г) 22,4л
9. РЕАКЦИЯ, ПО КОТОРОЙ В ЛАБОРАТОРИИ ПОЛУЧАЮТ ВОДОРОД, ОТНОСИТСЯ К РЕАКЦИЯМ
а) разложения в) соединения б) замещения г) обмена
10. КУСОЧКИ МРАМОРА ЗАЛИЛИ СОЛЯНОЙ КИСЛОТОЙ. ЕСЛИ ВНЕСТИ ГОРЯЩУЮ ЛУЧИНКУ В ЭТОТ СТАКАН, ТО ПЛАМЯ
а) вспыхнет ярче б) не изменится в) изменит цвет г) погаснет
Аттестационный лист
1. Конкурс «Классификация веществ» ___________ баллов
(у доски)
1а. Конкурс «Установите соответствия» __________баллов
За скорость выполнения задания _________
За проверку выполненного задания (у доски) _____________
2. Химическая формула ____________ баллов
За скорость выполнения задания _________
2а. Конкурс «Математическая экспертиза» ______________
(у доски)
3. Конкурс «Допиши предложения» _____________ баллов
(у доски)
3а. Конкурс «Выбери правильный ответ» _________ баллов
За скорость выполнения задания _________
4. Практическое задание «Физические и химические явления» _________________ баллов
5. Конкурс «Тест по технике безопасности»________ баллов
(у доски)
5а. Правила использования оборудования и реактивов _____
6. Конкурс «Химическая экспертиза» __________ баллов
7. Кроссворд (у доски) ___________ баллов
7а. Конкурс Химические процессы вокруг нас» ____ баллов
8. Задача