- Учителю
- Урок химии в 8 классе
Урок химии в 8 классе


 Ахметханова Гульнар Мадиевна
Ахметханова Гульнар Мадиевна
учитель химии КГУ СШ №6 С ДМЦ,
стаж работы 27 лет, в том числе в данной организации 17 лет
высшая категория
Родилась ст. Лепсы 29 сентября 1961 года, в 1 класс поступила 1968 году и окончила СШ №54, и поступила КАЗ ГУ им. Кирова на химический факультет,1984 году окончила по специальности химик, учитель химии. С 1984 - 1987 годах работала там же в кафедре аналитической химии под руководством Кенжебековой Д. над научной темой « Поверхностно активные вещества» 1987 году по семейному обстоятельству переехала ст.Лепсы и работала в СШ № 54 учителем начальных классов до 1998 года,1998 году по семейному обстоятельству переехала в город Текели и устроилась в СШ №6 учителем химии . За эти годы готовила детей предметную олимпиаду, научно практические конференции, семинары. Ежегодно дети занимают призовые места в городе ,в области, поступают по гранту В ВУЗы. Одним из них являются Сарайкина А., Цыплина Т., Бузенус Н.,Гизатулина З., Им С.,Погромские Алла и Анеля, Есимов Е., Бек Д.,Есенгелды А.,Кокошкина О.,Гизатулина З.,, Искаков Д. Гизатулин Д.Мартыненко А., Бражникова А., Решетняк И.,Майер Е., Дель М., Зюбина Д.
Я, благодарна судьбе, что выбрала профессию УЧИТЕЛЯ !
Тема урока: Основные сведения о строении атомов.
Цель урока :
Сформировать знания учащихся о составе атома, и атомного ядра (протон, нейтрон, и массовое число) ;показать взаимосвязь понятии: протон и нейтрон, массовое число.
Подчеркнуть физический смысл атомного номера элемента в Периодической системе.
Дать современное определение понятий «атом», «химический элемент».
Ход урока
I. Организационный момент.
II. Повторение изученного материала. Самостоятельная работа (15 мин)
1 вариант
-
В предложение вставит слово « атом» и «молекула»
а) … водорода образована … водорода
б)… углекислого газа образована … углерода и … кислорода
-
Записать знаки следующих химических элементов и их произношение: натрия, железо, кальция, марганца, углерода, хлора.
-
Запишите формулы вещества и вычислите его относительную молекулярную массу, если известно, что в состав его молекулы входят:
а) 2 атома водорода
б) 2 атома фосфора и 5 атома кислорода
Указать какое из этих веществ является простым, а какое сложным
2 вариант
-
В предложение вставит слово « атом» и «молекула»
а) … кислорода образована … кислорода
б)… сернистого газа образована … серы и … кислорода Записать знаки следующих химических элементов и их произношение: алюминия, калия, кремния, серы, цинка, серебра.
-
Запишите формулы вещества и вычислите его относительную молекулярную массу, если известно, что в состав его молекулы входят:
а) 2 атома азота
б) 2 атома натрия и 1 атома кислорода
Указать какое из этих веществ является простым, а какое сложным
III. Изучение нового материала. Доказательство сложности строения атома
Прежде чем приступить к изложению нового материала, связанных со строением атома необходимо рассмотреть важнейшие этапы истории развития представлений о строении вещества: возникновении идей атомного строения, атомная теория Дальтона (19 веке).
Таким образом, делаете вывод, что в начале 20 века в связи с открытием электронов и явления радиоактивности разрушились прежние представления о неделимости атомов, а также о том, что атомы являются самыми маленькими частицами вещества.
Атом - это сложная система, в состав которой входят электроны и другие частицы.
А Т О М
Я Д Р О ЭЛЕКТРОННАЯ ОБОЛОЧКА
Протоны (р+) нейтроны (nо) состоит из электронов е-
Практически вся масса атома (99,95%) сосредоточена в очень малом объёме, находящемся в его центре - в ядре. Диаметр ядра, если считать его шарообразным составляет приблизительно 1/100 000 часть от диаметра атома. Если увеличить ядро атома железа до размера макового зерна, то диаметр атома железа составил бы более 30 метров. Из-за малого объёма плотность ядра атома неимоверно велика 230 млн т/см3 (миллион тепловозов в одном напёрстке).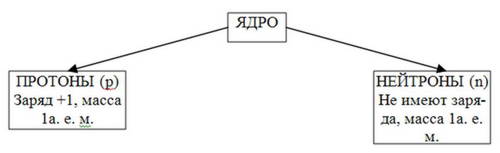
Ядра атомов заряжены положительно, число протонов равно заряду ядра. Вокруг ядра электроны ē, заряжены отрицательно (-1), масса в 2000 рез меньше массы протона. Атом состоит из очень маленького, но тяжёлого положительно заряженного ядра, состоящего из протонов и нейтронов, около которого движутся электроны.
Протоны - это частицы с положительным зарядом +1 (в условных единицах) и относительной массой 1.
Нейтроны - это электронейтральные (незаряженные) частицы с относительной массой 1.
Положительный заряд ядра равен числу протонов.
Атом - электронейтральная частица.
Электрон (ē) - это частица с отрицательным зарядом -1 (в условных единицах) и относительной массой равной 1/1837 массы протона. Вся масса атома сосредоточена в ядре.
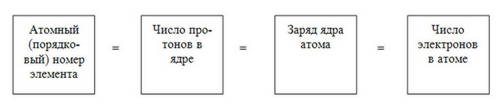
Число электронов в атоме равно числу протонов в ядре.
Планетарная теория строения атома Резерфорда.
Атом - это электронейтральная и химически неделимая частица, состоящая из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов.
Химический элемент - это вид атомов с одинаковым зарядом ядра.
IV. Закрепление. Определите число электронов, протонов, нейтронов для атомов - К, Са, S. Mn, Si, Al
элементы
К
Са
S
Mn
Si
Al
Число р+)
Число nо
Атомный(порядковый) номер элемента
V. Итог урока Домашнее задание: §53 , задания 4-5.