- Учителю
- Конспект урока химии в 8 классе по теме: 'Обобщение и систематизация знаний о классах неорганических соединений'
Конспект урока химии в 8 классе по теме: 'Обобщение и систематизация знаний о классах неорганических соединений'
Урок химии в 8 классе по теме:
«Обобщение и систематизация знаний учащихся об основных классах неорганических соединений.
Цель урока:
Обучающие: систематизировать знания учащихся по разделу «Основные классы неорганических соединений», повторить, обобщить, корректировать знания учащихся о составе, классификации, свойствах важнейших классов неорганических соединений, закрепить экспериментальные умения, знания о взаимопревращениях, т.е. генетической связи между классами неорганических соединений.
Развивающие: развивать умение учащихся сравнивать, анализировать, обобщать, делать выводы, развивать логическое мышление.
Воспитательные: развивать познавательный интерес к предмету с помощью химических игр.
Организационные формы работы: фронтальная , индивидуальная, групповая.
Методы и методические приёмы: беседа, эксперимент, игра.
Оборудование: таблица «Генетические связи неорганических веществ»,
Реактивы: 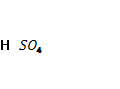
![]()
![]() кислоты: соляная, серная азотная
кислоты: соляная, серная азотная![]() , индикаторы: фенолфталеин, лакмус, метилоранж, оксиды натрия, кальция, меди, щёлочи.
, индикаторы: фенолфталеин, лакмус, метилоранж, оксиды натрия, кальция, меди, щёлочи.
План урока:
-
Актуализация прежних знаний
Мы завершили с вами изучение основных классов неорганических соединений. Какие соединения нами были изучены? Сегодня мы с вами обобщим все классы изученных соединений при помощи химических игр и эксперимента.
-
На столе реактивы всех изученных классов неорганических соединений. Вам необходимо классифицировать их по классам.
Ученик классифицирует, и коротко, и ясно даёт объяснение классификации.
-
Учащиеся на местах выполняют задания:
Осуществить превращения:
а). Углерод кислотный оксид кислота
![]()
![]()
![]()
![]()
соль
![]()
![]()
![]()
![]()
Кальций основной оксид основание
-
Работа в группах. На столах карточки с заданиями. Задания дифференцированы по уровню сложности:
1-я группа Fe → FeO → FeCl2 → Fe(OH)2 → FeO → Fe.
2-я группа Cu → CuCl2 → Cu(OH)2 → CuO → CuSO4
-
Экспериментальные задания.
а) На столе 3 стакана: вода, гидроксид натрия, серная кислота![]()
![]() (есть бумага с надписью)
(есть бумага с надписью)
Как узнать в каком стакане что?
( универсальный лакмус, метилоранж)
Загадка:
Отгадайте, о каком индикаторе идёт речь?
а) От щёлочи я жёлт, как в лихорадке,
Краснею от кислот, как от стыда,
А в воду я бросаюсь без оглядки:
Ведь здесь не знает меня среда.
( метилоранж)
б) 2 стакана: гидроксид натрия, соляная кислота. Как узнать где что?
Попасть в кислоту для него неудача,
Но он перетерпит без вздоха и плача.
Зато в щелочах у того блондина,
Начнётся не жизнь, а сплошная малина.
(фенолфталеин)
Блиц - опрос:
-
Общее название солей азотной кислоты (Нитраты)
-
Название оксида водорода (Вода)
-
Формула серной кислоты (H2SO4)
-
Валентность натрия (Единица)
-
Состав соляной кислоты (Раствор HCl в воде)
-
Соли угольной кислоты (Карбонаты)
-
Рстворимое основание (Щёлочь)
-
Какой газ выделяется при дыхании? (CO2)
-
Соли серной кислоты (Сульфаты)
-
Химическая формула воды (H2O)
Вычисления:
-
Найти молярные массы веществ: оксида магния, азотной кислоты, гидроксида натрия.
-
Определите массовую долю каждого элемента в оксиде серы (VI).
-
Определите массу воды, полученной при взаимодействии 1 моль кислорода с 2 моль водорода.
Домашнее задание: пов. § 18-21