- Учителю
- Урок 'Азот' 9 класс.
Урок 'Азот' 9 класс.
Урок по теме: «Азот». 9 класс.
Урок вводный по теме: «Подгруппа азота».
Цель: создать условия для изучения строения и свойств азота, опираясь на алгоритмы освоения материала о химических элементах.
Обучающие задачи: конкретизировать знания учащихся о строении атома и ковалентной неполярной связи на примере строения атома и молекулы азота; рассмотреть физические и химические свойства азота в свете ОВР; показать значение азота как биогенного элемента, познакомить учащихся с нахождением его в природе.
Развивающие задачи: продолжить развитие умений прогнозировать свойства элементов на основании положения их в ПСХЭ и строении атомов, аргументировать свою точку зрения, умений работать с дополнительными источниками информации.
Воспитательные задачи: продолжить работу по накоплению фактического материала для углубленного усвоения понятий, последующих обобщений мировоззренческого характера, представить доказательства неизбежности использования открытий новых химических элементов на любом этапе развития науки и техники.
Оборудование: компьютер, мультимедийный проектор, электронное пособие «Общая и неорганическая химия» МарГУ. Асбестовая сетка, бихромат аммония.
Ход урока.
-
Введение. Актуализация знаний. Организация беседы (3 минуты).
Продолжая путешествие по ПСХЭ, делаем остановку на 5 группе. Темой нашего урока является Азот, чтобы понять особенности строения и свойств азота, рассмотрим общую характеристику элементов 5 группы главной подгруппы.

Перечислите элементы 5 группы главной подгруппы.
Подробно мы изучаем только 2 элемента этой группы: азот и фосфор, сравним их по строению атомов (работа с таблицей в рабочей тетради). Какой можно сделать вывод о строении этих атомов и на основании строения об их свойствах? Азот и фосфор принадлежат к одному семейству, у них сходное строение, а, следовательно, и свойства. Проверить эти выводы мы сможем в конце изучения темы, когда будут рассмотрены свойства фосфора. А сейчас вашему вниманию представлен азот.
2.Активизация знаний по теме. Сообщение цели урока. Историческая справка, постановка проблемного вопроса (5 минут).
1772г. шотландец Даниел Резерфорд увлекся опытами с воздухом и обнаружил, что после удаления кислорода остается «удушливый воздух», в котором гаснет огонь свечи. Почти одновременно с ним азот открыли шведский ученый Карл Шееле и английский химик Джозеф Пристли. Современное название элементу дал французский химик Антуан Лоран Лавуазье.
«А-зоос» с греческого «безжизненный». Лавуазье не мог не знать, что алхимики пользовались словом «азот» для обозначения «жизненной силы», исцеляющей больных и делающих уродливых красивыми. А согласно Библии «азот» - это начало и конец всего сущего, суть жизни, первое и последнее деяние. Выходит, азот - одновременно и безжизненный, и исцеляющий, жизнь утверждающий и жизнь отрицающий. Какой он на самом деле? Чтобы ответить на этот вопрос нам понадобятся некоторые знания об азоте. Какие именно?
3. Планирование работы по изучению строения и свойств азота. Беседа (5 минут).
План изучения азота (составляем вместе с учениками).
-
Строение атома. Окислительно-восстановительная активность.
-
Строение молекулы азота.
-
Физические свойства.
-
Химические свойства.
-
Получение азота.
-
Применение азота.
-
Нахождение в природе.
-
Круговорот азота в природе.
4. Формирование знаний о строение и свойствах азота. Беседа с опорой на содержание электронного пособия (17 минут).
Упражнение 3 в рабочей тетради.
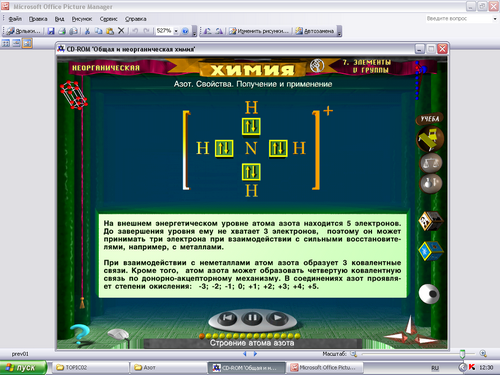
Обратим внимание на строение электронной оболочки атома азота. На основании этого предположим строение молекулы азота. Упражнение 4 в рабочей тетради.
От строения кристаллической решетки зависят физические свойства веществ. Какие свойства характеризуют вещества с молекулярной кристаллической решеткой? На основании строения молекулы азота предположим химическую активность этого элемента. С какими веществами будет вступать в реакции азот и при каких условиях?
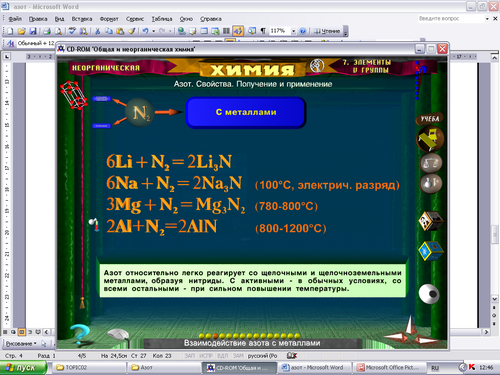
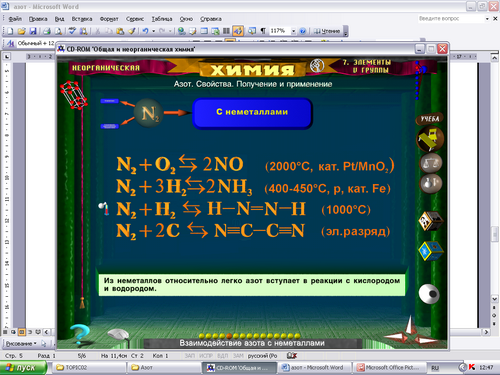
Схемы баланса.
Сравнить реакции по разным факторам. Предложить способы смещения химического равновесия.
Существуют промышленные и лабораторные способы получения азота.
«И ударил по своей наковальне гигантским молотом черный от копоти и пыли бог Гефест, и проснулись вулканы на Земле». Домашний вулкан предложил Беттегр в 1843г. Демонстрация опыта.
От строения зависят свойства, от свойств - применение.
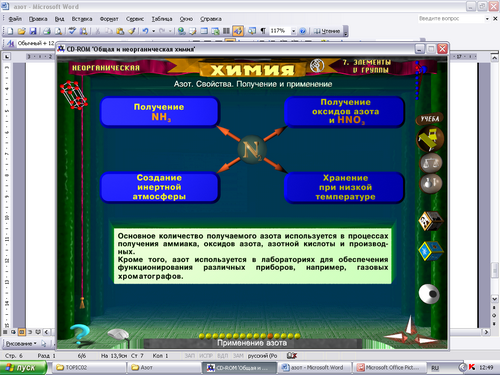
Зная свойства азота можно предположить формы его нахождения в природе.
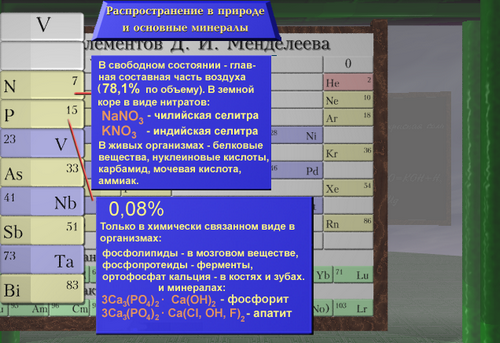
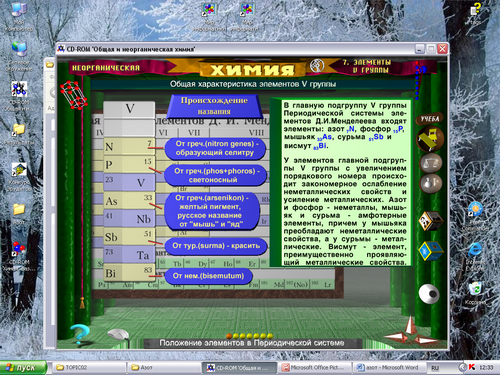
Азот как безжизненный элемент находится в свободном виде, входит в состав минералов (селитр), его латинское название нитрогениум в переводе означает рождающий селитру, но в русском и во французском языках сохранилось название «азот». В «Диалектике природы» Фридрих Энгельс писал: «Жизнь - есть способ существования белковых тел». Азот- это биогенный элемент, он активно включен в круговорот живой и неживой природы, так как азот входит в состав белков живых организмов (16%).
5. Закрепление материала. Составление уравнений. (6 минут).
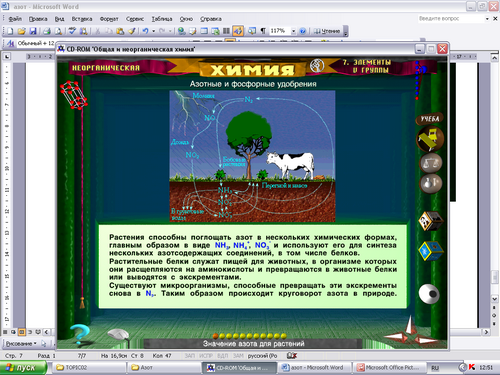
На основании схемы круговорота азота в природе, составьте уравнения реакций, подтверждающие данную схему.
Азот жизненный? Но нитраты негативно влияют на здоровье человека. В ВлГУ работает НОУ старшеклассников по проблемам экологии, исследования по влиянию нитратов и нитритов на живые организмы провел Аргам Акопян (сообщение о результатах исследований).
6. Выводы, подведение итогов урока. Беседа (2 минуты)
Таким образом: азот - инертен, химически стоек, но жизненно важный элемент, поступающий в наш организм с белковой пищей, но и в виде нитратов и нитритов, вредных для организма. В этом проявляется один из законов диалектики, законов развития природы: единство и борьбы противоположностей.
7. Домашнее задание (2 минуты).
На дом: п. 23, упр. 2,4,5. В организме человека 10% азота по массе. Рассчитайте, какая масса азота приходится на ваш организм?
Доп. Определить каких атомов больше азота или меди и во сколько раз, если известно, что их массовые доли в земной коре равны.