- Учителю
- Урок по химии на тему Предельные одноатомные спирты (10 класс)
Урок по химии на тему Предельные одноатомные спирты (10 класс)
Учитель химии: Быкова О.С.
Урок по теме «Предельные одноатомные спирты»
Тип урока: изучение нового материала.
Вид урока: комбинированный урок
Цель урока: на основе анализа строения молекул спиртов и известной вам информации об их применении,спрогнозировать свойства спиртов и подтвердить прогноз экспериментально.
Задачи:
-изучить состав, физические свойства, номенклатуру и изомерию спиртов; выявить причины токсичности метилового и этилового спирта, обеспечить в ходе урока повторение основных терминов и понятий по теме;
-создавать условия для развития логического мышления учащихся, умение анализировать, сравнивать, обоснованно высказывать свою точку зрения, делать выводы;
-формировать навыки работы с различными информационными источниками.
Ход урока
I. Организационный момент.
II. Мотивация и целеполагание.
Мы уже встречались с этим классом соединений на уроках биологии при изучении темы «гликолиз». Спирты имеют огромное народнохозяйственное значение. Именно поэтому мы их и изучаем.
III. Актуализация знаний.
Мы изучили большую группу органических соединений, состоящих только из двух химических элементов - углерода и водорода. Вы уже знаете, что в состав органических веществ могут входить и другие химические элементы, например, кислород. Вещества, содержащие в своем составе помимо углерода и водорода еще и кислород, называются кислородсодержащими органическими соединениями. В состав этих соединений входят кислородсодержащие функциональные группы. Вспомним некоторые из них.
ОН -
-
Как называется эта функциональная группа? (гидроксильная).
-
Вещества какого класса веществ имеют такую группу? (спирты, фенолы)
:С = О
-
Как называется эта функциональная группа? (карбонильная).
-
Вещества какого класса имеют такую группу? (альдегиды, кетоны)
- СООН
-
Как называется эта функциональная группа? (карбоксильная).
-
Вещества какого класса веществ имеют такую группу? (карбоновые кислоты)
-
Что, по вашему мнению «спирты»?
-
Какие названия спиртов вам известны?
-
Пользу или вред наносят людям представители ряда спиртов?
-
Какие области применения спиртов вы можете назвать?
IV. Изучение нового материала.
На сегодняшнем уроке мы познакомимся с классом кислородсодержащих веществ предельными одноатомными спиртами, с их гомологическим рядом, строением, особенностью функциональной группы и природой связи в ней, расширим представления о взаимном влиянии атомов на примере одноатомных спиртов.
Спирты большой по разнообразию и свойствам класс
органических соединений которые широко применяются в различных
областях народного хозяйства.
Это фармацевтика, производство косметики, пищевая промышленность, а
также как расстворитель, при производстве пластмасс, лаков, красок
и др. Рассмотрим таблицу.
Таблица 1.
НЕКОТОРЫЕ ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ КЛАССА СПИРТОВ
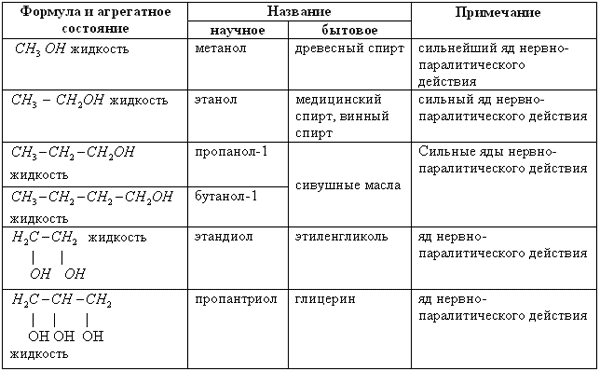
Если говорить о действии на организм человека, то все спирты -
яды. Молекулы спирта пагубно действуют на живые
клетки..
В самом простом случае строение спирта можно выразить следующей
формулой:
R - OH, где R - углеводородный радикал.
Спирты можно классифицировать по трем признакам:
1. Числу гидроксильных групп (одноатомные, двухатомные, многоатомные).
Таблица 2.
КЛАССИФИКАЦИЯ СПИРТОВ ПО ЧИСЛУ ГИДРОКСИЛЬНЫХ ГРУПП (-ОН)
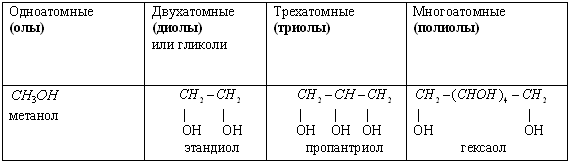
Таблица 3.
КЛАССИФИКАЦИЯ СПИРТОВ ПО ХАРАКТЕРУ УГЛЕВОДОРОДНОГО РАДИКАЛА
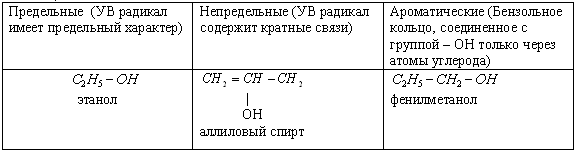
Таблица 4.
КЛАССИФИКАЦИЯ СПИРТОВ ПО ХАРАКТЕРУ АТОМА УГЛЕРОДА СВЯЗАННОГО С ФУНКЦИОНАЛЬНОЙ ГРУППОЙ -ОН
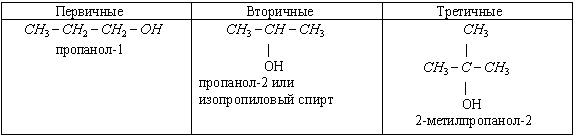
Четвертичных спиртов не существует, т.к. четвертичный атом С связан с 4 другими атомами С, поэтому на связь с гидроксильной группой нет больше валентностей.
Мы с вами в школьном курсе будем подробно изучать одноатомные предельные спирты с общей формулой: CnH2n+1OH
Рассмотрим модели молекул отдельных представителей этих спиртов (метилового, этилового)
Гомологический ряд этих спиртов начинается с метилового спирта:
CH3 - OH -метиловый спирт
CH3 - CH2 - OH
-этиловый спирт
CH3 - CH2 -
CH2 - OH -пропиловый спирт
CH3 - CH2 -
CH2 - CH2 - OH
-бутиловый спирт
CH3 - CH2 -
CH2 - CH2 -
CH2 - OH -амиловый
спирт или пентанол
Изомерия
Для предельных одноатомных спиртов характерны следующие виды изомерии:
1) положения функциональных групп:
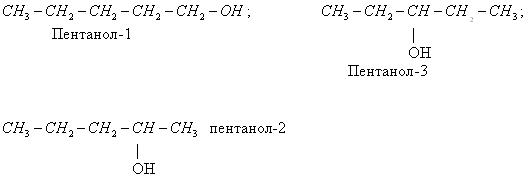
2) углеродного скелета.
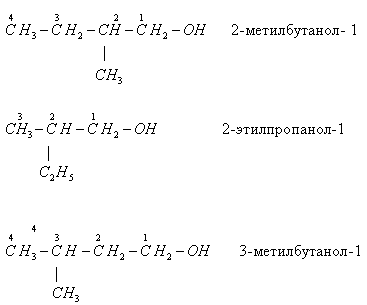
Заметьте - нумерация атомов углерода начинается с конца, близкого к группе -ОН.
3) межклассовая изомерия (с простыми эфирами R - O - R)
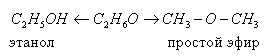
Физические свойства спиртов.
Сейчас мы рассмотрим свойства, проведём лабораторную работу.
Виртуальный опыт. «Растворимость спиртов».
Ребята делают вывод о растворимости спиртов.
- А какие ещё физические свойства характерны для спиртов?
В гомологическом ряду предельных одноатомных спиртов нет газообразных веществ. Это связано с тем, что молекулы спиртов в значительной степени ассоциированы, т. е. связаны друг с другом водородными связями. Этим объясняются более высокие по сравнению с соответствующими алканами температуры кипения и плавления спиртов. Спирты до С12 являются жидкостями, высшие спирты - твёрдыми веществами.
Жидкие спирты бесцветны, обладают характерным запахом. Метанол и этанол смешиваются с водой в любых соотношениях. С увеличением относительной молекулярной массы растворимость спиртов уменьшается. Твёрдые спирты в воде практически не растворимы и лишены запаха. Метанол очень ядовит. Небольшое его количество вызывает слепоту и смерть.
Виртуальный опыт . Горение спиртов.
Учащиеся пишут уравнение горения этилового спирта с объяснением учителя и затем самостоятельно пишут уравнение реакции горения пропанола самостоятельно.
Виртуальный опыт . Окисление спиртов оксидом меди (II).
Ребятам объясняется механизм этой реакции и они пишут уравнение окисления этилового спирта оксидом меди (II).
Виртуальный опыт. Окисление спиртов перманганатом калия KMnO4.
Ребятам объясняется механизм этой реакции и они пишут уравнение окисления этилового спирта перманганатом калия.
Виртуальный опыт. Взаимодействие спиртов с металлическим натрием (кислотные свойства).
Ребятам объясняется механизм этой реакции и они пишут уравнение этой реакции.
Виртуальный опыт . Взаимодействие спиртов с галогеноводородами (основные свойства).
Ребятам объясняется механизм этой реакции и они пишут уравнение реакции взаимодействия этилового спирта с бромоводородом.
- Итак, спирты проявляют и кислотные, и основные свойства.
Виртуальный опыт . Дегидратация спиртов с образованием непредельных углеводородов (алкенов).
Ребятам объясняется механизм этой реакции, её условия протекания и они пишут уравнение этой реакции.
Виртуальный опыт. Дегидратация спиртов с образованием простых эфиров.
Ребятам объясняется механизм этой реакции, её условия протекания и они пишут уравнение этой реакции.
Влияние алкоголя на организм.
Спирты или алкоголи находят широкое применение в промышленности и народном хозяйстве в качестве топлива, растворителя, сырья для химической промышленности и т. д. Этанол используется для приготовления спиртных напитков, несмотря на то , что оказывает отрицательное воздействие на организм. Посмотрим несколько сюжетов о влиянии этанола на некоторые системы органов.
Употребление алкоголя особенно опасно тем, что вызывает привыкание, т.е. обладает наркотическим действием, и чем моложе организм, тем быстрее может возникнуть привыкание. Об этом свидетельствует известный исторический пример. В клинике нашего знаменитого врача-физиолога Ивана Петровича Павлова наблюдалась девочка грудного возраста, которая поступила в клинику с признаками алкоголизма, развившегося у нее после однократного приема алкоголя, который дала мама, чтобы ребенок лучше спал. С тех пор девочка стала еще более беспокойной, постоянно плакала, не могла уснуть, пока не получала очередную порцию
V. Закрепление новых знаний.
-
Что такое спирты?
-
Какое можно дать определение спиртам, одноатомным спиртам?
-
Определить строение С3Н7ОН, если известно, что это - одноатомный спирт.
-
Как распознать, находящийся в пробирке одноатомный спирт?
VI. Подведение итогов урока. На сегодняшнем уроке мы с вами рассмотрели новый класс кислородосодержащих соединений - одноатомные спирты. Познакомились с их строением, свойствами, применением, получением.
VII. Домашнее задание по учебнику О.С. Габриелян § 9 №5-10
VIII. Рефлексия.
-
Что заинтересовало вас сегодня на уроке более всего?
-
Как вы усвоили пройденный материал?
-
Какие были трудности? удалось ли их преодолеть?
-
Помог ли сегодняшний урок лучше разобраться в вопросах темы?
-
Пригодится ли вам знания, полученные сегодня на уроке?