- Учителю
- Зат мөлшері. Молярлық масса.
Зат мөлшері. Молярлық масса.
29.09.16
8-класс Химия
Сабақтың тақырыбы: Зат мөлшері. Молярлық масса.
Сабақтың мақсаты: Білімділік: Зат мөлшерінің өлшем бірлігі - моль туралы, Авогадро саны жөнінде ұғым қалыптастыру. Заттың берілген өлшемі бойынша құрылымдық бөлшектердің санын анықтауға үйрену. Дамытушылық: Молярлық масса ұғымын, заттың молярлық массасын есептеп шығару білігін қалыптастыру. Масса, зат мөлшерінің өлшем бірлігі, молярлық масса деген ұғымдарды өзара байланыстыра отырып, есеп шығаруға үйрету. Молярлық және салыстырмалы молекулалық массалар сандық мәні бойынша тең болатындығын түсіндіру.Тәрбиелік: Өз еркімен жұмыс жасауға, ойын жеткізе білуге тәрбиелеу.
Сабақтың түрі: аралас сабақ.
Пән/қ байланыс: физика, биология.
Құрал жабдықтар: зат мөлшері бір моль болатын металлдармен бейметаллдар үлгілері (күкірттің, темір ұнтағының, мырыштың, )
Тірек біліммен біліктер: Зат мөлшері, заттың салыстырмалы молекулалық массасы, зат мөлшерінің өлшем бірлігі, заттың салыстырмалы молекулалық массасын есептеу.
Жаңа материалды оқыту. Мұғалім өткен сабақтан байланыстыру мақсатымен оқушыларға бірнеше сұрақ қояды:
1. Заттың құрам тұрақтылығы дегеніміз не?
2. Темір сульфидінде темір мен күкірттің тұрақты масса қатынасы қанда?
Оқушыларға ұнтақтар 4 г. күкіртте күкірттің қанша атомы болса, 7 г. темірде темірдің сонша атомы болатынын түсіндіреді. Демек, әрбір темір атомы күкірттің бір атомымен қосылысады деген тағы бір тұжырымды оқушы өз бетімен жасайды.
Бұрын алған білімін еске түсіріп, талдау нәтижесінде жасаған қорытындыларына сүйене отырып, мұғалім заттардың атомдары мен молекулаларының қажетті санын алу іс жүзіне мүмкін еместігін айтады. Сондықтан химияда «зат мөлшері» деген физикалық шама қолданылады.
Ал зат мөлшері сол заттың құрылымдық бөлшектерінің санымен анықталады, яғни атом, молекула немесе басқа бөлшектер саны. Зат мөлшерінің өлшем бірлігі - моль. Моль-берілген заттың құрылымдық бөлшектері 12г көміртегіндегі атом санына сәйкес келетін зат мөлшері. ν (ню) әрпімен белгіленеді, құрылымдық бөлшектер саны Na әрпімен белгіленеді.
Заттың керекті мөлшерін қалай өлшеп алуға болады?
Осы жерде молярлық массаны пайдаланатындығын айтып, оқушыларды сабақтың мақсатымен таныстыру. Зат мөлшерін моль арқылы өрнектеген сияқты молярлық масса зат массасын грам арқылы көрсетеді. Демек, мұғалім «Заттың молярлық массасы М зат массасының зат мөлшеріне қатынасына тең шама» деген анықтаманы айтып, оқушылардың дәптеріне жазғызады.
Молярлық масса г/мольмен, яғни граммен алынған мольмен өрнектеледі: М=m / ν Мысалы: 1) M(H2)= 2 г/моль; 2) M(O2) =32 г/моль; 3) M(H2O) =18 г/моль
Оқушылардың өздігінен шығаруына берілетін есептер:
-
Массасы 112г темір неше моль болады?
-
Массаса 132г көміртегі(IV) оксиді неше моль болады?
-
Массасы 272г мырыш хлориді неше моль болады?
-
Мөлшері 0,3 моль көміртегі(IV) оксидінің массасын есептеп шығарыңдар;
-
Мөлшері 0,2 моль мыс (ІІ) оксидінің массасын есептеп шығарыңдар;
-
Мөлшері 0,5 моль судың массасын есептеп шығарыңдар;
Оқушылардың шығарған есептерін тексеріп, қателерін түзеткеннен кейін, жаңа тақырып бойынша қорытынды жасалады.
Сабақ соңында төмендегі сұрақтар көмегімен оқушыларда жаңадан қалыптастырылған ұғымдарды бекітуге болады:
-
Заттың молярлық массасы дегеніміз не?
-
Заттың молярлық массасының өлшем бірлігі не?
-
Қай формуланың көмегімен заттың молярлық массасын, массасын, мөлшерін анықтауға болады? Зат мөлшерінің өлшем бірлігі не?
-
Зат мөлшері қалай белгіленеді?
-
a) ν (C) = 4 моль деген жазу нені білдіреді?
б) ν (H2O)=2 моль деген жазу нені білдіреді?
-
Үш молекула су қанша моль болады?
Үйге тапсырма. (5-6)
1.10.16
8-класс Химия
Сабақтың тақырыбы: Химиялық формулалар, химиялық элементтердің атомдарының валенттілігі.Зат құрамының тұрақтылық заңы
Сабақтың тақырыбы:
Заттың сандық және сапалық құрамын білдіретін химиялық формула жайлы білімді қалыптастыру
Заттың Мr,күрделі зат құрамындағы элементтің массалық үлесін табуды есептер шығара отырып үйрету және логикалық ойларын дамыту.
Өз еркімен жұмыс жасауға, ойын жеткізе білуге тәрбиелеу. Валенттілік туралы түсінік беру. Екі элементтен тұратын заттың берілген формуласы бойынша валенттіліктерін анықтауға үйрету. Валенттілік құра отырып ойларын тереңдетіп дамыту. Ұжымдық жұмысқа, таза жазуға тәрбиелеу.
Құрал − жабдықтар: Химиялық таңбалар және элементтердің салыстырмалы атомдық массасы берілген кесте. Сабақтың түрі: аралас сабақ. Әдіс-тәсілі: өзіндік жұмыс. Сабақтың түрі: аралас сабақ.
Әдіс-тәсілдері: есептер шығару.
Сабақ барысы: Ұйымдастыру кезеңі.
Сабақты үй жұмысын тексеруден бастау.
-
Төменде берілген заттарда элемент жайлы айтыла ма: а)оттек демалу үшін қажет; ә)оттек судың құрамына кіреді;
-
Оттек, натрий, күкірт, сутек, калий, көміртек элементтерінің таңбаларын жазып, оны оқып беріңдер.
-
Таблицаны толтыру:
-
Жаңа сабақ тақырыбы тақтаға жазылады: Оқушыларға белгілі
заттардың химиялық формуласын және сол арқылы салыстырмалы
молекулалық массасын, күрделі заттағы әр элементтің массалық
үлесін табуға есептер шығарып үйрету.
1. Заттың формуласы бойынша салыстырмалы молекулалық массасын есептеу.
Мr(H2O) = 2Ar(H) + 1Ar(O)= 2•1+16=18
2. Күрделі зат құрамындағы элементтердің массалық қатынастарын есептеу.
1-есеп: Алюминий гидроксидіндегі А1(ОН)3 алюминий, оттек және сутек атомдары массаларының қатынасын есептеңдер.Шешуі: Әр элементтің атом санын оның салыстырмалы атомдық массасына көбейтіп алюминий, от- тек, сутек массаларының қатынастарын тауып, сосын қысқартамыз:
m(А1) ׃ m(О) : m(Н) = Ar(А1) : 3Аг(O) : 3Ar(Н) = 27 : 48 : 3 = 9׃16:1 =15
Жауабы: Алюминий гидроксидінің қүрамындағы алюминий, оттек, сутек атомдары массаларының қатынасы: m(AI) : m (H) : m(O) = 9 : 16 : 1.
3. Күрделі зат құрамындағы элементтердің массалық үлестерін есептеу
2-есеп: Алюминий гидроксиді А1(ОН)3 құрамындағы элементтердің массалық үлестерін есептеңдер. Есепті екі тәсілмен шығаруға болады:
1) массалық үлестің дайын формуласын пайдалану;
2) пропорция арқылы.
2) Оттектің массалық үлесін у деп пропорция қүрамыз:
78 - 100 %,
3 •16 - у
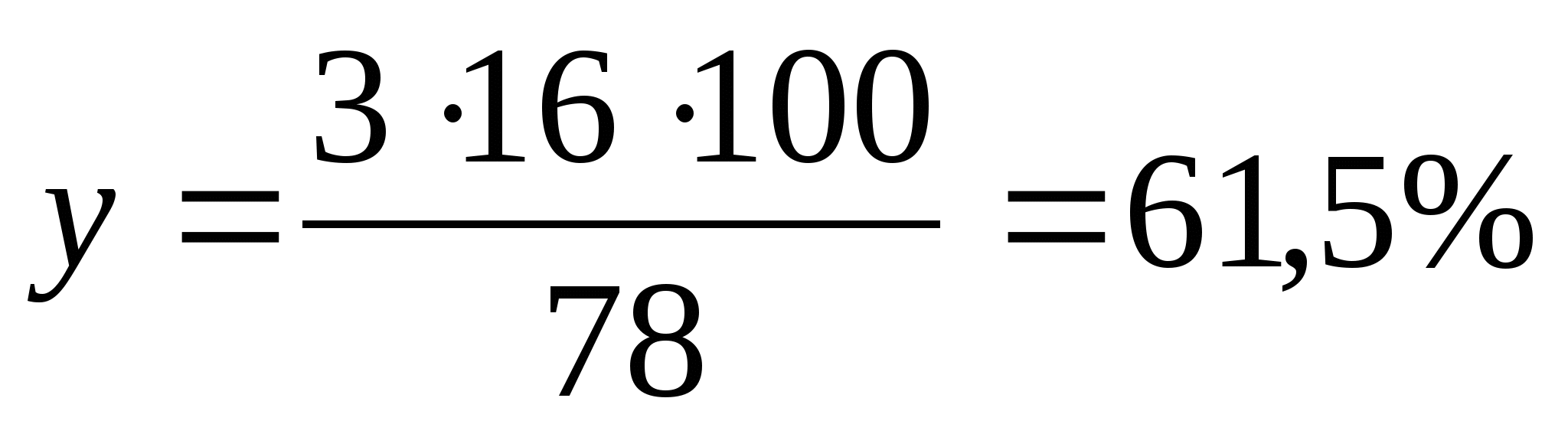
3) Сутектің массалық үлесін z десек: 78 - 100 %,
3 • 1- z
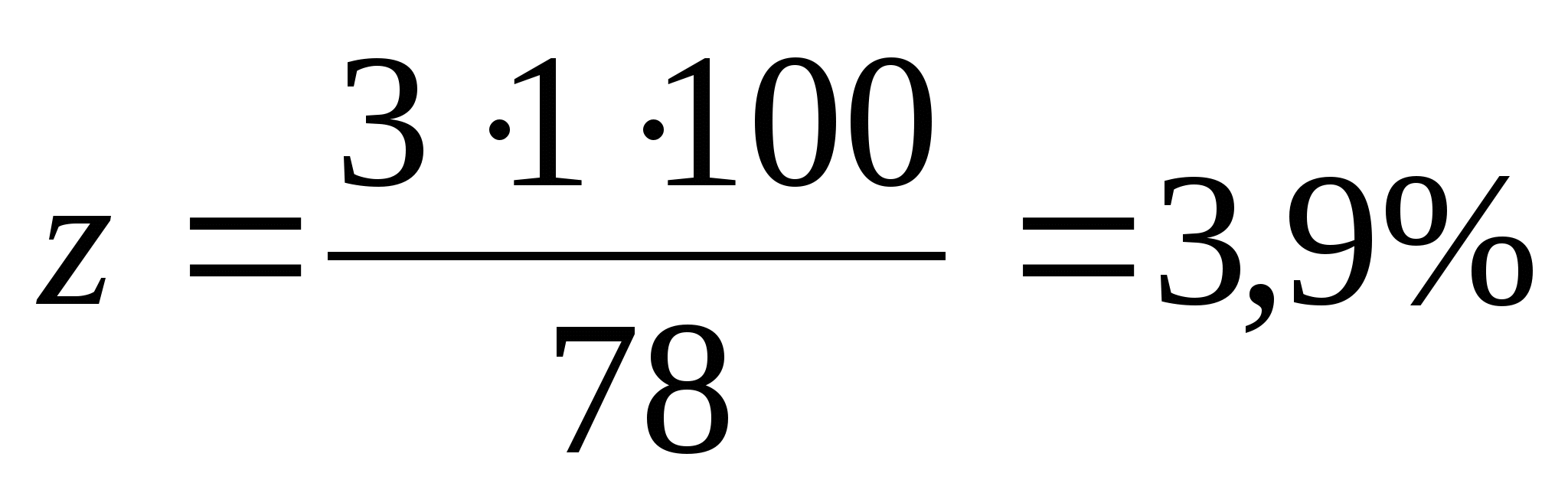
Жауабы. ω(АІ) = 34,6%, ω(0) = 61,5%, ω(Н) = 3,9%.
Жаңа материалды бекіту мақсатында жаттығулар мен есептер жинағы бойынша есептер беріліп шығарылады.
Тірек білім мен біліктер: Элементтердің химиялық таңбасын білу, салыстырмалы молекулалық массаны анықтау, индекс, коэффициент, ең кіші ортақ еселік.
Білім мен біліктерін тексеру: Оқушылардың салыстырмалы молекулалық массаны есептеу біліктерін химиялық формула туралы түсініктерін тексеру және бекіту мақсатында құрастырылған 10−15 минутқа есептелген өзіндік жұмыс ұсынылады.
1 - нұсқа.
1.Химиялық таңбалар арқылы өрнекте: оттегінің бес молекуласы; оттегінің екі жеке атомы; оттегінің бір молекуласы; екі молекула оттегі;
2.Na2CO3 химиялық формуласы нені көрсетеді?
2 - нұсқа.
1.Төмендегі белгілер нені көрсетеді: 5Н; Н2; 7Н2;
2.HNO3 химиялық формуласы нені көрсетеді?
3 - нұсқа
1.Химиялық таңбалар арқылы жазып өрнекте: күкірттің бес атомы; сутегінің бір ,молекуласы; судың үш молекуласы; сутегінің үш молекуласы;
2.Н3РО4 химиялық формуласы нені көрсетеді?
4 - нұсқа
1.Төмендегі химиялық формулалар нені көрсетеді? 3О2; 5О; О;
2.Күкірт қышқылының химиялық формуласы - Н2SO4. Осы формула бойынша ,,,,,,,,,,,,қышқылдың сандық және сапалық құрамын көрсет.
Жаңа материалды оқыту:
1. Оқушыларды бейметалдардың сутекті қосылыстарының мысалында атом валенттілік терінің жаңа қасиеттерімен таныстыру. HBr, H2S, PH3, SH4, CH4, H2O, NH3. Валенттілікке анықтама бергеннен кейін, жоғарыда көрсетілген заттардың формулалары жазылып, оқушыларды бромның, күкірттің, фосфордың, кремнийдің, көміртегінің, оттегінің және азоттың валенттіліктерін осы элементтер мен қосылған сутегі атомдарының жалпы саны бойынша анықтауға жаттықтыру жұмысы жүргізіледі.
2. Егер бір элементтің валенттілігі белгілі болса екінші элементтің валенттілігін табуға болатындығын Al2O3 мысалымен түсіндіреміз.
Оның алгоритмі ұсынылады. (мұғалім бұл алгоритмді кесте түрінде тақтаға іліп қоюына болады)
1. Қосылыстың формуласы жазылады: Al2 O3 ; ІІ
2. Қосылыстағы оттегі атомының валенттігі белгілі, оны рим санымен үстіне жазу: Al2O3 ;
3. Оттектің валенттігін оның индексіне көбейтіп, алюминийдің индексіне бөлу:
ІІ * 3 = 6; 6 : 2 = III; ІІІ ІІ
4. Қосылыстағы алюминийдің валенттігі үшке тең, оны рим санымен үстіне жазу: Al2O3;
Тұрақты және ауыспалы валенттілік туралы түсінік беріледі. Оқушыларға дәптеріне тұрақты валенттілік сақтайтын элементтерді жаздырамыз.
I - валентті Na, K, Ag, H; IІ - валентті Mg, Ca, Ba, Zn, O; III - валентті Al
Элементтердің ауыспалы валенттілік көрсететіндігін дәлелдейміз. FeCl2, FeCl3, SO2, SO3, PbO2, CO, CO2 қосылыстарын мысалға ала отырып, бұл заттардың аталуындағы ерекшелікті түсіндіреміз. Мысалы, көміртегі (II) оксиді, көміртегі (IV) оксиді.
Жаңа материалды бекіту: Формуласы бойынша химиялық элементтердің валентілі гін табуды үйрету мақсатында төмендегі жаттығулар орындатамыз. Төмендегі сутегі мен оттегінің үстіне рим цифры арқылы валенттілігі қойылған, қосылыстағы қалған элементтердің валенттілігін рим цифрымен жазып көрсетіңдер.
І нұсқа: H2, MgO, Al2O3, HCl, P2O5,
ІІ нұсқа: SiH4, Na2O, BaO, Ag2O, H2O,
ІІІ нұсқа: N2O5, NH3, MnO2, ZnO, N2O,
Егер бұл жұмысты оқушылар сабақта үлгере алмаса, үйде аяқтау тапсырылады.
Үйге тапсырма беру:§ 10. 1-63,1-64,1-65,1-77,1-111,1-112, 1-110. Есептер жинағы
Бағалау.
6.11.16
8-класс Химия
Сабақтардың тақырыбы: Физикалық және химиялық құбылыстар; Химиялық реакциялар. №1 көрсетілім(1.3) №1 зертханалық тәжірибе(1.2,1.3)
Сабақтың мақсаты:
Білімділік; Химиялық құбылыстың физикалық құбылыстан айырмашылығын түсіндіру, химиялық реакцияның алуан түрлілігімен таныстыру, химиялық реакцияның басталуы мен жүру барысының жағдайын және химиялық реакцияның негізгі белгілерін бақылауға үйрету.
Дамытушылық: құбылыстардың айырмашылығы мен ұқсастығын айыра отырып ойларын дамыту.
Тәрбиелік: өз еркімен жұмыс жасауға, ой ын жеткізе білуге тәрбиелеу.
Сабақтың түрі: аралас сабақ.
Сабақтың әдіс-тәсілдері: жеке тапсырма беру, іздендіру.
Пәнаралық байланыс: физика, биология.
Құрал - жабдықтар: Мыс пластинкасы, магний лентасы, мәрмәрдің немесе бордың түйірлері, тұз қышқылының ерітіндісі, қант түйірлері, мыс сульфатының ерітіндісі, парафин, сынауықтар, шыны түтіктер, қысқыш, спиртшам, тигель, электрондық оқулық.
Тірек білім мен біліктер: Физикалық құбылыс, зертханалық құралдармен жұмыс істей білу.
Сабақтың барысы: Оқушылардың білім мен біліктерін тексеру үшін таза заттар мен қоспаларды ажырата білуге арналған төмендегі тапсырмаларды беруге болады.
1. Келтірілген тізімнен заттар мен қоспаларды жеке бөліп жазыңдар:ауа,темір,ас тұзы,сүт.
2. Өзің білетін қоспаларды бөлудің әдістерін қолданып, судан мына заттарды қалай бөлуге болатындығын көрсет: а/қант: ә/ бор: б/ бензин: в/ ас тұзы. Қандай қасиеттеріне сүйеніп, бұл заттарды судан бөлдің?
3. Төмендегі келтірілген әдістермен қандай қоспаларды бөлуге болатындығына мысал келтір : а/ сүзу: ә/ суалту: б/ тұндыру.
Жаңа материалды оқыту:Оқушылардың физика курсынан алған біліміне сүйене отырып, физикалық құбылыс кезінде заттың пішіні мен агрегаттық күйінің өзгеретінін еске түсіре келіп, химиялық құбылыс туралы түсінік беру. Осыған орай химиялық құбылыс заттар қасиетінің өте күрделі өзгерістері екендігін оқушыларға таныстыру. Сабақты табиғаттағы заттардың түрлі өзгерістерін еске түсіре отырып, әңгімелеуден бастаймыз. Оқушыларға мынадай сұрақтар береміз:
1. Табиғатта жүретін қандай өзгерістерді білесің?
2. Табиғаттағы өзің бақылаған заттар өзгерісіне мысал келтір.
3. Заттардағы байқалатын өзгерістердің барлығы бірдей ме?
Физикалық және химиялық құбылыстарды өзара салыстыру арқылы жақсы нәтижеге жетуге болады. Бұл үшін оқушылар шыны түтікті ию, қантты ұнтақтау, еріту және жағу, парафинді балқыту тәжірибелерін жасайды. Тәжірибе нәтижесінде оқушылар заттың қасиетін өзгермегенін, жаңа зат түзілмегенін көріп қорытындылайды. Ал қанатты жағу кезінде оқушылар назарын жаңа зат - көмір мен су түзілгеніне аударамыз. Осыдан кейін магнийді, парафинді жағу, мыс пластикасын күйдіру тәжірибесі жүргізіледі. Оқушылар жаңа заттардың түзілуіне назар аударады. Сонымен құбылыстар екіге бөлінеді - физикалық және химиялық деген қорытынды жасалады. Оқушыларды оқулықпен жұмыс істеуге және оқулықтан анықтаманы таба білуді дағдыландыру үшін оқулықтан физикалық және химиялық құбылыстардың анықтамасын табуды тапсыру керек. Химиялық құбылыстың химиялық реакция деп аталатындығын, химиялық реакциялардын өз белгілері бола- тындығы айтылып, әр түрлі белгілері бар реакциялар жасап көрсетіледі: ерітінділерде тұнба түзілу
( мысалы, BaSO4 ,AgCl,т.б) газ бөліну(H2, O2, NH3, CO2, т.б.), батареяда тоқтың пайда болуы, соның әсерінен электр шамының жануы химиялық құбылыс екендігі түсіндіріледі. Оқушылардың назарын ең басты қорытындыға аудару керек: химиялық реакцияның ең негізгі белгісі жаңа заттардың түзілуі.Содан соң реакцияның жүру жағдайлары қарастырылады.
Жаңа материалды бекіту үшін оқушылар төмендегі сұраққа жауап береді.
1. Мына құбылыстардың қайсысы химиялық құбылысқа жатады: а)қар қиыршықтары- ның түзілуі; ә) қанттың көмірленуі.
Одан соң сыныпта оқушыларға мына тапсырмаларды орындатамыз. Төменде келтірілген мысалдардан а) физикалық: ә) химиялық құбылысты бөліп жаз: парафиннің балқуы, жаңқаның көмірленуі, сүттің ашуы, темірдің таттануы, ағашта қыраудың пайда болуы , электр шамы қылының қызаруы, қанттың көмірленуі, қанттың суда еруі.
Үйге тапсырма беру. 1-8 жаттығулар,жұмыс дәптері 1-7 жаттығулар.
8.10.16
8-класс. Химия
Сабақтың тақырыбы:. Химиялық реакциялардың теңдеулері. Зат массасының сақталу заңы
Сабақтың мақсаты: Білімділік: Химиялық реакция теңдеулерін жазу, коэффициент қою,жазылған реакция теңдеулерін білу икемділіктерін қалыптастыру. Дамытушылық: реакция теңдеулерін теңестіре отырып логикалық ойларын дамыту. Тәрбиелік: Өз еркімен жұмыс жасауға, ойын жеткізе білуге тәрбиелеу. Сабақтың мақсаты: Білімділік: Оқушыларды зат массасының сақталу заңының мәнін ұғып, қарапайым мысалдар арқылы ойларын дамыту. Тәрбиелік: Өз еркімен жұмыс жасауға, ойын жеткізе білуге тәрбиелеу.
Құрал - жабдықтар. Кестеге жазылған алгоритм, элементтердің валенттілігі көрсетіл- ген кесте.
Темір, күкірт, мыс ұнтақтары, спиртшам, сынауықтар, тұрғы, зертханалық таразы.
Тірек, білім мен біліктер: Құрам тұрақтылық заңы, зат массасы, қоспалар, химиялық қосылыстар, химиялық реакция заттың салыстырмалы молекулалық массасын, зат массасын есептеу, химиялық қосылыстардың формуласын құрастыра білу.
Тірек білім мен біліктер: Заттың құрам тұрақтылық қағидасы, зат массасының сақталу заңы, химиялық формулаларды құрастыру.
Білім мен біліктерін тексеру: Заттың құрам тұрақтылығы жөніндегі қағида, қоспа мен химиялық қосылыстарды ажыратуға, химиялық қосылыс құрамын формула арқылы көрсетуге мүмкіндік туғызды.
1. Зат массасының сақталу заңының маңызы неде ?
Бұл сұраққа оқушылар өткен сабақта алған біліміне сүйене отырып жауап береді.
Мұғалім оқушылардың пікір алысуын, ойлау іс-әрекетін басқара отырып, тек зат масса- сының сақталу заңының ашылуы нәтижесінде химиялық формулаларды теңдеу ретінде көрсетуге мүмкіндік туды деген қорытындыға келтіру керек .
Осыдан кейін мұғалім оқушыларды сабақ мақсатымен таныстырып өтіп, жаңа материалды түсіндіруге кіріседі:
Судың айырылу реакциясын мысалға ала отырып теңдеудің сол жағы мен оң жағындағы формулаларды, қойылатын таңбаларды, индекстерді жазып көрсеткеннен кейін мұғалім химиялық реакция теңдеуінің коэффициенті деген жаңа ұғымды түсіндіреді. Оқушы коэффициенттің не үшін керектігін білу қажет. Осы мақсатта оқушыларға мынадай сұрақ беріледі:
1. Химиялық реакциялардың мәні неде?
Мұғалімнің оқушыларды химиялық реакцияның мәні бастапқы заттардың атомдары өзара қайта топтасып, жаңадан байланысуында деген тұжырым жасауына бағдарлау керек. Осыған сүйене отырып, мұғалім реакцияны коэффициент арқылы теңестіруді көрсетеді. Химиялық теңдеу коэффициенті жөніндегі білімін бекіту мақсатымен оқушыларға бірнеше теңдеуді теңестіру тапсырылады .
1/ ? AL + S = AL2S3
2/ ? Ca + O2 = ? CaO
3/ ? Fe + O2 = ? Fe2O3
Химиялық теңдеуді қалай оқуға болатындығын мұғалім көрсеткеннен кейін тақтадағы реакция теңдеулерін оқушыларға оқытады .
Жалпы бұдан былай қарай әрбір жазылған формуланы , химиялық теңдеуді ауызша оқытып отыру қажет, яғни оқушыларды химиялық тілмен сөйлей білуге дағдыландыра білген жөн . Оқушыларға химиялық теңдеулер дегеніміз не? деген сұрақ қойылады. Әрине оқушылардың жауабы толық дұрыс болмауы мүмкін . Бірақ бұл сұрақтың қойылуы оқушыларды ойландырып, сабақ барысында алған білімін қорытындылай білуге үйретеді.
Содан кейін мұғалім химиялық теңдеудің алгебралық теңдеуден айырмашылығына тоқталып өтеді .
Оқушылар химиялық теңдеулерді құру ережесін оқулықтан оқып , танысқаннан кейін төмендегі алгоритмді құрады. Ол үшін мұғалім алгоритмнің әрбір жолын өзінің қойған сұрағына жауап алғаннан кейін тақтаға жазып отырады немесе алгоритм кесте түрінде жазылған болса, мұғалім есепті шығару жолдарын қайталағаннан кейін таныстырып шығады. (Оқулықтан қарауға болады.)
Зат массасының сақталу заңын дұрыс түсініп, игеруін қамтамасыз ету мақсатымен оқушыларды жаңа ұғымды қабылдауға дайындау. Ол үшін оқушыларға көп сұрақтар қойылады.
-
Қоспа мен химиялық қосылыстың айырмашылығы неде?
-
Заттың химиялық формуласының маңызы мен қажеттігі неде?
Сұрақтарға жауап беру барысында оқушылардың өзара пікір алысуына көмектесе отырып, жаңа материалды қабылдауға қажетті ұғымдарды естеріне түсіру.
а) Алыну әдісіне қарамастан химиялық қосылыстардың құрамы тұрақты;
ә) Химиялық реакция кезінде атомдар сақталады.
б) Реакция нәтижесінде түзілетін өнімдер бастапқы алынған зат құрамындағы атомдардан құралады деген қорытындыға келу.
Осы қорытындыларға сүйене отырып, химияның негізгі заңдарының бірі - зат массасының сақталу заңын түсіндіремін. Сабақ мақсатымен таныстырамын.
1.Реакция кезінде атомдар сақталса, реакцияға түскен барлық атомдардың массасы сақтала ма?
Осы тұста оқушыларға белгілі темір сульфидін алу реакциясын көрсетуге болады. Заттардың құрам тұрақтылық қағидасына сай 7 г темір, 4 г күкірт өлшеп алу керек. Бастапқы заттарды өлшеймін, реакция аяқталғаннан кейін түзілген өнімді өлшеймін. Сонда түзілген өнімнің массасы 11 г, ал бастапқы алған заттардың жалпы массасы да 11 г-ға тең болады. (КК) Тәжірибені талдау нәтижесінде оқушылар химиялық реакцияда түзілген өнімдердің массасы бастапқы заттардың жалпы массасына тең болады деген қорытындыға келеді.
Іс жүзінде көпшілік жағдайда бұл ой дұрыс емес сияқты болып көрінеді. Неге?
Алдын ала өлшеніп алынған темір ұнтағы не мыс ұнтағы қыздырылады. Бастапқы заттың түсінің өзгергеніне оқушылар назарын аудара отырып, химиялық реакцияның жүріп жатқанын айтамын.Түзілген өнім өлшенеді. Бастапқы және реакция нәтижесінде түзілген өнімнің массалары тең емес екеніне оқушылардың көзі жетеді. Оқушылар үшін туған бұл қарама- қайшылықты М.В.Ломоносовтың жүргізген тәжірибесін айтып, түсіндіремін. Осыдан кейін оқушыларды зат массасының сақталу заңының қазіргі анықтамасымен таныстырып, дәптерлеріне жазғызамын.
Енді зат массасының сақталу заңының маңызына тоқталайық .
Біріншіден, бұл заң табиғатта заттардың жоқтан пайда болмайтынын немесе мүлдем жойылмайтындығын, яғни материяның мәңгі екендігін дәлелдейді. Осы арқылы оқушыларда материалистік көзқарас қалыптасады, дүние танымдары кеңейеді.
Екіншіден, бұл заң химиялық реакцияның мәнін ашады, яғни бастапқы заттардың құрамындағы атомдар реакция нәтижесінде түзілетін заттардың құрамына кіреді. Бастапқы заттардың атомдары өзара қайта топтасып, жаңадан байланысуының нәтижесінде жаңа заттар түзіледі.
Үшіншіден, бұл заң химиялық реакция теңдеуін жазуға, сол теңдеу көмегімен есептеу лер жүргізуге мүмкіндік туғызды. Демек ,бастапқы заттардың біреуінің массасы белгілі болса реакцияға түскен басқа заттардың не түзілген заттардың массасын есептеп шығаруға болады.
Мысалы: 12г күкіртті темір ұнтағымен қыздыру нәтижесінде 33г темір сульфиді түзілді.Қанша грамм темір реакцияға қатысты?
Берілгені: m(FeS) = 33г Шешуі: 33г - 12г = 21г Жауабы: m(Fe) = 21г
m(S) = 12г
Т/к: m(Fe) = ?
-
Массасы 24г мыс сульфиді түзілу үшін 16г мыс алынған. Ал күкірттің неше грамы керек?
-
Массасы 56г магний сульфидін алу үшін 32г күкірт жұмсалды. Ал магнийдің қанша грамы жұмсалады?
Сабақ соңында оқушыларға қойылатын бекіту сұрақтары:
-
Зат массасының сақталу заңын ашқан кім?
-
Зат массасының сақталу заңының анықтамасын айт.
-
Реакция нәтижесінде зат массасының сақталатынынқалай дәлелдеуге болады?
Жаңа материалды бекіту:
1.Мына реакция теңдеулерінің коэффициенттерін қойыңыз:
а) N2 + H2 NH3 ә) CO + O2 CO2
б) Al + Cl2 AlCl3 в) KOH + H2SO4 K2SO4 + H2O
г) MnO2 + H2 Mn + H2O
2.Реакция нәтижесінде шыққан заттардың формуласын валенттігі бойынша құрыңыз, және реакция теңдеулерінің коэффициенттері қойып теңестіріңіз:
III II II II V II
а) Al + S Al S ә) Ba + O2 Ba O б) P + S P S
Үйге тапсырма беру: (1-8) Жұмыс дәптері.
15.10.16
8-класс. Химия
Сабақтың тақырыбы: Химиялық реакциялардың типтері: орынбасу, алмасу;
Сабақтың мақсаты: Білімділік-химиялық реакциялардың типтерін түсіндіру, реакция теңдеулерін жазып, айтып беру дағдысын дамыту; Дамытушылық-реакция теңдеулерін теңестіруді орындай білуге дағдыландыру; Тәрбиелік-химия пәні нақты дәлелдемені қажет ететін ғылым екеніне оқушылардың көзін жеткізу.
Сабақтың типі: Жаңа білім беру
Сабақтың түрі: Аралас сабақ
Әдіс-тәсілдер: тәжірибе жасау, есептер шығару, интерактивті тақтамен жұмыс.
Сабақтың көрнекілігі: интерактивті тақта
Құрал-жабдықтар: сынауықтар, тұрғы, спиртшам, темір ұнтағы, күкірт, мырыш түйірі, калий перманганаты, тұз қышқылы,барий хлориді, натрий сульфаты ерітінділері.
Сабақтың жүру барысы:
I.Ұйымдастыру
II. Жаңа сабақ
Химиялық реакциялардың типтері 1.Қосылу 2.Айырылу 3.Орынбасу 4.Алмасу
Анықтамалары: Қосылу реакциясы-екі немесе бірнеше жай заттан бір күрделі заттың түзілуі.
Айырылу реакциясы -қүрделі заттың жай заттарға ыдырауы.
Орынбасу реакциясы-жай зат пен күрделі зат арасында,атомдарының орнын ауыстыруы арқылы жүретін реакция.
Алмасу реакциясы-екі күрделі заттың арасында жүретін ,атомдарының алмасуы арқылы жүретін реакция.
Мысалдар: Қосылу реакциялары: Fe+S=FeS 2Cu + O2=2CuO
Айырылу реакциялары: 2KMnO4→ K2 MnO4 + MnO2 + O2↑ CaCO3 → CaO + CO2↑
Орынбасу реакциялары: Zn+ 2HCl = ZnCl2 + H2↑ Mg + H2SO4 = MgSO4 + H2
Алмасу реакциялары: CaO + 2HCl= CaCl2 + H2O BaCl2 + H2SO4= BaSO4 + 2HCl
Тәжірибе көрсету:
1.Темір мен күкірттің қосылуы .
2.Калий перманганатының айырылуы.
3.Мырыш пен тұз қышқылының әрекеттесуі.
4.Барий хлориді мен натрий сульфатының реакциясы.
III. Білімді бекітуЕсеп-1.Мынадай реакциялар:-қосылу; - айырылу нәтижесінде мыс (II) оксидінің түзілуіне мысалдар келтіріңдер. 2Cu + O2=2CuO Cu (OH)2*CuCO3 =2CuO+ CO2↑+ H2O
Есеп-2.Төмендегі реакция теңдеулерін теңестіріп,типін анықтаңдар: Al + Cl2→ AlCl3 ,қосылу реакциясы NaHCO3 →Na2CO3 + CO2↑+ H2O , айырылу реакциясы Na2O + P2O5=Na3PO4, қосылу реакциясы
Есеп-3.Оттектің натриймен,магниймен,мырышпен,күміспен,алюминиймен қосылысының реакция теңдеулерін құрыңдар.
4Na+O2→2Na2O
2Mg+ O2→2MgO
2Zn + O2→ 2ZnO
4Ag+ O2→ 2Ag2 O
4Al + 3O2→ 2Al2O3
Есеп-4.Теңдеулерді толықтыр,теңестіріп.типін анықта.
1. 2Mg+ O2→2MgO
2. 2Fe (OH) 3 = Fe2O3+ 3H2O
3. Zn+ 2HCl = ZnCl2 + H2↑
4. 2HgO = 2Hg+ O2
Оқушылардың өзін-өзі бағалауы
Өте жақсы
Жақсы
Қанағаттанарлық
Теорияны практикада қолдану
Химиялық тілді игеру
Реакция теңдеулерін жаза білу
IV. Үйге тапсырма Химиялық реакциялардың типтері № 6, 9 есептер
V. Бағалау.
13.10.16
8-класс. Химия
Сабақтардың тақырыбы: Химиялық реакциялардың типтері:қосылу, айырылу
Сабақтың мақсаты: Білімділік: Қосылу, орын басу, айырылу және алмасу реакциялары жөніндегі ұғым, оларды химиялық теңдеулері бойынша ажырата білу білігін қалыптастыру. Дамытушылық: Химиялық реакцияның типтері бойынша есептер шығара отырып ойларын тереңдете дамыту.Тәрбиелік: Өз еркімен жұмыс жасауға, ойын жеткізе білуге тәрбиелеу.
Құрал- жабдықтар: Суды айыруға қажетті құрал, сынауықтар, спиртшам, мыс, мырыш, темір, мыс (II) хлоридінің ерітіндісі.
Сабақтың түрі: аралас сабақ.
Сабақтың әдіс - тәсілі: есептер шығару, оқулықпен жұмыс.
Тірек білім мен біліктері: Зат массасының сақталу заңы , валенттілік , жай және күрделі заттар жөніндегі білім; заттың химиялық формуласын, химиялық теңдеуді құрастыра білу біліктері.
Сабақ барысы: Зат массасының сақталу заңына сүйеніп, химиялық реакцияларды бастапқы және алынған заттардың белгілері бойынша бірнеше түрге бөлуге болады. Солардың бірі қосылу, айырылуы, орынбасу және алмасу реакциялары. Мұғалім оқушыларға реакцияның химиялық теңдеуін жазуды тапсырады.
Бұл сабақта химиялық реакцияның төрт түрі - қосылу, айырылуы, орынбасу және алмасу реакциялары. талданады . Мұғалім мысал ретінде мысты ауада қыздырып көрсетеді. Оқушылар реакцияға тек мыс қатысты деп қателесуі мүмкін. Сондықтан сұрақ қойылады: реакцияға мыстан басқа тағы қандай зат қатысады?
Реакцияға мыстан басқа ауадағы оттегі қатысатынын анықтап алғаннан кейін оның теңдеуін оқушылар мұғалімнің басқаруымен жазады. Ол үшін мыстың валенттілігін, оттегі молекуласында қанша атом бар екенін еске түсіреді. Келесі мысалды тәжірибе жасап , түсіндіруге болады . Көрнекі көрсету: мыс хлоридінің ерітіндісіне мырыш түйіршіктері салынады. Мұғалім реакция өнімі түзілу үшін элемент атомдары бірінің орнын бірі басатынын тәжірибе нәтижесінен көрсетеді. Одан әрі мұғалім реакцияға түскен және нәтижесінде түзілген заттар санының тұрғысынан жоғарыдағы екі теңдеуді салыстыра отырып, оқушыларды орын басу реакциясының анықтамасымен таныстырады, дәптерге жазғызады. Одан әрі мыс (ІІ) оксиді мен тұз қышқылы әрекеттестіріледі. Реакция нәти- жесіндегі өзгерістер түсіндіріледі. Тақтаға жазылған теңдеулерді оқушылардың өздері теңестіреді:
2Cu + O2 = 2CuO А + В = АВ
2H2O = 2H2 + O2 АВ = А + В
СuCI2 + Zn = ZnCI2 + Cu АВ + С = СВ + А
CuO + 2HCI = CuCI2 + H2O АВ + СД = СВ + АД
Оқушыларға оқулықтағы реакция типтеріне мысалды дәптерлеріне жазып алуды тапсыру.
Үйге тапсырма беру: 6-9 жаттығулар.
</ 20.10.16
8-класс. Химия
Сабақтың тақырыбы: Сандық есептерді шығару
Мақсаты: есептің шартын сауатты құра білу;
•есепке талдау жасай білу, зерттеу жүргізе білу;
•есептің типін анықтау;
•есептің шығару тәсілін таңдай білу, шығару жолының жоспарын жасау;
• масса мен көлем брліктерін Халықаралық жүйеге (СИ)- халықаралық жүйесіне келтіре білу;
• алынған жауапқа талдау жасай білу;
• қосымша әдебиетпен жұмыс жүргізе білу қабілеттерін қалыптастыру
Сабақтың түрі: аралас сабақ
Сабақтың әдісі:есептер шығару
Барысы:
Деңгейлік тапсырмалар№1
Химиялық формулалар бойынша есептеу(§7-§10)
І-деңгей
1. Мына элементтердің формуласын жазыңдар: қорғасын, сутегі, азот, алюминий, мыс, мырыш, алтын.
2. Оқылуы бойынша элементтің таңбасын жазыңыз: пе, плюмбум, це, эс.
3. H2SO4 күкірт қышқылының құрамындағы элементтерді атаңдар.
ІІ - деңгей.
1. күкірт қышқылының коэффиценттері мен индекстерін көрсетіп, осы заттың салыстырмалы молекулалық массасын есепте.
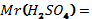
2.
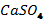 кальций сульфатының құрамындағы элементтердің массалық
үлестерін есептеңіз.
кальций сульфатының құрамындағы элементтердің массалық
үлестерін есептеңіз.
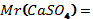
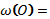
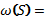
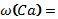
ІІІ-деңгей.
1. Қанттың құрамына: көміртектің 12, сутектің 22, оттектің 11 атомы кіреді. Оның химиялық формуласын жазып, оқыңдар, салыстырмалы молекулалық массасын есептеп, құрамындағы элементтердің массалық үлестерін есептеңдер
2. Химиялық элементтерге ребустар құрастыру
Деңгейлік тапсырмалар№2
Химиялықформулаларбойыншаесептеу(§7-§10)
І-деңгей
1. Мына элементтердің оқылуын және атауын жазыңыз.
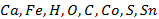
2. Мына элементтердің салыстырмалы атомдық массаларын және таңбасын жазыңдар: күміс, фтор, хлор, калий, литий
3. H3PO4 - фосфор қышқылы құрамындағы элементтерді атаңыз.
ІІ-деңгей.
1. Химиялық элементтер мен коэффиценттердің көмегімен жазыңдар: мыстың екі атомы, темірдің он атомы, алюминийдің екі атомынан оттектің үш атомынан тұратын алюминий оксидінің үш молекуласы.
2. Келтірілген формуланың оқылуын жазып, салыстырмалы молекулалық массасын және құрамындағы элементтердің массалық үлесттерін есептеңдер Mr(
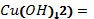
ІІІ-деңгей.
1. Берілгендеріне сәйкес химиялық қосылыстардың формуласын жазыңдар.
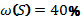
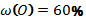
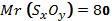
Табу керек:
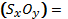 ?
?
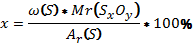
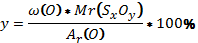
2. Химиялық элементтерге сөзжұмбақ құрастыру
Деңгейлік тапсырмалар№3
Химиялық элементтің валентілігі, химиялық заңдар, химиялық реакция теңдеулері
(§11-§14)
І -деңгей
1. Мына элементтердің таңбасын жазыңдар.
Магний, калий, барий, оттегі, күкірт, хлор, никель, мышьяк, марганец, алтын.
2. Француз ғалымы Ж.Пруст қандай заң ашты? Ол заң қалай тұжырымдалады?
3. Реагенттер мен өнімдер дегеніміз не?
4. Мына химиялық теңдеуден регенттер мен өнімдерді көрсет.
4Al+3O2=2Al2O3
5. Мына қосылыстың құрамындағы элементтерді атап, валенттілігін тауып, төбесіне жазыңдар.
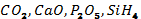
ІІ - деңгей.
1. Химиялық теңдеу дегеніміз не?
2. Химиялық реакция теңдеуін теңестіп, түзілген өнімдерді атаңдар.
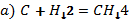
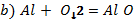
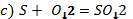
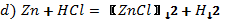
3. Бір ғана зат түзілетінін біле отырып, реакция теңдеулерін аяқтаңдар: а) барий+оттек(O2) =
б) натрий+ хлор(Cl2)=
в) мыс + оттек =
г) калий + күкірт =
д) литий + оттек =
4. Мына реакция теңдеуін теңестір, түзілген өнімді атап, оның молекулалық массасын есепте.
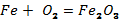
ІІІ-деңгей
1.Бос қалдырған орындарды толтырыңдар, коэффиценттерін қойып, теңестіріңдер, түзілген өнімді атаңдар.
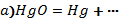
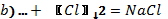
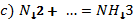
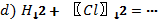
2. Теңдеулерде коэффициенттердің дұрыс қойылған-қойылмағанын анықтап, дұрыс мәнін қойыңдар.
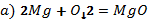
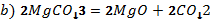
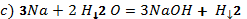
3. Мына қосылыстың құрамындағы элементтердің массалық үлестерін анықтаңдар:
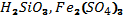
Деңгейлік тапсырмалар№4
Химиялық реакция теңдеулері, типтері, зат мөлшері, молярлық масса бойынша есептеулер(§15-§18)
І-деңгей.
1. Химиялық реакция теңдеулері қандай типтерге бөлінеді? Оларды атаңыз.
2. 2Mg+O2=MgO Мына теңдеу қандай реакция типтіне жатады? Ережесін айтыңыз.
3. Зат мөлшері мен молярлық масса қалай белгіленеді және олардың өлшем бірліктерін жазыңыз.
4. Мына заттың молярлық массасын есептеңіз:
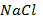
ІІ - деңгей
1. Берілген сызбанұсқаларда коэффиценттерді қойып теңестіріңдер, реакция типтін анықтаңдар.
a) Al+O2 =Al2O3
b) H2 + Cl2 = HCl
c) PH3 + O2 = P2O5 + H2O
2.Келтірілген валенттіліктері бойынша реакция нәтижесінде түзілетін заттың формуласын құрастырып, коэффициенттерін қойыңдар, реакция типтін анықтаңдар.
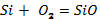
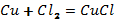
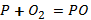
ІІІ-деңгей.
1.Төмендегі теңдеулерде қажетті заттың формуласын тауып, теңестіріңдер, реакция типін анықтаңыз.
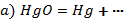
b) …+ … = AlCl3
c) Au2O3 = Au + …
d) … + N2 = NH3
e) HI = … + I2
2.
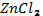 зат
мөлшері 0,5 моль осы заттың массасын және молекула санын
есептеңіз.
зат
мөлшері 0,5 моль осы заттың массасын және молекула санын
есептеңіз.
Деңгейлік тапсырмалар№5
Оттектің жалпы сипаттамасы, физикалық, химиялық қасиеттері (§20-§24)
І-деңгей.
1. Оттектің таңбасын, атомдық массасын, валенттілігін, физикалық қасиеттерін жазыңыз.
2. Өршіткі деген не?
3. Жану реакциясы дегеніміз не?
4. Мына затты атаңыз:
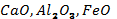
5. Ауа құрамын анықтаған ғалым кім?
ІІ - деңгей
1. Оттегінің лабораторияда алыну реакциясының теңдеуін жазыңдар.
2. Оттегінің темірмен, күкіртпен және фосформен әрекеттесу теңдеуін жазыңдар, түзілген заттарды атаңдар.
3. Мына оксидтерді атаңдар: мыс (ІІ) оксиді, күкірт (IV) оксиді, күміс (І) оксиді. Осы оксидтердің молярлық массасын есептеңдер.
4. Мына реакция теңдеулерін аяқтап, түзілген заттарды атаңдар:
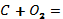
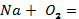
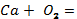
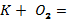
ІІІ-деңгей.
1. Мына өзгерістерді жүзеге асыратын реакция теңдеулерін жазып, түзілген өнімдерді атаңдар.
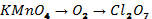
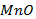
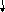
2. 3 моль азот (IV) оксидінің массасын есепте. Осы оксид құрамындағы әр элементтің массалық үлестерін есептеңдер.
3. 8 г оттегін алу үшін жұмсалатын сынап (ІІ) оксидінің массасын есептеңдер.
Сабақты бекіту: жалпылама сұрақтармен ауызша жұмыс
Бағалау:
Үйге тапсырма: 4-6 есептерді шығару
-