- Учителю
- Дидактические карты, которые можно использовать на уроках химии в 8 классе
Дидактические карты, которые можно использовать на уроках химии в 8 классе
Дидактические карты для первых пяти уроков химии в 8 классе, для проведения уроков в специальном (коррекционном) классе.
Материалы, могут использоваться как обучающие карты с учебной информацией. Материалы могут быть использованы учителем на любом этапе урока.
В создании карт использовалась информация учебника химии 8 класса под редакцией О.С. Габриеляна, материалы интернет-источников.
1. Введение. Предмет химии.
Известно, что человеку для жизни нужно не так уж много: кислород (воздух), вода, пища, одежда и жильё. Однако человек, осваивая окружающий его мир постоянно изменяет его. Создавая новые вещи, он делает свой быт более удобным и привлекательным; получая новые лекарства, избавляется от болезней; производя новые красители и волокна, делает более красивым одежду, жильё. Помогает всё это делать наука - химия. Химия относится к естественным наукам. Мы изучаем окружающий нас мир во всём многообразии его форм. Химия сложная и интересная наука.
Химия - это наука о веществах, их свойствах и превращениях
Химия как наука возникла в 18 столетии. Химическое производство существовало уже за 3 - 4 тысячи лет до н. э. Египетские жрецы владели приёмами бальзамирования тел умерших фараонов и знати. Демокрит в V в. до н. э., впервые высказал мысль о том, что все тела состоят из мельчайших, невидимых, неделимых твёрдых частиц материи, которые он назвал атомами. В Киевской Руси выплавляли металлы, производили стекло, соли, краски, ткани. При Иване Грозном в Москве в 1581г была открыта аптека.

Основоположником химии в России был М.В. Ломоносов

При изучении химии широко используют методы: наблюдение, эксперимент, моделирование.
Наблюдение - восприятие химических объектов (веществ, их свойств и превращений) с целью их изучения.
Эксперимент - исследования, которые проводят в строго контролируемых и управляемых условиях.
Моделирование - изучение объекта с помощью построения и изучения моделей, т.е. его заменителей.
!
Химия - это наука о веществах, их свойствах и превращениях
2. Вещества, их физические свойства.
2.1. Тела и вещества
Вспомни к уроку:
-
Химия
Всё бесконечное многообразие твёрдых, жидких и газообразных, окрашенных в разные цвета, блестящих, тусклых и прозрачных, обладающих различными запахами и прочими свойствами тел состоят из веществ.
Телами называют все предметы, окружающие нас.
Все тела состоят из веществ. Вещества бывают твердые, жидкие, газообразные (газ).



Вещество - это то, из чего состоит физическое тело
Многие вещества состоят из молекул, а молекулы из атомов. Атомы так малы, что на острие иглы их может поместиться много миллиардов.
Частицы, из которых состоят вещества, - это молекулы.
Молекулы невозможно увидеть невооружённым глазом, даже разглядеть в световой микроскоп. Хотя молекулы очень маленькие, они делимы, т.е. состоят из ещё более мелких частиц.
Частицы, из которых состоят молекулы, - это атомы.
В химии кроме терминов "атом" и "молекула" часто употребляется понятие "элемент". Что общего и чем эти понятия различаются? Химический элемент - это атомы одного и того же вида. Так, например, все атомы водорода - это элемент водород; все атомы кислорода и ртути - соответственно элементы кислород и ртуть.
Химический элемент - это определённый вид атомов.
В настоящее время известно более 107 видов атомов, то есть более 107 химических элементов.
2.2. Физические свойства веществ.
Свойства веществ - это признаки, по которым одни вещества отличаются от других.
Физические свойства веществ
Агрегатное состояние
 жидкость
жидкость
 твёрдое вещество
твёрдое вещество
 газообразное
газообразное
Цвет
Запах
Пластичность, хрупкость, эластичность
Температуры плавления и кипения
Плотность
Тепло и электропроводность
Вспоминай и объясняй.
1. Что такое вещество? Что из него состоит?
2. Что такое молекула, атом, химический элемент?
3. Какие физические свойства веществ тебе известны?
3. Практическая работа №1. Правила безопасности при работе в кабинете химии. Ознакомление с лабораторным оборудованием.
3.1. Правила безопасности при работе в кабинете химии.
Общие требования
1. Соблюдать все требования безопасности при работе в кабинете химии.
2. Во время работы в кабинете химии соблюдать дисциплину, поддерживать порядок на рабочем месте.
3. Начинать выполнение практической работы только с разрешения учителя.
4. Соблюдать правила техники безопасности при работе с веществами и оборудованием.
5. По первому требованию учителя остановить выполнение работы (опыта).
6. Немедленно сообщить учителю:
-
о получении травмы (порез, ожог), плохом самочувствии;
-
обо всех разливах жидкостей, а также о рассыпанных твердых реактивах;
-
обо всех неполадках в работе оборудования.
При возникновении в кабинете во время занятий аварийных ситуаций не допускать паники и подчиняться указаниям учителя.
В кабинете химии запрещается:








Соблюдай правила!



3.2. Ознакомление с лабораторным оборудованием.
Тема: Ознакомление с лабораторным оборудованием.
Цель: ознакомиться с лабораторным оборудованием.
Оборудование: лабораторный штатив, спиртовка, спички, колбы.
Ход работы
Название опыта
Рисунок
Пояснения к рисунку (сделать самостоятельно)
Вывод
(сделать самостоятельно)
Устройство лабораторного штатива
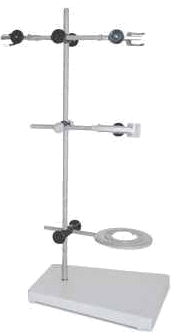

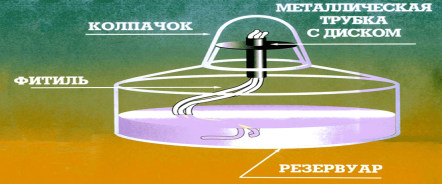
Приёмы обращения со спиртовкой
![]() ЭТИЛОВЫЙ СПИРТ
ЭТИЛОВЫЙ СПИРТ
![]() ЭТИЛОВЫЙ СПИРТ
ЭТИЛОВЫЙ СПИРТ
![]() ЭТИЛОВЫЙ СПИРТ
ЭТИЛОВЫЙ СПИРТ
Строение пламени

4. Чистые вещества и смеси. Способы разделения смесей.
4.1. Чисты вещества и смеси.
Чистые вещества в природе встречаются очень редко, чаще вещества встречаются в виде смесей.
Воздух представляет собой смесь кислорода, углекислого газа, азота и некоторых других газов; морская вода - смесь воды и солей; молоко - смесь воды, жира, белка; металлические изделия - смеси разных металлов, которые называются сплавами.
Слово "смесь" произошло от слов "смешивать", "перемешивать"
Смесь состоит из двух и более компонентов, находящихся в непосредственном контакте друг с другом.
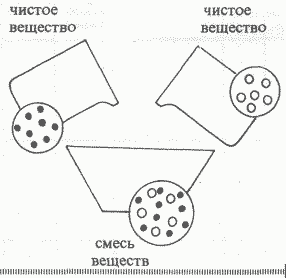
Рассмотрите рисунок:
Смесь - физико-химическая система, в состав которой входят два или несколько
Смеси
Однородные смеси (нельзя различить из чего состоит)
Неоднородные смеси (можно различить из чего состоит)




Расвор медного купороса, вода с поваренной солью
Вода с песком, вода с маслом
4.2. Способы разделения смесей.
Одна из задач экспериментальной химии - разделение смесей. Для чего нужно разделять смеси?
Разделение смесей - одна из наиболее распространенных операций в разл. отраслях промышленности. Так, отделяют золото от пустой породы, добываемую нефть от воды и т.д. Выделение жира из молока для получения из него сливок, сметаны и масла - также процесс разделения.
При изучении свойств вещества его надо иметь в чистом виде, иначе мы определим свойства не данного вещества, а его смеси с другими.
Способы разделения неоднородных смесей
Отстаивание
Фильтрование
Действие магнитом



Разделение смеси угля и воды
Разделение смеси глины и воды
Разделение смеси железа и серы
Способы разделения однородных смесей
Перегонка (дистилляция)
Кристаллизация
Плавление и кристаллизация
Возгонка и кристаллизация



Жидкая смесь
Твердая смесь
Твердая смесь
Твердая +жидкая смесь
5. Практическая работа 2. Очистка загрязненной соли.
Всё запиши в тетрадь
Тема: Очистка загрязненной поваренной соли методом фильтрования
Цель: научиться основным приемам фильтрования
Реактивы и оборудование: смесь NaCl и SiO2, H2O, стеклянный стакан, воронка, бумажный фильтр, стеклянная палочка, плоскодонная колба
Ход работы.
Название опыта
Что делали
Что наблюдали
Вывод
1. Растворение смеси в воде
Растворяли выданную смесь в 50 мл воды

Вывод о способности соли и песка растворяться
2. Фильтрова-ние
Изготовили складчатый фильтр, профильтровали выданную смесь

Вывод о возможности очистки соли методом фильтрования
3. Выпаривание
Полученный фильтрат выпарили в чашке для выпаривания

Вывод о способе разделения выпариванием