- Учителю
- Коррозия металлов и сплавов как результат, фактора загрязнения
Коррозия металлов и сплавов как результат, фактора загрязнения
9 класс химия "Знать - значит победить."
А. Н. Несмеянов
Класс 9 13.02.15
Урок № 43
Тема занятия
Коррозия металлов и сплавов как результат, фактора загрязнения
Ссылки, ресурсы
Учебник «Химия 9 класс», ТСО pedsovet.su/load/43-1-0-5078</</span>
Общая цель
систематизация знаний и способов действий по теме.
Цели урока
сформировать представление учащихся о механизме коррозийных процессов, об их последствиях и способах защиты от коррозии;
развивать умение работать с опорным конспектом, наблюдать, делать выводы;
воспитывать эмоциональное отношение к изучаемому явлению.
Задачи: познакомить учащихся с сущностью химической и электрохимической коррозии, со способами защиты от коррозии металлов и сплавов;
восстановить в памяти учащихся объяснение окислительно-восстановительных процессов;
сформировать эмоциональное отношение учащихся к данному явлению.
Результаты обучения для учителей
Освоили новую тему, учатся самооцениванию, фомируют навыки работы в группе
Ожидаемый результат
1. Самостоятельное формирование знаний, умений и навыков.
2. Умение отображать теоритические и практические навыки, закрепить и углубить знания, развить умение самостоятельно пополнять и систематизировать знания и пользоваться учебником и другими дополнительными источниками.
3. Соблюдать правила работы в коллективе при этом достигать поставленной цели через соперничество.
4.Выработать навыки самооценивания.
5. При работе с раздаточными материалами развить критическое мышление учащихся.
Этапы урока
Время
Действия учителя
Действия ученика
І. Организационный момент-5 минут
Рефлексия
Цель:
Проанализировать состояние психологического климата на уроках и выявить условия и факторы.
1минута
Предоставить различные смайлики с различными настроениями

Выбирают, соответствующие их настроению смайлики и крепят их на доске
Психологический настрой
1-2 минуты
Предложить ученикам стать в круг и сказать друг другу пожелания к уроку
Ученики становятся в круг и говорят пожелания
Распределение по парам:
1минута
Предлагает вытянуть жребий и разделиться на две группы «металлы» и «неметаллы»
Ученики садятся за столы с соответствующим названием
Создать «Правила группы»
1минута
Предлагает вспомнить правила в группе
Каждый ученик может озвучить одно правило
Стадия - ВЫЗОВ4-5 минут
ІІ. Проверка д/з
Что такое окислитель?
Что такое восстановитель?
Учащиеся отвечают на вопросы устно в течении 2 минут
ІІІ. Повторение пройденного материала:
2-3 минуты
Устная провека задании и выставление оценки.
Отмечают на оценочном листе свой полученные оценки.
IV. Подготовка к изучению новой темы:
«Проблемный вопрос»
1-2 минуты
1. 31 января 1951 г. обрушился железнодорожный мост в Квебеке (Канада ), введенный в эксплуатацию в 1947 г.
- в 1964 г. рухнуло одно из самых высотных сооружений в мире - 400-метровая антенная мачта в Гренландии.
- Из-за повреждений нефтепроводов в реки и на грунт выливается нефть.
Что же объединяет эти примеры? (разрушение металлических изделий)
Этот процесс и станет предметом нашего изучения на уроке. Разрушение, или правильнее разъедание, в переводе на латинский звучит как "кородире"
Тема нашего урока "Коррозия металлов".
Коррозия металлов…
Что поставить в конце предложения? Может знак ! или ? И нашей
задачей будет в ходе урока выработать собственное отношение к этому
процессу. А в конце урока каждый поставит в название свой знак
препинания.
Рассказ сегодня я буду вести с помощью опорного конспекта. У вас на
столах розданы такие же конспекты только в уменьшенном варианте.
- Как вы думаете, почему здесь изображен дракон?
Коррозию можно сравнить со сказочным Змеем Горынычем. Это давний и коварный враг большинства металлов. Но в отличии от него коррозия реально существует и, оставаясь невидимой, наносит огромный урон металлам и сплавам. И чтобы его победить, человек должен проникнуть во все его тайны, ведь не случайно эпиграфом к нашему уроку выбрано высказывание академика Несмеянова "Знать - значит победить."
Ученики:
Стадия «ОСМЫСЛЕНИЕ»12-13 минут
V. Изучение нового материала самостоятельно
Техника «Карусель»
5-6 минут
-
Проблемная ситуация: Колосс Родосский и затонувшая яхта миллионера.
В III до нашей эры на острове Родос был построен маяк в виде огромной статуи Гелиоса. Колосс Родосский считался одним из семи чудес света, однако просуществовал всего 66 лет и рухнул во время землетрясения.
В 20 годы ХХ в. один из американских миллионеров, не жалея денег, решил построить самую шикарную яхту. Ее днище было обшито дорогим металлом (сплав 70% никеля и 30% меди), а киль и раму руля изготовили из стали. В морской воде в подводной части яхты образовался гальванический элемент с катодом из металла, а анодом из стали. Он настолько энергично работал, что яхта еще до завершения отделочных работ вышла из строя, ни разу не побывав в море. Ученые считают, что в обоих случаях причиной произошедших событий были окислительно-восстановительные процессы. Какие именно?
Ответ: Причиной была контактная коррозия. У Колосса Родосского бронзовая оболочка была смонтирована на железном каркасе. Под действием влажного, насыщенного солями средиземноморского воздуха железный каркас разрушился.
Днище яхты было обшито медно-никелевым сплавом, а рама руля, киль и другие детали изготовлены из стали. Когда яхта была спущена на воду. Возник гигантский гальванический элемент, состоящий из катода- днища, стального анода и электролита - морской воды. В результате судно затонуло, ни сделав ни одного рейса.
При возникновении гальванической пары сила возникающего электрического тока тем больше, чем дальше стоят металлы друг от друга в ряду напряжений. При этом поток электронов от более активного металла идет к менее активному металлу. Более активный металл (железо), расположенный в ряду напряжений левее, будет разрушаться (т.к. является анодом), предохраняя тем самым менее активный металл от коррозии (медь).
Коррозионные процессы весьма разнообразны, рассмотрим их протекание в различных средах электролита.
В кислотной среде атомы железа отдают электроны, которые переходят к меди и на ее поверхности соединяются с ионами водорода, выделившимися из компонентов среды. На катоде идет процесс восстановления ионов водорода с образованием газообразного водорода.
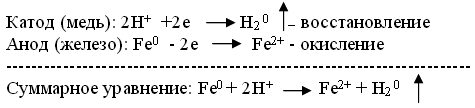
В щелочной или нейтральной среде идет восстановление кислорода, растворенного в воде с образованием OH-. Далее катионы железа и гидроксид-ионы соединяются с образованием неустойчивого гидроксида железа (II), который далее окисляется до оксида железа (III).
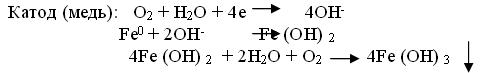
При использовании металлических материалов очень важен вопрос о скорости их коррозии. От чего зависит скорость коррозии?
2. 1 группа
1.Итак, что же такое коррозия?
В переводе с латинского слово "коррозия" - значит разъедать.
Примерно 20% железа ежегодно выплавляемого в мире разрушается от коррозии.
Коррозия - разрушение металлов под действием окружающей среды,
при этом металлы окисляются по схеме: ![]()
В зависимости от вызываемых коррозией повреждений поверхности металлов различают следующие ее виды: равномерную (сплошную),
равномерную (сплошную),
язвенную,
точечную (питтинг).
2.Как вы думаете какой вид коррозии самый опасный?
Почему? (Питтинг - большая глубина поражения и малая площадь)
2 группа По механизму протекания коррозия делиться на два вида: химическую и электро-химическую.
Химическая коррозия
- Как вы думаете, почему этот блок изображен в виде пламени?
Это вид коррозии протекает в средах, непроводящих электрический ток (газ, нефть, керосин ) или при высоких температурах, когда невозможна конденсация воды.
В результате химической коррозии происходит переход электронов от восстановителя к окислителю. Если прокалить медную проволоку в пламени, образуется серый налет, это и будет оксид меди.
Второй вид коррозии - электрохимическая.
- Какой процесс будет сопровождать этот вид коррозии?
- Что такое электрический ток с точки зрения физики?
Этот вид коррозии протекает в среде электролита.
3. этап: Читаем текст учебника и делаем пометки на полях: (я это знаю «+»; это новая для меня информация «√»; это мне непонятно «-»
При работе на постере приготовить раздаточный материал для работы в группе
Работа с информационными источниками
Стратегия «Инсерт»
2 мин
Дает сигнал напоминающий о регламенте- 1 минута
Команды поочередно выходят к доске и раскрывают тему
2-3 мин
Дает сигнал напоминающий о регламенте- 1 минута
Команды поочередно выходят к доске и раскрывают тему соперников
Стадия «РЕФЛЕКСИЯ» 13-15 минут
VI. Первичная проверка
усвоения нового материала:
-
мин
1. Ответить на вопросы теста. (ответом будут буквы, составляющие слово "коррозия" )
Тест
1. Слово "коррозия" в переводе с латинского означает:
и) разрушать;
п) окислять;
к) разъедать;
р) ржаветь.
2. Питтинг - это:
ж) электрохимическая коррозия;
н) язвенная коррозия;
о) точечная коррозия;
р) сплошная коррозия.
3. Окисление металла в среде не электролита:
а) электрохимическая коррозия;
г) язвенная коррозия;
о) точечная коррозия;
р) химическая коррозия.
4. Разрушение металла, находящегося в контакте с другим металлом в присутствии водного раствора электролита:
в) газовая коррозия;
и) химическая коррозия;
т) сплошная;
р) электрохимическая коррозия;
5. Эмалирование это:
б) способ предания красоты металлическому изделию;
е) электрохимический метод защиты металлов от коррозии;
о) защитное неметаллическое покрытие металла;
ч) защитное металлическое покрытие металла.
6. Легирование это:
з) специальное введение в сплав элементов, замедляющих процесс коррозии;
и) покрытие железного листа слоем олова;
к) создание контакта с более активным металлом;
т) покрытие металла краской.,
7. Вещества, замедляющие процесс коррозии называются:
и) ингибиторы;
о) электроды;
н) протекторы;
т) краски.
8. Присоединение к защищаемому металлу другого, более активного металла называется:
а) металлопокрытие;
о) контактная защита;
р) легирование;
я) протекторная защита.
После проверки теста дается задание всему классу, которое выполняется в парах, по карточкам.
Несколько учеников озвучивают свои ответы.
VII. Закрепление полученных знаний
7-10 мин
Упр к теме Составление синквейна.
Вы познакомились с понятием коррозия, с механизмом и видами коррозии и теперь вы решили, какой знак поставить в конце предложения?
Выразить свое отношение к предмету изучения я вам предлагаю через синквейн:
Ученики отвечают на вопросы и решают задачи.
VIII. Подведение итогов
1-2 мин
Просит расмотреть смайлики на начало урока, если настроение изменилось исправить и смайлики
Исправляют улыбки у смайликов
IX. Оценивание
3 мин
Оценивание по оценочным листам.
Учащиеся оценивают работу друг друга
X. Информация о д/з
1-2 минут
Домашнее задание: прочитать параграф, упражнение к теме
Составьте синквейн, осмысливая все знания, что мы сегодня систематизировали об Э.О..
Источники, оснащение и оборудование
Учебник, карточки, жребий, ТСО
Анализ и оценивание практического занятия
Изменения к занятиям