- Учителю
- Урок по химии для 8 класса «Соли»
Урок по химии для 8 класса «Соли»
Проект учебной и совместной деятельности учащегося и учителя.
Тема: Соли.
Цели:
Воспитательная - продолжать развитие у учащегося адекватной самооценки на базе коллективной и индивидуальной учебной деятельности.
Развивающая - продолжить формирование знаний учащихся о классах неорганических соединений - классе солей. Учить сравнивать, анализировать, делать выводы.
Образовательная - формировать способность прогнозировать состав нового класса веществ.
Средства: растворы гидроксида натрия и соляной кислоты, лакмуса; бюретка, лупа, спиртовка, предметное стекло.
Ход учебного занятия.
-
Ориентировочно-мотивационный этап.
Перед началом урока учитель дает разъяснения учащимся, как будет оцениваться урок.
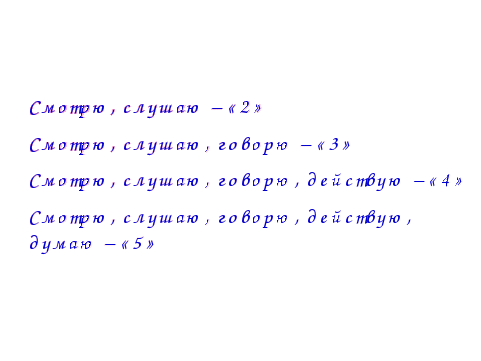
Каждому ученику предлагается в конце урока заполнить
На доске написаны формулы веществ: CaO, NaCl, H2SO4, Ca(OH)2,Na2O, CuSO4, HCl, KOH, K2O, HNO3, K3PO4, Fe(OH)3.
Деятельность учителя
Деятельность учащихся
Ребята, чем мы занимались на прошлом уроке?
На прошлом уроке давали характеристику оксидам и гидроксидам.
Выбирали металлические и неметаллические элементы, назначали соответствующие им оксиды или гидроксиды.
Каким способом? Приведите примеры.
Me →+O2 MeO →+H2O кислота
HeMe→+O2 HeMeO→H2O основания
На доске записаны формулы веществ, перепишите и подчеркните красной пастой кислоты, синей - основания, черной - оксиды. Кто хочет, может выписать отдельно оксиды, кислоты и основания.
Оксиды Кислоты Основания
Ca O H2SO4 Ca(OH)2
Na2O HCl KOH
K2O HNO3 Fe(OH)3
Ребята, для того чтобы сэкономить время, работайте в парах.
Самостоятельная работа учащихся
Давайте проверим. Кто хочет сказать, что такое оксиды, и написать их на доске?
За каждый правильный ответ поставьте по 1 баллу. Вы должны набрать 3 балла.
Оксиды: CаO, Na2O, K2O.
Оксиды - это сложные вещества, состоящие из атомов двух элементов. Один из которых - кислород в степени окисления -2
Кто хочет сказать, что такое кислоты и написать их на доске?
За каждый правильный ответ поставьте по 1 баллу. Вы должны набрать 3 балла.
Кислоты: Н2SO4, HCl, HNO3.
Кислоты - это сложные вещества, диссоциирующие в водном растворе с образованием только ионов H+.
Кто хочет сказать, что такое основание и написать их на доске.
Вспомните, какие вещества называются щелочами?
За каждый правильный ответ поставьте по 1 баллу. Вы должны набрать 3 балла.
Всего вы должны были заработать за все задания 9 баллов. Я думаю, что все справились с этим заданием.
Основания: Ca(OH)2, KOH, Fe(OH)3.
Основания - это вещество диссоциирующие в водном растворе с образованием гидроксид-ионов OH-.
Растворенные в воде основания называются щелочами.
Посмотрите, остались ли еще какие-нибудь вещества. Что это за вещества?
Да, действительно, данные вещества могут получиться в результате взаимодействия кислот и оснований. Чтобы ответить на вопрос, что это за вещества, отгадайте, что находится в черном ящике:
Давным-давно это вещество было на вес золота.
Без этого вещества нельзя обойтись при приготовлении пищи.
Его используют при осенних заготовках овощей и тд.
NaCl, CuSO4, K3PO4.
Может это те вещества, которые должны были бы получиться в результате взаимодействия оснований и кислот.
Соль
Это будет нашей новой темой, которую мы назовем…
Правильно. Запишите данную тему в тетрадь.
Соли
IIОперационно-исполнительский этап.
Внимательно посмотрите, подумайте и скажите, чем эти вещества отличаются от других раннее изученных классов.
Эти вещества отличаются тем, что состоят из атомов металлов и кислотного остатка.
Наверно вам интересно узнать, как они получаются?
Думаем, что они получаются при взаимодействии кислот и оснований.
Верно. Давайте проведем эксперимент. Не забудьте о правилах техники безопасности при работе с кислотами и щелочами. Осторожно прильем к раствору кислоты раствор щелочи.
Действия учащихся.
Что наблюдаете?
Никаких изменений нет, значит, реакции не было.
А какие изменения должны были быть?
Изменение цвета, появление запаха или осадка, выделение энергии.
Потрогайте пробирку.
Пробирка нагрелась, значит все-таки реакция была.
Какие же продукты образовались?
Может быть Na, Cl2, H2, O2. Может быть, Н2О и еще какие-нибудь вещества.
Как вы думаете, а какова сущность данной реакции?
Давайте попробуем прилить лакмус в щелочь и потом добавим кислоту
Зачем?
Чтобы пронаблюдать изменяется ли цвет. По изменению цвета, мы сможем узнать, какие вещества образовались
Хорошо. Вспомните тогда, какие ионы вызывают изменение цвета индикаторов. В нашем случае - лакмуса.
Ребята, если вы все помните об этом, поставьте себе 1 балл.
При диссоциации любой кислоты в растворе образуются катионы (Н+), которые окрашивают лакмус в красный цвет. При диссоциации любой щелочи образуются гидроксид-ионы(ОН-). Они окрашивают лакмус в синий цвет.
Итак, давайте приступим к выполнению предложенного вами эксперимента. К раствору щёлочи NaOH прилейте несколько капель раствора лакмуса. Затем из бюретки налейте небольшими порциями - хлороводородную кислоту HCl.
Что заметили?
Раствор приобретает синюю окраску.
Окраска лакмуса стала фиолетовой. Значит, среда раствора стала нейтральной.
Это значит, что в растворе нет больше щелочи.
Тогда может быть, осталась кислота?
Нет кислоты тоже нет, так как лакмус в кислотной среде имел бы красный цвет. Может тогда ионы Н+ и ОН- исчезли?
Может быть. А как?
Изобразите в виде схемы.
Образовали воду - нейтральную среду.
Na+ + OH- + H+ + CI- = H2O + ?
Что же ещё образуется кроме H2O?
До реакции были ионы Na+ и CI-, значит они перешли в раствор, потому что состояние атомов натрия и хлора устойчивее. Поэтому они останутся после реакции неизменными.
Почему вы так думаете?
Атом натрия легко отдает свой электрон и образует катион натрия Na+, а атом хлора принимает электрон, образуя ион CI-. Поэтому я могу написать так:
Na+ + OH- + H+ + CI- = H2O + Na+ + CI-
Молодцы! Все, кто думает так, поставьте себе по 1 баллу. Ребята, будет ли между молекулами воды и ионами существовать связь?
Предположение детей. Кто-то может сказать, что молекулы воды как бы обволакивают ионы и могут образовывать неизвестную нам связь. Кто-то может сказать, что образуется NaCl.
Да, ионы натрия и хлора находятся в воде. Молекулы воды полярны, поэтому они будут ориентированы вокруг каждого из ионов и возникает ион-дипольная связь, которая довольно прочная.
Теперь понятно, почему мы не увидели, какое вещество образуется в пробирке. А увидеть это можно только тогда, когда от ионов оторвутся молекулы воды.
Правильно! А как же разорвать эту связь?
Может быть раствор нагреть, тогда связи разорвутся и вода улетит.
Не забудьте о правилах безопасности при работе со спиртовкой.
Выпаривание.
Рассмотрите через лупу кристаллы. Что вы видите?
Мы видим кристаллы, похожие на поваренную соль.
Вы получили кристалл поваренной соли. Так к чему же ведет реакция между растворами кислоты и щелочи?
Реакция ведет к образованию соли и воды.
Значит, данную реакцию мы можем назвать реакцией …
Солеобразования.
Какие реакции называются реакциями солеобразования?
Напишите в тетрадь определение. Повернитесь друг к другу и скажите, какие реакции называются реакциями солеобразования. Поставьте себе по 1 баллу, если правильно повторили, что такое реакции солеобразования и записали в тетрадь верное определение.
Реакции идущие с образованием соли. Реакции между кислотами и щелочами.
Любое вещество имеет название, как назовем это вещество?
Предположение детей: соль, натрий, хлор.
Название солей складывается из названий анионов кислотного остатка (в им. падеже) и названия катионов металлов (в род. падеже).
Теперь давайте попробуем дать название полученной соли.
NaCI - хлорид натрия
Подумайте и дайте определение новому классу соединений. Запишите в тетрадь, работайте в парах.
Оцените себя на 1 балл
Соль - это сложное вещество, в твердом состоянии построенное из катионов металлов и анионов кислотного остатка, в водном растворе диссоциирующееся на эти ионы.
Итак, в начале урока мы с вами рассмотрели вещества и разделили их на классы, среди которых были иные вещества. Еще раз перечислим их и назовем.
Теперь вы знаете, какие это вещества, и какому классу они относятся.
NaCl - хлорид натрия
CuSO4,- сульфат меди
K3PO4.- ортофосфат калия
III Рефлексивно-оценочный этап
Какая тема была сегодня на уроке?
Если вы все поняли, расскажите мне, а потом друг другу что такое соли, как их можно получить. Работайте в парах и оцените друг друга. Подсчитайте количество баллов, которое вы получили за урок и поставьте себе оценку.
«Соли». Мы узнали о новом классе - классе солей. Узнали как они получаются. Как они называются.
Если вы получили:
13-12 баллов -5. Молодцы!
11-9 баллов - 4. Хорошо!
8-6 баллов - 3. Неплохо!
Сегодня мы с вами узнали, каким способом можно получить новый класс веществ. А как вы думаете, чем мы будем заниматься с вами на следующем уроке?
Будем учиться составлять формулы солей и называть их. Узнаем о новых солях.
Правильно!
Запишем домашнее задание: §60, подготовить сообщение о поваренной соли.
Спасибо за сотрудничество!