- Учителю
- Планирование урока по химии 'Степень диссоциации. Сильные и слабые электролиты'. (9 класс)
Планирование урока по химии 'Степень диссоциации. Сильные и слабые электролиты'. (9 класс)
Сабақты құру және жоспарлау кестесі
Сабақтың тақырыбы:
Диссоциациялану дәрежесі. Күшті және әлсіз электролиттер.
Сілтеме, көрнекіліктер
Химия 9 сынып М.Б.Усманова, Қ.Н.Сақариянова, электрондық оқулық.
Жалпы мақсаты
Оқушыларға диссоциациялану дәрежесінің мәнін меңгерту арқылы әлсіз және күшті электролиттер ұғымдарын қалыптастыру.
Міндеттері
Оқушылардың өздерін-өзі оқыту арқылы білім алуға ықпал жасау, сыни тұрғыдан ойлау үдерістері арқылы әр баланы қамтуға жағдай жасау. Оқушыларды ойланта отырып, өз беттерімен, жұппен және топпен жұмыс жасауға үйрету.
Қажетті құралдар
Ерітінділердің электрөткізгіштігін зерттейтін құрал, электролиттер ерітінділері.
Мұғалім үшін оқу нәтижесі
-
Диссоциациялану дәрежесі. Күшті және әлсіз электролиттер тақырыбын өздері меңгеріп шығуы.
-
Оқушыларды оқуға бағыттып отыру.
-
Бір-біріне көмектесуі.
-
Оқушыларды мадақтап отыру және оқушылардың өзін-өзі бағалауы.
Сабақта туындаған негізгі идеялар
Алған білімдерін өмірде қолдана алуына жағдай жасау, ойлау дағдыларын арттыру.
Күтілетін нәтиже
Диссоциациялану дәрежесін есептеу арқылы әлсіз және күшті электролиттерді ажырата білу.
Сабақтың әдісі
Баяндау, сұрақ-жауап, диалог, топпен жұмыс, жұппен жұмыс, жеке жұмыс, электрондық оқулықпен жұмыс.
Жалпы
-Білу:
Үй тапсырмасы:
Қышқылдар, сілтілер, тұздардың диссоциациялану үдерістерінің теңдеулерін құру.
-Түсіну:
Жаңа сабақ
1. Диссоциациялану дәрежесі. Күшті және әлсіз электролиттер.
2. Постер қорғау
-Қолдану:
Деңгейлік тапсырмаларды орындау
-Талдау:
Талдау, талқылау, салыстыру тапсырмалары
-Жинақтау:
электронды оқулықпен жұмыс
-Бағалау: Смайликтер арқылы
Бағалау бетшелері арқылы өз-өздерін бағалау
Сабақ жүрісі
Ойлау деңгейлері
Мұғалімнің іс-әрекеті
Оқушылардың іс-әрекеті
1. Ұйымдастыру
2. Сыныппен сәлемдесу, сабаққа қатыспаған оқушыларды белгілеу
3. Топқа бөлу: сыныптың оқушыларын түрлі-түсті стикерлер арқылы топқа бөлу
4. Оқушыларға бағалау критерийлерін ұсыну.
1. Мұғаліммен сәлемдесу
2. Оқушылар суреттер бойынша топтасып, өз үстелдерінің басына жиналады
Білу
Үй тапсырмасы:
Біліміңді сына!
1-топ: қышқылдардың диссоциациялану теңдеулерін құру.
2 -топ: сілтілердің диссоциациялану теңдеулерін құру.
3-топ: тұздардың диссоциациялану теңдеулерін құру.
Үздік оқитын оқушыларға үлестірме бойынша тапсырма беру:
-
көпнегізді қышқылдардың диссоциациялану теңдеулерін жазу;
-
қышқылдық және негіздік тұздардың диссоциациялану теңдеулерін жазу.
Тапсырманы топта талқылап, орындайды.
Әр дұрыс жауап 1 ұпайдан есептеледі.
Оқушылар жеке жұмыс жасайды, теңдеулерді жазып, қорғайды.
Негіздік және қышқылдық тұздар анықтамасын беру.
Семантикалық карта толтыру
Н+
ОН-
R-
Me+
Қышқыл
+
+
Негіз
+
+
Орта тұз
+
+
Негізік тұз
+
+
+
Қышқылдық тұз
+
+
+
Түсіну
-
тапсырма
1-топ: Диссоциациялану дәрежесі.
2 -топ: әлсіз және орташа электролиттер
3-топ: күшті электролиттер
Постер қорғау
Өзім қосымша түсіндіріп кетемін.
Электролиттің диссоциациялдану дәрежесіндегі айырмашылықты, олардың электрөткізгіштігі арқылы анықтауға болады. Ол үшін концентрациялы сірке қышқылының ерітіндісіне электрөткізгіштікті тексеретін аспаптың электродтарын батырып, ток көзіне қосамыз. Электр шамы әлсіз жанады.
Енді электродтарды тұз қышқылының ерітіндісіне салып ток көзіне қосамыз, аспаптың шамы жарқырап жанады. Бұның себебін түсіндіріңдер.
Мағынаны ажырату.
Тақырыптың басты идеясын табу, түсіндіру.
Сірке қышқылында диссоциацияланған молекулалар саны аз, сондықтан электр шамы әлсіз жанады, яғни электрөткізгіштік ерітіндідегі иондар санына байланысты болады. Ал тұз қышқылының ерітіндісінде диссоциацияланған молекулалар саны өте көп болғандықтан электр шамы жарық жанады.
Сергіту сәті
Қолдану
Деңгейлік тапсырмалар
-
«Тұз қышқылының диссоциациялану дәрежесі 90%» деген сөйлем нені білдіреді?
-
Егер электролит молекулаларының әр 200-нің 60-ы иондарға ыдыраса, сол заттың диссоциациялану дәрежесі қанша пайызға тең?
-
Барий гидроксидінің 0,01 моль ерітіндісіндегі иондар концентрациясын анықтаңдар, егер α
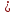 85% болса.
85% болса.
№3
Берілгені:
с(Ва(ОН)2 0,01моль/л
0,01моль/л
α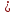 85%
85%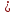 0,85
0,85
Табу керек: с1(Ва2+, ОН-) - ?
Шешуі: Ва(ОН)2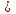 Ва2+ + 2ОН-
Ва2+ + 2ОН-
Моль 1 1 2
n(Ва2+)=1;
n(ОН-)=2; c = n/V
с1= c · α · 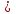
с1(Ва2+) =10-2 · 0,85 ·1= 8,5 · 10-3 моль/л
с1 (ОН-) =10-2 · 0,85· 2 = 1,7 · 10-2 моль/л
Талдау
Әр топтың шығарған есептерін талдау.
Оқушылар топ болып, берілген тапсырмаларды орындайды.
Өзара пікірталасқа түсіп, жауаптың дұрыстығын дәлелдейді.
Жинақтау
Диссоциациялану дәрежесінің мәніне қарай электролиттерді «Топтастыру» стратегиясы
күшіне қарай жіктеу:
H2CO3, HCI, NaOH, H2SO3, KOH, Mg(NO3) 2, CaSO4,
H3PO4, Na2SO4, HNO2, H2S, NH4OH, CH3COOH.
Алған білімді жинақтау.
Жеке жұмыс.
Бағалау
Рефлексия ББҮ кестесі
Оқушылар сабақ туралы пікірлерін, өз ойларын жазып ілу.
Үйге тапсырма:
Диссоциациялану дәрежесі. Күшті және әлсіз электролиттер.
Оқушыларға үй тапсырмасын жаздыру
Дайын бағалау парақшалары сабақ басында таратылды.
Әрқайсысы өз тұстарындағы ұпайларын есептеп, бүгінгі бағасын айтады.