- Учителю
- Конспект урока по химии на тему: Аммиак
Конспект урока по химии на тему: Аммиак
Зарецкая Оксана
Конспект урока по теме: «Аммиак и его свойства» (§24)
(О.С. Габриелян 9 класс)
Цель: сформировать у учащихся понятия о строении, составе, свойствах аммиака и его применении.
Задачи урока:
образовательные: изучить строение молекулы аммиака, его физические свойства и получение в лаборатории, сформировать у школьников новые понятия: аммиак, катион аммония, донорно-акцепторный механизм образования связи, соли аммония.
развивающие: сформировать в учениках наблюдательность при проведении демонстрационного лабораторного опыта по теме «Аммиак»; развить у учащихся умение логически мыслить и анализировать; продолжить формирование самостоятельной работы учащихся с учебником;
воспитательные: продолжить экологическое просвещение школьников; привить заботу к окружающей среде и здоровью.
Методы: словесный, наглядный, практический.
Оборудование и реактивы:. U-образная трубка, трубка заполненная активированным углем, раствор фенолфталеина, вода, штатив с лапкой, спиртовка, спички, пробка, пробирка, хлорид аммония, гидроксид кальция, газоотводная трубка, ступка с пестиком, шпатель, HCIконц.., фенолфталеин, раствор нашатырного спирта, круглодонная колба.
Организационный момент.
Цель перед учеником: организация рабочего места учащихся; наличие учебных принадлежностей; проверка оборудования и реактивов.
Цель перед учителем: проверить готовность учащихся к уроку; создать психологический настрой; выявление отсутствующих для определения пробелов в знаниях.
Методы: вводная беседа с целью организации учебной деятельности.
Здравствуйте, ребята. Скажите мне, кто отсутствует. Сегодня мы с вами повторим материал прошлого урока по теме «Азот» и изучим новую тему - «Аммиак и его свойства». Запишите название темы в свои тетради . Мы рассмотрим строение аммиака, его нахождение в природе, его физические и химические свойства, применение, также рассмотрим демонстрационный опыт.
Опрос учащихся по заданному на дом материалу.
Цель перед учеником: вспомнить материал по теме «Азот»; провести самооценку домашнего задания.
Цель перед учителем: проверить подготовку учащихся по теме «Азот»; проконтролировать самостоятельную работу учащихся; выявить готовность учащихся к восприятию нового материала.
Метод: фронтальный опрос по понятиям; индивидуальная работа с дидактическим материалом.
Отметка: «5»- 75-100%
«4»- 60-75%
«3»- 50-60%
«2»- менее 50%;
Ребята, на дом вам был задан §23-«Азот» и задачи №1,2,4 после параграфа. Я попрошу трех человек выйти к доске и подготовить домашние задачи для объяснения. С остальными мы проведём опрос. Итак, ответьте на следующие вопросы:
1. Выберите правильное утверждение о химических свойствах азота:
-
взаимодействует с кислородом (н.у.)
-
при взаимодействии с металлами образует нитриды
-
азот - высокоактивное вещество при нормальных условиях
2. Напишите продукты реакции:
N2 + Li =
3. Какие из живых организмов могут усваивать азот из воздуха?
4. Перечислите известные вам химические свойства азота?
5. Что в переводе с греческого языка значит азот?
6. С каким единственным веществом азот реагирует при комнатной температуре?
-Хорошо, а теперь давайте разберем домашние задачи. Дети, работающие индивидуально, сдают свои работы. (Оценивание ответов учащихся и выставление оценок)
Изучение нового учебного материала.
Цели для ученика: изучить химические и физические свойства аммиака на примере опыта получения аммиака, рассмотреть демонстрационные опыты; изучить новые понятия: аммиак, катион аммония, донорно-акцепторный механизм образования связи, соли аммония.
Цели для учителя:
Метод: рассказ с элементами беседы.
Теперь мы с вами переходим к новому материалу.
Демонстрация опыта.
В химическую колбу, в которой находится немного раствора аммиака
приливаем HCIконц..
- Вас взволновало то, что вы сейчас увидели, как густой дым наполнил колбу и начал выливаться на стол?
А представьте, как были взволнованы алхимики, когда имели дело с этим веществом!
Алхимики всегда с изумлением и мистическим ужасом наблюдали образование белого дыма при смешении этих двух газов. Они считали, что в воздухе встречаются два «духа», сражение которых заканчивается пролитием их «крови» - образованием дыма и белого налета на окружающих предметах.
Посредине ливийской пустыни стоял храм, посвященный богу
Амону Ра. В древности арабские алхимики получали из оазиса Амон, находившегося около храма, бесцветные кристаллы. Они звали вещество «нушадир», его растирали в ступках, нагревали - и всякий раз получался едкий газ. Сначала его именовали «аммониаком», а потом сократили название до «аммиак».
Аммиак NH3 - это самое важное из водородных соединений азота. В чистом виде аммиак впервые был собран в конце XVIII в. англичанином Дж. Пристли. Однако несмотря на то, что ученый смог описать свойства аммиака, ему не удалось определить состав соединения из-за несовершенства существовавших в то время экспериментальных методик. Заслуга в этом принадлежит К. Л. Бертолле. Он разложил аммиак действием электрической искры и получил точные данные о его количественном составе.
Далее проводится беседа о распространении данного вещества в окружающем мире.
Вопросы для обсуждения:
-
Содержится ли аммиак в атмосфере Земли?
В средние века этот газ называли почему - то «щелочной воздух», а его раствор и поныне называется «нашатырный спирт».
- Давайте, ребята, проведем небольшое исследование и решим, откуда у этого газа столь необычные свойства и названия
-
Объяснение нового материала.
-
Физические свойства аммиака: NH3↑, Ц , запах (резкий, удушливый), tкип.= -33,4 ◦С, tпл. = -77,8 ◦С,
ЯДОВИТ.
-
Строение молекулы аммиака.
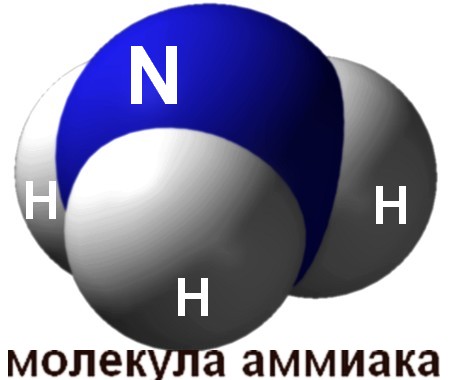
Молекула аммиака NH3 имеет пирамидальное строение. Атом азота N находится в центре незавершенного тетраэдра с тремя атомами водорода Н в вершинах, а к четвертой вершине обращено электронное облако с парой электронов, не участвующих в образовании химических связей.
В подходящих условиях эта «неподеленная» пара электронов может
служить для присоединения катиона водорода в реакциях аммиака с
кислотами, либо для взаимодействия с водой.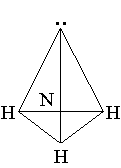
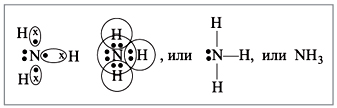
Аммиак очень хорошо растворим в воде: 1 объем воды растворяет при комнатной температуре около 700 объемом аммиака. И этот процесс - не простое растворение. Аммиак с водой объединяется в слабое основание гидрат аммиака NH3 ● H2O. Это происходит за счет того, что между атомом азота, обладающим неподеленной электронной парой, и атомами водорода молекулы воды возникает так называемая водородная связь.
Что такое водородная связь?
Это дополнительная связь между полярными молекулами, содержащими атом водорода. Если партнеры по химической связи в значительной степени переместили электронное облако к себе, то водород превращается в практически «голый» протон. И этот протон способен сильно притягиваться к богатым электронами электроотрицательным «соседям». Такие партнеры водорода, которые почти полностью лишают его электронного окружения - это элементы кислород, фтор или азот.
Вот почему химики говорят, что в воде, фтороводороде и аммиаке, а также в их водных растворах существует водородная связь.
Правда, водородная связь не очень прочна. Именно поэтому водные растворы аммиака всегда пахнут аммиаком: он постоянно выделяется из них в атмосферу.
Встречаем ли мы в быту водный раствор аммиака?
(выслушиваются ответы детей)
Водные растворы аммиака - вещь в хозяйстве очень нужная: с их помощью отмывают и отстирывают застарелую грязь, выводят жирные пятна на стекле и фарфоре, приводят в порядок золотые и серебряные ювелирные изделия, а иногда добавляют в жидкость для мытья оконных стекол.
Нашатырный спирт, который продается в аптеках, - это 5-10%-ный раствор аммиака в воде. В технике используется и более крепкий раствор аммиака (его максимальная концентрация составляет 25%). Такой раствор называется аммиачной водой.
По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных при ингаляционном поражении вызвать токсический отёк лёгких и тяжёлое поражение нервной системы.
Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы. Это человек и воспринимает как резкий запах. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог конъюнктивы и роговицы, потерю зрения, приступы кашля, покраснение и зуд кожи. При соприкосновении сжиженного аммиака и его растворов с кожей возникает жжение, возможен химический ожог с пузырями, изъязвлениями. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени. Запах аммиака ощущается при концентрации 37 мг/м³.
В медицине 10 % раствор аммиака, чаще называемый нашатырным спиртом</, применяется при обморочных состояниях (для возбуждения дыхания), для стимуляции рвоты, а также наружно - при укусах насекомых, для обработки рук хирурга. При неправильном применении может вызвать ожоги пищевода и желудка (в случае приёма неразведённого раствора), рефлекторную остановку дыхания (при вдыхании в высокой концентрации).
Применяют для возбуждения дыхания и выведения больного из обморочного состояния осторожно подносят небольшой кусок марли или ваты, смоченный нашатырным спиртом, к носу больного (на 0,5-1 с).
Физиологическое действие нашатырного спирта обусловлено резким запахом аммиака, который раздражает специфические рецепторы слизистой оболочки носа и способствует возбуждению дыхательного и сосудодвигательного центров мозга, вызывая учащение дыхания и повышение артериального давления. При укусах насекомых - в виде примочек. В хирургической практике разводят в тёплой кипяченой воде и моют руки.
Гидрат аммиака NH3 ● H2O в водном растворе, как и полагается слабому основанию, частично диссоциирует с образованием катионов аммония и гидроксид - ионов:
NH3 + H2O ↔ NH3 ● H2O ↔ NH4+ + OH-
В результате среда становится щелочной. Это будет заметно по малиновой окраски индикатора фенолфталеина в растворе нашатырного спирта.
Демонстрация опыта.
Добавить фенолфталеин в раствор нашатырного спирта.
А теперь попробуйте объяснить, почему в средние века этот газ называли «щелочной воздух», а его раствор и поныне называется «нашатырный спирт»?
Кроме гидроксид - иона, в реакции диссоциации, которую мы записали, появляется кое-что совсем новое - сложный катион. Это катион аммония NH4+.
Катион аммония NH4+ - частица совершенно симметричная и имеет форму тетраэдра, в центре которого расположен атом азота, а по вершинам четыре атома водорода.
H +
N•• + H+ → N [NH4]+
H H H H H H
ИОН АММОНИЯ
В ходе нашего эксперимента вначале урока мы видели, как появляется «белый дым», который выливался из колбы. Это мельчайшие кристаллики соли NH4CI - хлорида аммония.
Это протекает реакция: NH3 + НCI → NH4CI , или в ином виде
NH3 + Н+ = NH4+
Ничего удивительного, что в результате такого взаимодействия получается новый сложный катион. У молекулы аммиака, как уже было сказано, есть неподеленная пара электронов. А у катиона водорода нет вовсе, зато есть пустая атомная орбиталь, которая ждет не дождется дорогих гостей - чужую пару электронов. Поскольку катион водорода - частица с положительным зарядом, электроны притягивают ее очень крепко. Такой способ образования химической связи, когда один атом предоставляет электронную пару, а второй свободную орбиталь, химики назвали донорно-акцепторным механизмом. Здесь атом азота молекулы аммиака выступает в роли донора, отдающего свои электроны, а катион водорода - в роли акцептора. Его дело предоставить электронам азота удобную «квартиру» - атомную орбиталь.
В химическом отношении аммиак довольно активен; он вступает во взаимодействие со многими веществами. В аммиаке азот имеет самую низку степень окисления (-3). Поэтому аммиак обладает только восстановительными свойствами.
-
С кислотами соли
-
С водой основание
-
Аммиак азот + водород
t◦
2NH3 ↔ N2 + 3H2
(без kat) азот + вода
-
Аммиак + кислород
(kat) оксид азота (II) + вода
Если пропускать ток NH3 по трубке вставленной в другую широкую трубку, по которой проходит кислород, то аммиак можно легко зажечь; он горит бледным зеленоватым пламенем. При горении аммиака образуется вода и свободный азот.
4NH3 +3O2 → 2N2 + 6H2O
При других условиях (kat - Pt) аммиак может окисляться до оксида азота (II) NO.
-
При замещении в молекулах аммиака только одного атома водорода металлами образуются амиды металлов. Так, пропуская аммиак над расплавленным натрием, можно получить амид натрия NaNH2 в виде бесцветных кристаллов:
2NH3 + 2Na → 2 NaNH2 + H2
-
Аммиак - сильный восстановитель. При нагревании он восстанавливает тяжелые металлы из их оксидов, а сам окисляется до свободного азота:
3CuO + 2NH3 → 3Cu + N2 + 3H2O [2]
-
Получение аммиака.
Демонстрация опыта. Получение аммиака взаимодействием хлорида аммония с гидроксидом кальция.
В фарфоровой ступке тщательно перемешайте 5 мас. ч. хлорида аммония и 8 мас. ч. гидроксида кальция. Поставьте рядом три стакана: в один насыпьте хлорид аммония, во второй - смесь хлорида аммония с гидроксидом кальция, в третий гидроксид кальция. В стаканы на стеклянных палочках повесьте смоченные раствором фенолфталеина полоски фильтровальной бумаги.
Обратите внимание! В первом и третьем стакане полоски остаются без изменения, а во втором полоска остается розовой от выделяющегося аммиака.
В лаборатории аммиак обычно получают, нагревая хлорид аммония NH4CI с гашеной известью Са(ОН)2. Реакция выражается уравнением
2 NH4CI + Ca(OH)2 → CaCI2 + 2H2O + 2 NH3↑
Поскольку этот газ легче воздуха (масса 1 л аммиака при нормальных условиях равна 0,77 г), то его можно собрать в перевернутые вверх дном сосуды.
Эта реакция подтверждает, что нельзя одновременно известковать почву и вносить азотные удобрения, так как азот удобрения улетучиваются в виде аммиака.
б) Основным промышленным способом получения аммиака является его синтез из азота и водорода. Реакция экзотермическая, обратимая и протекает в присутствии катализатора:
kat, t◦, P
N2 + 3H2 ↔ 2NH3 + 46 кДж/моль
Закрепление учебного материала.
Цель для ученика: изучить и понять излагаемый учителем материал.
Цель для учителя: определить степень усвоения нового материала учащимися, выявить трудности в понимании изложенного и устранить все недочеты.
Методы:
Итак, сегодня мы разобрали тему «Аммиак и его свойства». Давайте закрепим изученный материал.
-
Закрепление.
Предлагается выполнить тестовое задание, которые потом проверяются в классе, вместе с учителем.
-
Степень окисления азота
-
Увеличивается 2. Уменьшается 3. Одинакова
в наборе соединений
а) NH3, Na3N, NH4CI
б) NH3, NO, HNO3
в) KNO2, N2O, NaNO3
г) N2O3, N2, Mg3N2
4-7. В веществе
-
NH3 2. NH3 ● H2O 3. NH4Br 4. N2
присутствуют химические связи
а) ионные
б) водородные
в) ковалентные полярные
г) ковалентные неполярные
8. В лаборатории аммиак получают при нагревании (выберите два правильных ответа)
а) NH4CI
б) NH3 ● H2Oконц.
в) N2 и H2 (катализатор)
г) (NH4)2SO4 и Ca(OH)2
9. Аммиак реагирует (по отдельности) с набором веществ
а) NH4CI, H2SO4
б) HNO3, Fe(OH)2
в) HCI, Mg(OH)2
г) Н2О, Н2SO4
10. Из 7,3 г хлороводорода и 7,3 аммиака получился продукт массой (в граммах), равной
а) 23
б) 16,8
в) 14,6
г) 10,7
11. Гидрат аммиака диссоциирует в растворе с образованием ионов
а) N3-
б) Н+
в) ОН-
г) NH4+
12. При образовании связи между молекулой аммиака и катионом водорода атомы азота и водорода по отношению к электронной паре являются
а) азот - донором
б) водород - акцептором
в) азот - акцептором
г) водород - донором
13. Геометрическая форма катиона аммония - это
а) треугольник
б) квадрат
в) тетраэдр
г) октаэдр
14. Соль аммония можно получить взаимодействием
а) NH3 и H2O
б) NH3 и HBr
в) NH3 и Na
г) NH3 ● H2O [5]
Задание на дом.
Цель для ученика: записать домашнее задание, усвоить ход его выполнения.
Цель для учителя: дать ученикам домашнее задание для лучшего изучения и усвоения материала.
Дома вы будете изучать §24. Просмотрите записи в тетради, ответьте на вопросы после параграфа. Сделайте в тетради небольшую таблицу о применении аммиака и его солей в народном хозяйстве. Таблица должна содержать колонки: свойство вещества и применение вещества.