- Учителю
- Урок по химии для 9 класса по теме «Железо»
Урок по химии для 9 класса по теме «Железо»
Урок по теме: «Железо или упавший с небес» (9 класс)
Цель урока: рассмотреть строение атома железа, как элемента побочной подгруппы, изучить свойства простого вещества железа и его соединений, нахождение в природе и его биологическая роль, рассмотреть качественные реакции на ионы железа.
Задачи:
-обучающие рассмотреть положение химического элемента железа в Периодической системе химических элементов Д. И Менделеева., строение атома. Изучить химические свойства простого вещества - железа, познакомиться с природными соединениями железа; рассмотреть биологическую роль железа;
-развивающие развивать интеллектуальные умения: выделять главное, анализировать, сравнивать, делать выводы, использовать ранее накопленные знания по химии в контексте нового материала, расширить научную лексику путем введения в активный словарь новых терминов, отработка ИКТ - компетентности;
-воспитательные воспитывать коммуникативные навыки, формировать научное мировоззрение, интерес к предмету, поддерживать устойчивую мотивацию к изучению химии на основании положительного эмоционального восприятия предмета и использования ИКТ - технологии.
Планируемые результаты обучения.
- учащиеся должны знать положение химического элемента железа в ПСХЭ, уметь характеризовать свойства атома на основании положения в ПСХЭ, особенности строения атома железа;
- уметь объяснять химические реакции, протекающие между простым веществом железом и простыми и сложными веществами;
- уметь записывать ОВР, указывать окислитель и восстановитель, процессы окисления и восстановления;
- знать общие физические свойства, области применения и биологическую роль железа.
Тип урока Комбинированный урок
Формы работы учащихся фронтальная, групповая, парная и индивидуальная работа
Необходимое техническое оборудование компьютер, проектор, химическое оборудование
Структура и ход урока
1. Психологический настрой
Здравствуйте ребята. Я рада видеть ваши лица, ваши улыбки, и думаю, что этот день принесет вам радость, общение друг с другом. Сядьте удобно, закройте глаза и повторяйте за мной: «Я в школе, я на уроке. Я радуюсь этому. Внимание мое растет. Я как разведчик, все замечу. Память моя крепка. Голова мыслит ясно. Я хочу учиться. Я готов к работе. Я работаю.
Отбросим в сторону переживания и неудачи.
Не опуская рук возьмемся за дела, мой друг,
И на уроке этом мы опять
Все поработаем на пять.
Cегодня я решила провести урок в форме особо важного задания. Любое задание, тем более особой важности, должно иметь сроки и оценку его выполнения. Срок нашего особо важного задания 45 минут, то есть протяжённость одного ученического часа. Чем же мы сегодня будем вооружаться? Оружия у нас нет, да и нет разрешения на его хранение, поэтому, мы сегодня можем вооружиться только своими знаниями, знаниями теоретическими, а также практическими навыками и умениями. Мишенями, что придется сегодня поражать, будут доска и человеческие сердца, сердца одноклассников перед которыми нельзя ударить в грязь лицом и моё сердце, которое надеется на положительный результат сегодняшнего урока.
Ну что ж, по-моему, все готово к началу основной части нашего боевого задания. Сверим часы, и, пожалуй, начнём.
1. Активизация знаний
Учитель: Ребята, скажите о чем мы с вами говорили на предыдущих уроках? (О металлах). Верно, вот сейчас вы мне и продемонстрируете свои знания о металлах. Проведем небольшой блиц-опрос, а поможет мне….
За каждый правильный ответ вы будете получать жетон. Чем больше жетонов вы наберете, тем выше оценка. На оценку пять нужно пять жетонов. Если вы наберете меньше, не страшно, это будет плюсом к вашей общей оценке за урок. У каждого на столе лист самооценки, в котором вы будете отмечать количество набранных вами жетонов.
-
Каковы особенности строения атомов металлов?
-
Самый распространенный на Земле металл. (Алюминий.)
-
Какие металлы самые активные? (Щелочные)
-
Какая область промышленности занимается получением металлов? (Металлургия)
-
Какие способы получения металлов вам известны? (пиро-, гидро-, электрометаллургия)
-
Какие металлы реагируют с водой при комнатной температуре? (активные)
-
Какие металлы не будут вытеснять водород из раствора кислот? (неактивные)
-
Какой металл чаще всего подвергается коррозии? (Железо.)
-
Назовите фамилию химика, впервые получившего натрий, калий, кальций, магний.
(Английский химик Деви)
-
Самый твердый металл. (Хром)
-
Металл- жидкость. ( Ртуть)
-
Самый пластичный металл. (Золото).
-
Какой металл убивает бактерий? (Серебро).
3. Мотивация
Выносят черный ящик под музыку. (в ящике гвозди, молоток, пила)
Ученик: Ребята послушайте историю и ответьте, что находится в черном ящике? Герою знаменитого романа Даниэля Дефо повезло. Корабль, с которого он спасся, сел на мель совсем недалеко от острова. Робинзон сумел погрузить на плот всё необходимое и благополучно переправился на остров. Ему повезло ещё раз - цитируем роман: «После долгих поисков я нашел ящик нашего плотника, и это было для меня поистине настоящей находкой». Что было в плотницком ящике? Обыкновенные железные инструменты: топор, пила, молоток, гвозди.
Я давно в названии века,
В организме человека.
Называют мной характер,
Из меня почти весь трактор.
Очень в яблоке полезно,
Одна легенда гласит: «Водяной царь сидит на троне, вокруг него танцуют русалки. Вдруг забрасываются сети и русалки уплывают, а царя рыбаки вытаскивают на берег. Взмолился царь, чтобы отпустили его обратно, за это он предложил выкуп: либо золота на 1 год, либо серебра на 10 лет, либо железа на вечные времена».
- Ребята, как вы думаете, что выбрали рыбаки (местные жители)?
Местные жители без сожаления выбрали железо. А водяной, судья по всему, свое слово сдержал: железные запасы до сих пор не иссякли.
Как видим, без железа не может обойтись даже приключенческая литература.
3. Целеполагание
Учитель: Итак, ребята какова же тема нашего урока? (Тема урока «Железо или «упавший с небес»»). А вопросом сегодняшнего урока будет «Продолжается ли век железный?»Мы должны опровергнуть это или доказать.
Эпиграф нашего урока - слова академика А. Е. Ферсмана: « …железо не только основа всего мира, самый главный металл окружающей нас природы, оно - основа культуры и промышленности, оно - орудие войны и мирного труда. и трудно во всей таблице Менделеева найти другой элемент, который был бы так связан с прошлым, настоящим и будущими судьбами человечества». сегодня на уроке вы в этом убедитесь.
Учитель: Ребята, давайте составим план по которому мы будет изучать данный металл.
Учащиеся высказывают свои идеи и составляют план.
-
Положение в ПСХЭ
-
Физические свойства
-
Нахождение в природе
-
Биологическая роль
-
Химические свойства
-
Способы получения
-
Соединения железа
-
Применение железа и его соединений
Посмотрите на пункты с 1 по 5 и сформулируйте цель нашего урока.
4. Работа в группах
Для погружения в урок используем приём «верите ли вы?». каждой группе даётся по 2 вопроса. на обсуждение 1 мин. затем представители групп отвечают на вопросы (6 групп).
Вопрос 1 группе:
Железо - первый по распространённости элемент - металл в составе земной коры. (Железо (Fe) - 2-й элемент по распространённости в природе металл (после алюминия (Al). В земной коре его массовая доля составляет 5,1%.)
Вопрос 2 группе:
В Древнем Риме из железа делали обручальные кольца. (Древние римляне первоначально предпочитали обручальные кольца из железа и лишь во II веке до нашей эры стали делать их из золота. Они считали, что металл в обручальном кольце отражает нерушимость брачных уз. В Древнем Риме такие украшения носили только женщины.)
Вопрос 3 группе:
Ежегодно из-за коррозии теряется около 25% всего произведённого в мире железа. (Ежегодно из-за коррозии теряется около четверти всего произведенного в мире железа. Появление ржавчины и разрушение металлов происходит под действием воды, воздуха, и так же кислотных дождей)
Вопрос 4 группе:
Один немецкий студент подарил своей возлюбленной кольцо, сделанное из железа его крови. (В теле здорового человека постоянно присутствует 4-5 граммов железа. Впервые железо в крови человека обнаружил в прошлом веке француз Мери. В истории медицины известен такой печальный случай. Один молодой студент-химик решил подарить своей возлюбленной кольцо, сделанное из железа собственной крови. Выпуская время от времени кровь, он получал соединение, из которого химическим путем выделял железо. Юноша погиб от наступившего малокровия. Он так и не собрал нужного количества железа для изготовления кольца.)
Вопрос 5 группе:
Железо - пластичный металл. (Железо высокой чистоты - это блестящий серебристо-серый, пластичный металл, хорошо поддающийся различным способам механической обработки. резанию, ковке, штамповке, прокатке.)
Вопрос 6 группе:
Из железа делают цистерны для перевозки соляной кислоты. (Лучший растворитель железа - соляная кислота. Чем крепче она, тем лучше. Соляная кислота разъедает цистерны с большим аппетитом. Чтобы не разъедала, в неё добавляют ингибитор или перевозят в гуммированных цистернах. Гуммирование - нанесение резинового или эбонитового покрытия на изделия, главным образом из металла и железобетона, с целью их защиты от коррозии и истирания.)
5. Изучение нового материала (работа по группам)
Учитель: Итак, ребята мы с вами погрузились в тему и теперь нам предстоит ответить на вопросы, которые мы сформулировали.
Каждая группа сейчас получит информационный кейс для работы и ответы на вопросы (6 минут).
Раздаём листы с вопросами, на которые ученики должны ответить в результате работы.
Желтый цвет ассоциируется с солнцем и интуицией, стимулирует нервную систему, укрепляет печень и сердце, повышает аппетит. Синий цвет ассоциируется со спокойствием и умом, снимает раздражительность. Красный цвет жизни, помогает бороться со стрессом, выводит яды и стимулирует чувственность, возвращает жизненную силу. Оранжевый увеличивает снабжение кислородом головного мозга, оказывает бодрящий эффект, стимулирует умственную деятельность. Розовый цвет, по уверению психологов, помогает бороться с депрессией. Зеленый связан с природой. Из-за своей связи с природой зеленый считается успокаивающим и расслабляющим цветом.
Историкам
1.Что означает слово» железо»?
2.Где впервые нашли железо?
3.Какие примеры доказывают, что железо - древнейший металл?
Геологам
1.Какие в природе распространены руды железа?
2.Какие месторождения железных руд есть в Оренбургской области?
Химикам-теоретикам
1.Где в ПСХЭ находится железо?
2.Каково строение атома железа (число электронов, протонов, нейтронов, электронная формула)?
3.Какие степени окисления проявляет железо?
4. Физические свойства железа
Экологам
1.Какие существуют экологические проблемы, связанные с железом?
2. Меры профилактики.
Биохимикам
1.В состав какого вещества клетки входит железо?
2.Сколько грамм в организме и суточная потребность?
3.Где применяется в медицине железо?
4.При недостатке железа какие продукты необходимо употреблять?
Историки: В таблице Менделеева трудно найти другой металл, с которым была бы так неразрывно связана история цивилизации. в древности у некоторых народов железо ценилось дороже золота. лишь представители знати могли украшать себя изделиями из железа, причем нередко в золотой оправе. В Древнем Риме из железа изготавливали даже обручальные кольца. в египетских гробницах наряду с другими ценностями, было найдено ожерелье, в котором железные бусины чередовались с золотыми. Век каменный сменился веком медным, потом - бронзовым, а затем веком железным. Учёные предполагают, что первое железо, попавшее в руки человека, было метеоритного происхождения. Не случайно на некоторых древних языках железо именуется «небесным камнем». Самый крупный железный метеорит Гоба нашли в 1920 г. в Африке, он весил около 60 т. название металла означает «капнувший с неба» или «небесный металл». В истории известен факт: бухарский эмир приказал своим оружейникам отковать ему меч и метеоритного железа, но у оружейников ничего не получилось, т.к. нагретый металл не поддавался ковке. Это произошло по причине того, что метеоритное железо, содержащее никель, куётся только холодным, а при нагревании становится хрупким. Вероятно, человек заметил, что после горения костра в некоторых случаях наблюдается образование железа из тех кусков руды, которые случайно оказались в костре. При горении костра восстановление железа идёт за счёт реакции руды как непосредственно с углём, так и с образующимся при горении угарным газом.
в нашей области железорудная промышленность стала развиваться в 18 веке, а в начале 20 века появились небольшие металлургические заводы
Химики-теоретики: Железо как элемент образуется множество соединений, проявляя обычно степени окисления +2,+3. Это оксиды FeO и Fe2O3 соответствующие им гидроксиды Fe(OH)2 и Fe(OH)3. Железо - элемент побочной подгруппы VIII группы 4-го большого периода. Железо относится к d-элементам. Железо в соединениях проявляет степени окисления +2 и +3.
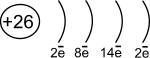 1s22s22p63s23p63d64s2
1s22s22p63s23p63d64s2
Металл средней активности, восстановитель.
Железо является вторым по распространенности металлом в природе (после алюминия).
Железо - серебристо-белый или серый металл, твердый, с высокой пластичностью, теплопроводностью и электропроводностью, плотность его равна 7,87 г/см3, тугоплавкий-1540? С0. В отличие от других металлов, железо способно намагничиваться. (демонстрация намагничивания)
Геологи: Железо встречается не только в метеоритах. В природе широко распространены руды железа:
Fe3O4 - магнетит
Fe2O3 - гематит
FeS2 - пирит
FeCO3 - сидерит
лимонит Fe2O3•nH2O
Редчайший каприз природы - самородное железо земного происхождения (его еще называют "теллурическим", от латинского "теллурс" - земля). Такое железо получается в уникальных геологических условиях - там, где потоки расплавленной лавы, богатой оксидом железа, на пути своего извержения из земных глубин пересекали пласты каменного угля. Метеоритное железо - всегда самородное.
В Оренбургской области разведано 8 месторождений железных руд .
Семь месторождений железных руд составляют Орско-Халиловскую группу, расположенную в Кувандыкском и Гайском районах области. Самые крупные - Аккермановское и Новокиевское.
Руды состоят в основном из лимонита, кроме железа содержат хром и никель. запасы руды невелики - 194,6 млн т.
В годы великой отечественной войны важнейшим центром передислокации тяжёлой промышленности из западных и центральных районов страны стал орско - халиловский район с его богатой рудной базой. Буквально с колёс начиналась жизнь прибывших заводов. на них изготавливали цилиндры для авиамоторов, корпуса фугасных снарядов, знаменитые «катюши», гильзы для снарядов, мины, гранаты. так в тылу ковалась победа.
Биохимики: Железо играет важную роль в жизни практически всех организмов, за исключением некоторых бактерий. При недостатке железа растения не образуют хлорофилла (что нарушает процесс фотосинтеза), теряют возможность ассимилировать углекислый газ и выделять кислород. Железо входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железо-белковых комплексов, которые находятся в печени и селезенке.
В организме взрослого человека имеется 4-5 г железа, из них 65% - в крови.
Красный пигмент крови - гемоглобин - осуществляет перенос кислорода от органов дыхания к тканям и обратный перенос углекислого газа от тканей к легким. в организм железо поступает вместе с пищей. Как вы думаете, в каких продуктах содержится больше всего железа? (обсуждение) в гречке, овсянке, фруктах (как определить железо в яблоках), черносливе, изюме, морской капусте, фасоли, петрушке. В пищевых продуктах содержатся соли железа со степенью окисления +3, а клетки кишечника пропускают только соли железа со степенью окисления +2, поэтому в желудке происходит восстановление fe2+ и fe3+, но, чтобы процесс был успешным необходимо тщательно пережёвывать пищу. Враги этого процесса: чай, кофе, алкоголь (прием даже умеренной дозы алкоголя выводит соединения железа из организма!).
Как правило, железа, поступающего с пищей, вполне достаточно, но в некоторых специальных случаях (, а также при ) необходимо применять железосодержащие и пищевые добавки (, ).
Экологи
Рассмотрим экологические проблемы, связанные с железом.
Пыль, дым промышленных производств могут содержать большие количества железа в виде аэрозолей железа, его оксидов, руд. Железо может накапливаться в почвах, водоемах, воздухе, живых организмах.
При воздействии на кожу возможны аллергические дерматиты, при вдыхании такого воздуха происходит раздражение дыхательных путей, разрушение легких, плевры, нарушения функции печени, желудочные заболевания. Поэтому установлено ПДК (Предельно Допустимая Концентрация) для железосодержащих частиц в воздухе рабочей зоны в зависимости от типа частиц от 2 до 4мг/м3.
Сульфаты и хлориды железа являются наиболее токсичными вредными примесями.
У рабочих, обрабатывающих пириты, наблюдаются желудочные заболевания (гастриты.
У рабочих железорудных шахт часты хронические бронхиты. Встречаются стоматиты, воспаления десен, поражения зубов, поражения слизистой рта.
Профилактика Очистка воздуха от вредных примесей, в эффективной вентиляции помещений, в применении спецодежды, респираторов, очков.
Токсичность соединений железа в щелочной среде возрастает. От избыточного содержания железа в воде могут гибнуть рыбы, водоросли. Большую опасность представляют сточные воды связанные с переработкой железосодержащих продуктов.
ПДК железа в питьевой воде 0,3 мг/л.
Далее проводится динамическая пауза (в это время звучит мелодия из серии «Звуки природы» либо используется по гиперссылке аналогичная музыка из этой же серии).
Закройте глаза и вспомните приятные моменты нашего занятия.
Я рада, что на протяжении всего занятия вы были внимательны.
Я хочу, чтобы все, кто работал хорошо - улыбнулись мне, а кто чувствует в себе потенциал работать еще лучше - поаплодировали себе.
Изучение химических свойств железа
Учитель: Ребята, давайте, попробуем предположить какими химическими свойствами может обладать железо? (высказывают идеи)
Железо взаимодействует как с простыми, так и сложными веществами.
Демонстрация видеоопыта (горение железа, взаимодействие с хлором, серой, с водой). Задание: записать уравнение реакции и составить электронный баланс. Чем является железо в данных уравнениях реакций?
У доски работают 3 человека.
-
3 Fe +2O2 = Fе 3O 4
-
При нагревании до 200-250 0С реагирует с хлором
2Fe+Cl2=2FeCl3
-
Fe+S=FeS
Действует ли вода на железо?
-
При обычных условиях вода не действует на железо, однако, в присутствии кислорода протекает следующая реакция:

Fe(OH)3 - гидроксид железа (III) - основная часть ржавчины. Для протекания данной реакции необходимо одновременно присутствие воды и кислорода, в противном случае коррозия так и не наступит. Известно, что в течение многих столетий стоит знаменитая железная колонна в столице Индии Дели. Почему? (Там сухой воздух).
Может вытеснять железо водород из воды? Да, может, но только при сильном нагревании (запись на доске).
-
Fe + H2O = FeO +H2
Fe0 - 2e = Fe+2 - восстановитель - окисление
2H+ + 2е = Н2 - окислитель - восстановление
Экспериментально рассмотреть взаимодействие железа с кислотами и солями. Записать уравнение реакции и наблюдаемый эффект.
-
Fe + 2HCI = FeCI2 + H2
-
Fe + CuSO4 = FeSO4 + Cu
Fe0 - 2e = Fe+2 (восстановитель)
Что вы наблюдали при проведении реакции? (Железо вытеснило медь из раствора сульфата меди)
В концентрированных азотной и серной кислотах железо не растворяется, так как на поверхности металла возникает пленка, препятствующая реакции металла с кислотой, поэтому концентрированные серную и азотную кислоты можно перевозить в железной таре (происходит пассивация металла).
Сделайте вывод о химической активности простого вещества - железа.
Выходят 2 учащихся в белых халатах - "доктор" и его "ассистент". Учитель представляет их классу.
Доктор: (держит в руках нож)
Вот еще одно развлечение:
Кто даст руку на отсечение?
Пауза.
Жалко руку на отсечение?
Тогда нужен больной для лечения. (Приглашают к столу ученика из класса.)
Ассистент.
Оперируем без боли,
правда, будет много крови.
Доктор.
При каждой операции
Нужна стерилизация.
Помогите, ассистент, дайте йод
Ассистент.
Один момент! (Подает "иод" - раствор FeCI3.)
Доктор.
Йодом смочим мы обильно,
Чтобы было все стерильно. (Тампоном, смоченным раствором FeCI3, смазывает обильно руку "пациента".)
Не вертитесь, пациент,
Нож подайте, ассистент! Скальпель "дезинфицирует" "спиртом" (раствором KSCN).
Доктор делает "разрез" ножом, смоченным обильно раствором KSCN, течет "кровь".
Ассистент: (испуганно)
Посмотрите, прямо струйкой кровь течет,
А не вода!
Доктор.
Не волнуйтесь!
Живой водой я смою руку
И от раны - ни следа! (Смывает "кровь" ваткой, смоченной раствором нашатырного спирта.)
Учитель.
"Этот опыт объяснить мы пока не можем
На следующий урок придем - объяснение найдем"
Тест соответствия.
Найдите соответствие между реагентами и продуктами:
Исходные вещества продукты реакции
Fe + H2SO4(p) à а) Fe(OH)3 + NaCl
Fe + Cl2 à б) Fe(OH)2 + NaCl
Fe + HCl(p) à в) FeCl2
FeCl2 + NaOH à г) FeCl2 + H2
Fe + О2 à д) FeCl3
е) FeSO4 + H2
ж) Fe3О4
Ответ оформите в виде таблицы:
1
2
3
4
5
Е
Д
Г
Б
Ж
Итоги урока
Итак, ребята, что сегодня мы с вами узнали на уроке. Ну и как мы ответим на наш вопрос: Продолжается ли век железа? достигли ли мы поставленной цели?
- что нового на уроке узнали?
- что было интересным?
Железо - основа всей металлургии, машиностроения, железнодорожного транспорта, судостроения, грандиозных инженерных сооружений - от башни Эйфеля до ажура железнодорожных мостов. Все, все - начиная от швейной иглы, гвоздя, топора и кончая паутиной железных дорог, плавающими крепостями - авианосцами и линкорами - и огнедышащими домнами, где рождается само железо, - состоит из железа. Железо - это металл созидания!
Выберите 1 фразу для соседа по парте:
Ты молодец.
Я доволен твоей работой на уроке.
Ты мог бы поработать лучше.
Заполнить листы рефлексии и самооценки.
Обращаясь к эпиграфу нашего урока, хотелось бы вам пожелать следующее: пусть ваш мозг истирается от работы мысли, а не пожирается ржавчиной от лени.
Так продолжается ли век железа?
Задачи
1.Суточная потребность человека в железе составляет 18 мг. В куске белого пшеничного хлеба содержится 0,8 мг железа. Сколько кусков хлеба нужно съесть в день для удовлетворения суточной потребности в этом элементе?
2.Требуется скрепить железные детали. Какими заклепками следует пользоваться - медными или цинковыми, чтобы замедлить коррозию деталей? Ответ обоснуйте.
Ответ: Если скрепить железные детали медными заклепками, то процесс электрохимической коррозии железа усилится, поскольку медь - менее активный металл, чем железо. Поэтому надо пользоваться цинковыми заклепками, которые замедляют коррозию железа. При этом сами заклепки буду корродировать быстрее, чем в отсутствие железа.
3.Почему применение чистого железа ограничено?
-
Ответ Чистое железо достаточно легко корродирует, поэтому его надо каким-то образом защищать от коррозии- либо покрывать защитным покрытием, либо применять в виде сплавов. Вычислите массу фисташек, которые необходимо съедать ежесуточно, для того чтобы восполнить суточную потребность организма в железе (20мг).
-
Как правильно принимать железосодержащие препараты? Напишите примерную инструкцию по их применению.
Железо в космосе, на звездах,
Железа много на Земле
Железо образует горы
Гора Магнитка, например.
Железо - труженик, строитель,
Станки, заводы, корабли
Ведь от иголки до машины
Все из железа состоит.
Железо в почве, в селезенке,
В любом растении, в крови...
В составе всех эритроцитов
Чудеснейший гемоглобин!
Таинственны земные недра,
Но физики убеждены:
Почти из чистого железа
Ядро земное состоит.
И верим мы, что век железа
Не станет веком роковым,
И дело мира неизбежно
Мрак на планете победит!
Технологическая карта к теме «Железо и его соединения»
Важнейшие руды железа
Магнетит-
Гематит -
Пирит -
Сидерит -
Лимонит -
Положение железа в ПСХЭ и строение его атома
Группа, период, электронная формула, степени окисления, восстановительные или окислительные свойства
Физические свойства железа:
Биологическая роль железа:
Суточная потребность
Продукты, содержащие железо
Химические свойства железа:
-
С простыми веществами (кислородом, хлором, серой)
-
С водой
-
С кислотами
-
С солями
Вопрос 1 группе:
Железо - первый по распространённости элемент - металл в составе земной коры.
Вопрос 2 группе:
В Древнем Риме из железа делали обручальные кольца.
Вопрос 3 группе:
Ежегодно из-за коррозии теряется около 25% всего произведённого в мире железа.
Вопрос 4 группе:
Один немецкий студент подарил своей возлюбленной кольцо, сделанное из железа его крови.
Вопрос 5 группе:
Железо - пластичный металл.
Вопрос 6 группе:
Из железа делают цистерны для перевозки соляной кислоты.
Тест соответствия.
Найдите соответствие между реагентами и продуктами:
Исходные вещества продукты реакции
Fe + H2SO4(p) à а) Fe(OH)3 + NaCl
Fe + Cl2 à б) Fe(OH)2 + NaCl
Fe + HCl(p) à в) FeCl2
FeCl2 + NaOH à г) FeCl2 + H2
Fe + О2 à д) FeCl3
е) FeSO4 + H2
ж) Fe3О4
Тест соответствия.
Найдите соответствие между реагентами и продуктами:
Исходные вещества продукты реакции
Fe + H2SO4(p) à а) Fe(OH)3 + NaCl
Fe + Cl2 à б) Fe(OH)2 + NaCl
Fe + HCl(p) à в) FeCl2
FeCl2 + NaOH à г) FeCl2 + H2
Fe + О2 à д) FeCl3
е) FeSO4 + H2
ж) Fe3О4
Тест соответствия.
Найдите соответствие между реагентами и продуктами:
Исходные вещества продукты реакции
Fe + H2SO4(p) à а) Fe(OH)3 + NaCl
Fe + Cl2 à б) Fe(OH)2 + NaCl
Fe + HCl(p) à в) FeCl2
FeCl2 + NaOH à г) FeCl2 + H2
Fe + О2 à д) FeCl3
е) FeSO4 + H2
ж) Fe3О4
Тест соответствия.
Найдите соответствие между реагентами и продуктами:
Исходные вещества продукты реакции
Fe + H2SO4(p) à а) Fe(OH)3 + NaCl
Fe + Cl2 à б) Fe(OH)2 + NaCl
Fe + HCl(p) à в) FeCl2
FeCl2 + NaOH à г) FeCl2 + H2
Fe + О2 à д) FeCl3
е) FeSO4 + H2
ж) Fe3О4
Историки:
1.Что означает слово» железо»?
2.Где впервые нашли железо?
3.Какие примеры доказывают, что железо - древнейший металл?
В таблице Менделеева трудно найти другой металл, с которым была бы так неразрывно связана история цивилизации. В древности у некоторых народов железо ценилось дороже золота. лишь представители знати могли украшать себя изделиями из железа, причем нередко в золотой оправе. В Древнем Риме из железа изготавливали даже обручальные кольца. В египетских гробницах наряду с другими ценностями, было найдено ожерелье, в котором железные бусины чередовались с золотыми. Век каменный сменился веком медным, потом - бронзовым, а затем веком железным. Учёные предполагают, что первое железо, попавшее в руки человека, было метеоритного происхождения. Не случайно на некоторых древних языках железо именуется «небесным камнем». Самый крупный железный метеорит Гоба нашли в 1920 г. в Африке, он весил около 60 т. название металла означает «капнувший с неба» или «небесный металл». В истории известен факт: бухарский эмир приказал своим оружейникам отковать ему меч и метеоритного железа, но у оружейников ничего не получилось, т.к. нагретый металл не поддавался ковке. Это произошло по причине того, что метеоритное железо, содержащее никель, куётся только холодным, а при нагревании становится хрупким. Вероятно, человек заметил, что после горения костра в некоторых случаях наблюдается образование железа из тех кусков руды, которые случайно оказались в костре. При горении костра восстановление железа идёт за счёт реакции руды как непосредственно с углём, так и с образующимся при горении угарным газом.
В нашей области железорудная промышленность стала развиваться в 18 веке, а в начале 20 века появились небольшие металлургические заводы
Химики-теоретики:
Химикам-теоретикам
1.Где в ПСХЭ находится железо?
2.Каково строение атома железа (число электронов, протонов, нейтронов, электронная формула)?
3.Какие степени окисления проявляет железо?
4. Физические свойства железа
Железо как элемент образуется множество соединений, проявляя обычно степени окисления +2,+3. Это оксиды FeO и Fe2O3 соответствующие им гидроксиды Fe(OH)2 и Fe(OH)3. Железо - элемент побочной подгруппы VIII группы 4-го большого периода. Железо относится к d-элементам. Железо в соединениях проявляет степени окисления +2 и +3.
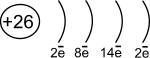 1s22s22p63s23p63d64s2
1s22s22p63s23p63d64s2
Металл средней активности, восстановитель.
Железо является вторым по распространенности металлом в природе (после алюминия).
Железо - серебристо-белый или серый металл, твердый, с высокой пластичностью, теплопроводностью и электропроводностью, плотность его равна 7,87 г/см3, тугоплавкий-1540? С0. В отличие от других металлов, железо способно намагничиваться.
Геологи:
1.Какие в природе распространены руды железа?
2.Какие месторождения железных руд есть в Оренбургской области?
Железо встречается не только в метеоритах. В природе широко распространены руды железа:
Fe3O4 - магнетит
Fe2O3 - гематит
FeS2 - пирит
FeCO3 - сидерит
Fe2O3•nH2O - лимонит
Редчайший каприз природы - самородное железо земного происхождения (его еще называют "теллурическим", от латинского "теллурс" - земля). Такое железо получается в уникальных геологических условиях - там, где потоки расплавленной лавы, богатой оксидом железа, на пути своего извержения из земных глубин пересекали пласты каменного угля. Метеоритное железо - всегда самородное.
В Оренбургской области разведано 8 месторождений железных руд .
Семь месторождений железных руд составляют Орско-Халиловскую группу, расположенную в Кувандыкском и Гайском районах области. Самые крупные - Аккермановское и Новокиевское.
Руды состоят в основном из лимонита, кроме железа содержат хром и никель. Запасы руды невелики - 194,6 млн т.
В годы Великой Отечественной войны важнейшим центром передислокации тяжёлой промышленности из западных и центральных районов страны стал Орско - Халиловский район с его богатой рудной базой. Буквально с колёс начиналась жизнь прибывших заводов. На них изготавливали цилиндры для авиамоторов, корпуса фугасных снарядов, знаменитые «катюши», гильзы для снарядов, мины, гранаты. так в тылу ковалась победа.
Биохимики:
Биохимикам
1.В состав каких соединений входит железо в организме человека?
2.Сколько грамм в организме и суточная потребность?
4.При недостатке железа какие продукты необходимо употреблять?
Железо играет важную роль в жизни практически всех организмов, за исключением некоторых бактерий. При недостатке железа растения не образуют хлорофилла (что нарушает процесс фотосинтеза), теряют возможность ассимилировать углекислый газ и выделять кислород. Железо входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железо-белковых комплексов, которые находятся в печени и селезенке.
В организме взрослого человека имеется 4-5 г железа, из них 65% - в крови.
Красный пигмент крови - гемоглобин - осуществляет перенос кислорода от органов дыхания к тканям и обратный перенос углекислого газа от тканей к легким. В организм железо поступает вместе с пищей. В сутки человек должен потреблять с пищей около 10-20 мг железа.
Как вы думаете, в каких продуктах содержится больше всего железа? в гречке, овсянке, фруктах (как определить железо в яблоках), черносливе, изюме, морской капусте, фасоли, петрушке. В пищевых продуктах содержатся соли железа со степенью окисления +3, а клетки кишечника пропускают только соли железа со степенью окисления +2, поэтому в желудке происходит восстановление fe2+ и fe3+, но, чтобы процесс был успешным необходимо тщательно пережёвывать пищу. Враги этого процесса: чай, кофе, алкоголь (прием даже умеренной дозы алкоголя выводит соединения железа из организма!).
Как правило, железа, поступающего с пищей, вполне достаточно, но в некоторых специальных случаях (, а также при ) необходимо применять железосодержащие и пищевые добавки (, ).
Экологи
-
Какие существуют экологические проблемы, связанные с железом?
-
Меры профилактики.
Рассмотрим экологические проблемы, связанные с железом.
Пыль, дым промышленных производств могут содержать большие количества железа в виде аэрозолей железа, его оксидов, руд. Железо может накапливаться в почвах, водоемах, воздухе, живых организмах.
При воздействии на кожу возможны аллергические дерматиты, при вдыхании такого воздуха происходит раздражение дыхательных путей, разрушение легких, плевры, нарушения функции печени, желудочные заболевания.
Сульфаты и хлориды железа являются наиболее токсичными вредными примесями.
У рабочих, обрабатывающих пириты, наблюдаются желудочные заболевания (гастриты).
У рабочих железорудных шахт часты хронические бронхиты. Встречаются стоматиты, воспаления десен, поражения зубов, поражения слизистой рта.
Профилактика Очистка воздуха от вредных примесей, в эффективной вентиляции помещений, в применении спецодежды, респираторов, очков.
Токсичность соединений железа в щелочной среде возрастает. От избыточного содержания железа в воде могут гибнуть рыбы, водоросли. Большую опасность представляют сточные воды связанные с переработкой железосодержащих продуктов.
ПДК (предельно допустимая концентрация) железа в питьевой воде 0,3 мг/л.