- Учителю
- Тест по теме Предельные углеводороды
Тест по теме Предельные углеводороды
ТЕСТ ПО ТЕМЕ «ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ»
Цель: систематизировать, закреплять, повторять и обобщать знания и умения по теме «Предельные углеводороды».
Тест включает 22 задания трех уровней. Задания базового, повышенного и высокого уровня сложности. Данный тест позволяет эффективно организовать подготовку учащихся к единому экзамену непосредственно на уроках в процессе изучения тем.
На выполнение теста отводится 45 минут. Задания рекомендуется выполнять по порядку. Часть 1 содержит тестовые задания с выбором одного правильного ответа. Ответом к заданиям части 2 является последовательность трех цифр, которые соответствуют номерам правильных ответов. В заданиях на установление соответствия нужно записывать буквы выбранных ответов в правильной последовательности. В части 3 необходимы объяснения, обоснование способа решения. Каждое задание части 1 оценивается в 1 балл, задание части 2 - 2 балла, а задания части 3 - 3 балла. Общее количество баллов равно 31.
Шкала перевода баллов в отметки:
0 - 9 баллов - «2»
10 - 15 баллов - «3»
16 - 22 баллов - «4»
23 - 31 баллов - «5»
Часть 1
При выполнении заданий части 1 нужно выбрать один правильный ответ.
А1. Дополните фразу: «Вещества, молекулы которых имеют одинаковый качественный и количественный состав, но разное химическое, а, следовательно, различные свойства, называются
-
гомологами
-
функциональными группами
-
изомерами
-
молекулами
А2. Дополните фразу: «Атомы или группы атомов, содержащих одну или несколько незавершенных электронных пар и за счет этого обладающих высокой реакционной способностью и коротким сроком жизни, называются …»
-
радикалами
-
функциональными группами
-
изомерами
-
гомологами
А3. Дополните фразу: «В углеводородах реализуется … связь»
-
ковалентная неполярная
-
ковалентная полярная
-
ионная
-
ковалентная неполярная и ковалентная полярная
А4. Формулы СН2---(СН2)2---СН3; СН3---СН2---СН2---СН3; СН3---СН2---СН3
-
трех разных веществ
-
одного вещества
-
двух разных веществ
-
одного вещества, называемого бутаном
А5. К классу алканов относится
-
С7Н12 2) С7Н16 3) С7Н6 4) С7Н8
А6. Число изомеров, имеющих формулу С5Н12, равно
-
5 2) 2 3) 3 4) 4
А7. Для алканов характерен тип реакции
-
замещения 3) обмена
-
соединения 4) присоединения
А8. Как правильно назвать хлорпроизводное углеводорода разветвленного строения?
С2Н5---СНСI---СН2---СН(СН3)---СН2---СН3
-
2-метилгептан-дихлор
-
3-метил-5-хлоргептан
-
3-хлор-5-метилгептан
-
дихлор-5-метилгептан
А9. Выберите пару веществ, являющихся гомологами
-
СН3---СН(СН3)---СН3 и СН3---СН(СН3)---СН2---СН3
-
СН4 и СН3---СНСI---СН3
-
С2Н6 и СН3---СН3
-
С3Н5Br и С3Н6
А10. Молекулы метана имеют геометрическую форму
-
тетраэдрическую
-
линейную
-
объемную
-
плоскую
Часть 2
Ответом к заданиям части 2 является последовательность трех цифр, которые соответствуют номерам правильных ответов.
В1. Пропан может реагировать с
-
метаном
-
хлором
-
раствором перманганата калия
-
бромной водой
-
кислородом
-
водой
В2. Реакция хлорирования метана
-
протекает по свободнорадикальному механизму
-
является реакцией присоединения
-
протекает в присутствии катализатора
-
является реакцией замещения
-
протекает на свету
-
без изменения степени окисления атома углерода
В3. Для предельных углеводородов характерны типы реакций
-
замещения
-
присоединения
-
дегидрирования
-
дегидратации
-
изомеризации
-
полимеризации
В4. Выберите признаки, характерные для структурных изомеров.
-
различные химические свойства
-
сходные химические свойства
-
разное строение
-
одинаковое строение
-
разный количественный состав
-
одинаковый количественный состав
-
различные физические свойства
В5. Выберите признаки, характерные для гомологов.
-
одинаковые физические свойства
-
Различные физические свойства
-
одинаковые и различные химические свойства
-
одинаковый количественный состав
-
разный количественный состав
-
одинаковое строение
-
сходное строение
В6. С метаном реагирует
-
HCI
-
CI2
-
NaOH
-
KMnO4
-
HNO3
-
O2
Часть 3
Запишите номер задания, а затем полное решение. Ответы необходимо записывать четко и разборчиво.
С1. Определите молекулярную формулу галогенпроизводного, если массовая доля углерода в нем составляет 24%, массовая доля хлора - 70%, а относительная плотность паров по воздуху равна 1,74.
С2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
+CI2 +2Na +AICI3
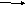
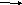
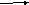 С2Н6 Х Х1
Х2
С2Н6 Х Х1
Х2
С3. Напишите уравнения реакций. с помощью которых можно осуществить следующие превращения:
+2Na +H2 +CI2
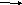
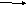
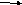 1,3-дихлорпропан Х
Х1 Х2
1,3-дихлорпропан Х
Х1 Х2
Ответы
С 1.
1.
Дано:
W(C) = 24%
W(CI) = 70%
Dв. = 1,74


Найти: CxHyCIz
Решение
-
М(вещества) = 29 * 1.74 = 50,5 г/моль
-
W(Н) = 100% -24% - 70% =6%
-
x: y: z =24%/12 : 6%/1 : 70%/35,5 = 2: 6 : 1?97 = 1 : 3 : 1
Простейшая формула CH3CI
M(CH3CI) = 12 + 3 + 35,5 = 50,5 г\моль
Ответ: CH3CI - хлорметан
С2.
-
С
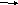 2Н2
+ CI2 C2H5CI + HCI
2Н2
+ CI2 C2H5CI + HCI
-
2
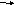 C2H5CI
+ 2Na C4H10 + 2NaCI
C2H5CI
+ 2Na C4H10 + 2NaCI
+AICI3
-
C
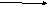 4H10
CH3 ---- CH(CH3) ---- CH3
4H10
CH3 ---- CH(CH3) ---- CH3
C3.
-
C
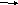 H2CI ----
CH2 ---- CH2CI + 2Na
C3H6(циклоалкан) + 2NaCI
H2CI ----
CH2 ---- CH2CI + 2Na
C3H6(циклоалкан) + 2NaCI
-
C
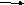 3H6
+ H2 C3H8
3H6
+ H2 C3H8
-
C
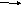 3H8
+ CI2 C3H7CI + HCI
3H8
+ CI2 C3H7CI + HCI
Литература
1.Рудзитис, Г.Е. Химия. Органическая химия. 10 класс [Текст]: учеб. для общеобразовательных учреждений: базовый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. - 14-е изд. - М.: Просвещение, 2011.-192 с.: ил. - 20 000 экз. - ISBN 978-5-09-025185-3.
2.Гара, Н.Н. Химия. Программы общеобразовательных учреждений. 8-9 классы 10-11 классы [Текст] / Н.Н. Гара // Пособие для учителей общеобразовательных учреждений. Базовый уровень. - 2-е издание. - М: Просвещение, 2009. - 56 с.: - 5000 экз. Заказ № 576. - ISBN 978-5-09-021793-4.
3.Соколова, И.А. Химия. 10-11 классы [Текст]: ЕГЭ тематические тренировочные задания / И.А. Соколова. - издание. - М: Эксмо, 2014. - 96 с.: - 2000 экз. - ISBN 978-5-699-74031-4.