- Учителю
- Конспект урока по химии по теме «Углекислый газ» 9 класс с использованием технологии критического мышления через чтение и письмо.
Конспект урока по химии по теме «Углекислый газ» 9 класс с использованием технологии критического мышления через чтение и письмо.
Конспект урока по химии по теме «Углекислый газ».
Предмет: химия.
Класс: 9.
Базовый учебник: О.С.Габриелян. Химия. 9 класс. Учебник для общеобразовательных учреждений. Рекомендовано МОиН РФ, 12-е издание, стереотипное. Дрофа, М., 2007.
Тип урока: урок усвоения новых знаний через работу с информационными источниками.
Технология: развитие критического мышления через чтение и письмо.
Методы: поисковый; репродуктивный, исследовательский.
Формы работы: индивидуальная; работа в парах, группах.
Оборудование и реактивы:
-
На столах учащихся: задание для выбора из перечисленных свойств тех, которые характерны углекислому газу (Приложение №2), инструктивные карточки (Приложение №3), текст с дополнительной информацией для приёма «инсерт» (Приложение №4).
-
Для выполнения эксперимента: пробирки, прибор для получения газов, вода, лакмус, соляная кислота, мел, мрамор, известковая вода, лучинка.
Цели урока: Познакомить с одним из представителей оксида углерода - углекислым газом, его строением, свойствами, развивать умения работать с химическим оборудованием и реактивами, сравнивать, анализировать, делать выводы, прививать интерес к предмету, воспитывать навыки коллективной работы.
Задачи урока:
-
обучающие:
- познакомить учащихся с углекислым газом как кислотным оксидом, раскрыть его свойства, биологическое значение и применение.
-
развивающие:
- продолжить формирование умений устанавливать причинно-следственные связи через умения прогнозировать свойства веществ на основе их строения, кислотно-основных свойств веществ;
- продолжить развитие предметных компетенций: умение составлять уравнения реакций, получать информацию из различных источников, конспектировать, выбирать главное, развивать умение учащихся работать с дополнительной литературой.
-
воспитательные:
- продолжить формирование коммуникативных компетенций при работе в группах;
- развивать критическое мышление через чтение информационного текста;
- воспитывать умение внимательно слышать и слушать другое мнение;
- прививать чувство ответственности за состояние нашей природы на основе формирования представлений о химической грамотности, экономической и экологической целесообразности использования оксида углерода (IV).
Технологическая карта урока
Цели
на каждом
этапе
Деятельность
учителя
Деятельность
учащихся
Педагогические
приемы
Система
ожидаемых
умений
1.Организационный момент урока
Приветствие учащихся, создание доброжелательной рабочей атмосферы, проверка готовности рабочего места ученика.
Приветствие учителя,
настрой на работу.
Этап урока: Вызов
1.Актуализация знаний по изучаемому вопросу
Учитель предлагает определить, о каком веществе идёт речь (читается одно утверждение по порядку):
1.Это вещество относится к оксидам. Твёрдый оксид носит название «сухой лёд».
2.Его обнаруживают с помощью известковой воды, которая впоследствии мутнеет.
3.Он образуется при прокаливании карбонатов.
4.Он не горит и не поддерживает горение, поэтому эти свойства позволяют использовать его в огнетушителях для тушения пожаров.
Выводит учащихся на тему урока.
Определяют вещество - углекислый газ.
Значит, тема урока «Углекислый газ».
Учащиеся индивидуально заполняют первую колонку таблицы «З-Х-У» записями о первоначальных знаниях об углекислом газе.
Составление таблицы «З-Х-У»
Умение использовать знания
из учебного и жизненного опыта.
2. Активизация деятельности учащихся
Заслушивание ответов учащихся, проверка первой колонки таблицы.
Учащиеся вслух отчитываются о проделанной работе, по необходимости дополняют записи первой колонки ответами одноклассников.
Фронтальный опрос
Развитие коммуникативных навыков.
3. Мотивация к дальнейшей деятельности.
Проблемная ситуация.
Учитель предлагает прослушать отрывок из произведения В. Короткевича «Чёрный замок Ольшанский. Дикая охота короля Стаха»: «… - Вы слышали об эффекте
«Собачьей пещеры» в Италии? … есть такая пещера - яма. Человек войдёт и ходит, а собака или кролик погибают через несколько минут.
- Почему?
- Из вулканической трещины выделяется углекислый газ … А поскольку он…»
Закончите фразу. Объясните «загадочную гибель животных».
Можете ли вы сейчас ответить на этот вопрос? Почему?
Ответ: (А поскольку углекислый газ тяжелее воздуха, то он остаётся внизу). Человеческая голова выше этой зоны. Собачья - нет…»
(Ответ не зачитывается учащимся, а предлагается ответить на него в конце урока)
Постановка новой познавательной задачи: предлагается заполнить вторую колонку таблицы, определить цели урока.
Ответы учащихся могут быть следующими: не знаем свойств углекислого газа, откуда попадает в пещеру углекислый газ и др.
Учащиеся заполняют вторую колонку таблицы (что бы хотели узнать нового о об углекислом газе), определяют цели урока.
Затем происходит обмен информацией (сравнение) в группе из 4 человек. После обсуждения каждая группа по очереди называет какую-то одну из целей урока, не повторяя ранее сказанное группами
(Приложение №1)
Составление таблицы «З-Х-У», определение целей урока.
Работа в группах.
Умение самостоятельно ставить новые задачи, определять цели урока.
Развитие коммуникативных навыков в группе.
Этап урока: ОСМЫСЛЕНИЕ
1.Формирование собственной позиции
Учитель предлагает написать формулу углекислого газа, найдите степень окисления углерода, определите тип химической связи в молекуле.
Учитель предлагает выявить среди перечисленных свойств те, которые характерны углекислому газу, аргументируя свой ответ.
(Приложение №2)
Учащиеся записывают формулу - С+4О2-2, с.о. +4, тип связи - ковалентная полярная.
Учащиеся находят правильные ответы сначала индивидуально, потом проверяют ответы в парах.
Работа в парах.
Фронтальный опрос
Умение систематизировать материал
из учебного и жизненного опыта
Умение слышать чужое мнение.
2. Получение новой информации.
Физические свойства СО2.
Учитель предлагает прочитать §30 стр. 173 (учебник «Химия» 9 класс под редакцией О.С.Габриеляна) с использованием приема «инсерт». Найти в тексте физические свойства углекислого газа и сравнить со свойствами, выбранными ими из списка. Учитель предлагает оформить полученные знания в третью колонку таблицы «З-Х-У».
Учащиеся читают информационный текст с использованием приема «инсерт», сравнивают физические свойства, выбранные ими из списка с физическими свойствами, описанными в учебнике.
Учащиеся заполняют третью колонку таблицы (что узнали нового об углекислом газе). Учащиеся озвучивают новую информацию вслух.
«Инсерт» (маркировка текста)
Умение работать с научным текстом. Умение отслеживать материал. Активизация внимания.
3.Пробуждение интереса к получению новой информации.
Размышление.
Учитель просит учащихся определить, какой характер у углекислого газа, и соответственно, какими химическими свойствами он будет обладать (с кем будет реагировать).
Учитель предлагает составить опорную схему.
Учащиеся выполняют задание. Записывают характер СО2 - кислотный, и составляют опорную схему:
 Н2О
Н2О
С
 О2 + основный
О2 + основный
оксид
щёлочь
Сопоставление записей. Фронтальный опрос. Взаимопроверка.
Умение систематизировать материал, составлять опорные схемы,
делать выводы,
4. Лабораторная работа. Получение и свойства углекислого газа
Учитель просит учащихся выполнить лабораторную работу, используя инструктивную карточку.
Учитель обращает внимание на признаки химической реакции. Инструкция учащихся перед началом выполнения лабораторной работы по технике безопасности.
Предлагается написать уравнения реакции и названия полученных веществ, используя учебник стр.174-175
(Приложение №3)
Учащиеся выполняют лабораторную работу, используя инструктивную карточку.
Используя учебник стр.174-175 записывают уравнения реакции и названия веществ.
Работа в парах.
Заполнение таблицы. Взаимопроверка.
Умение выявлять признаки реакции, составлять уравнения реакции, называть вещества.
5. Закрепление полученных знаний
Учитель предлагает прочитать текст с использованием приема «инсерт» и отметить, что они узнали в ходе сегодняшнего урока, а какая информация в тексте новая.
(Приложение №4)
Учитель предлагает оформить новую информацию в третью колонку таблицы «З-Х-У».
Учащиеся читают информационный текст с использованием приема «инсерт», отмечают, что они узнали в ходе сегодняшнего урока, а какая информация в тексте новая.
Учащиеся заполняют третью колонку таблицы (что узнали нового).
«Инсерт» (маркировка текста)
Умение работать с научным текстом. Умение отслеживать материал. Активизация внимания.
Этап урока: РЕФЛЕКСИЯ
1. Целостно обобщить полученную информацию
Учитель просит подготовить по таблице «З-Х-У» сообщение об углекислом газе.
Учитель снова предлагает прослушать отрывок из произведения В. Короткевича «Чёрный замок Ольшанский. Дикая охота короля Стаха»: «… - Вы слышали об эффекте
«Собачьей пещеры» в Италии? … есть такая пещера - яма. Человек войдёт и ходит, а собака или кролик погибают через несколько минут.
- Почему?
- Из вулканической трещины выделяется углекислый газ … А поскольку он…»
Закончите фразу. Объясните «загадочную гибель животных».
Можете ли вы сейчас ответить на этот вопрос?
Ответ: «А поскольку углекислый газ тяжелее воздуха, то он остаётся внизу. Человеческая голова выше этой зоны. Собачья - нет…»
Учащиеся готовят монологические ответы по теме, дополняют записи в таблице
Взаимопроверка по критериям оценивания
Умение целостно обобщать и систематизировать информацию
2 Домашнее задание
Прочитать §30 стр.173-175, написать применение углекислого газа, составьте синквейн по теме урока
синквейн
Приложение №1.
Приложение №2
Выберите из перечисленных свойств те, которые характерны углекислому газу:
-
Бесцветная жидкость;
-
Бесцветный газ;
-
Твёрдое вещество;
-
Не растворим в воде;
-
Плохо растворим в воде;
-
Хорошо растворим в воде;
-
Без запаха;
-
Имеет кислый запах;
-
Имеет резкий запах;
-
Легче воздуха;
-
Тяжелее воздуха;
-
Легко сжижается и затвердевает, превращаясь в снегообразную массу;
-
Не сжижается и не затвердевает.
-
Горит синеватым пламенем
-
Не поддерживает горение.
Приложение №3
Инструктивная карточка.
Лабораторная работа. Получение углекислого газа. Изучение химических свойств углекислого газа.
Цель: Получить углекислый газ и изучить его свойства.
Обратите внимание на технику безопасности при проведении опытов.
Ход работы:
-
Получите оксид углерода (IV) действием соляной кислоты на мел (карбонат кальция) в приборе для получения газов.
-
Пропустите полученный газ через воду, предварительно добавив в неё лакмус.
-
Затем углекислый газ пропустите через известковую воду.
-
Опустите в пробирку с углекислым газом горящую лучинку.
-
Опишите ход работы, отметив признаки реакций, составить уравнения реакций, сделать выводы.
-
Заполните таблицу:
Название опыта
Ход работы
Признаки реакции
Уравнения реакции, выводы
-
Получение
углекислого газа
В прибор для получения газов поместите кусочки мела или мрамора, добавьте соляную кислоту
2.Химические свойства углекислого газа:
Взаимодействие с водой
взаимодействие с известковой водой
Пропустите полученный газ через воду, предварительно добавив в неё лакмус
Пропустите полученный газ через известковую воду
3.Доказательство наличия в пробирке углекислого газа
Опустить в пробирку с углекислым газом горящую лучинку
Приложение №4
Прочитайте текст. По мере чтения карандашом на полях отметьте условными знаками:
-
- уже знал;
«+» - новое;
«-» - думал иначе;
«?» - не понял, есть вопросы.
Другие названия углекислого газа - оксид углерода (IV), или диоксид углерода.
Строение молекулы:
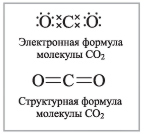
Обратите внимание на отсутствие свободных электронов у атома углерода, они принадлежат теперь и атому кислорода, и атому углерода. Атом углерода связан с атомами кислорода 4 общими электронными парами. В химических реакциях СО2 не может повышать в отличие от молекулы СО степень окисления, поэтому не может проявлять восстановительные свойства.
Большие количества углекислого газа поступает в атмосферу при дыхании растений и животных, а также при тлении их останков. За сутки каждый человек выдыхает в среднем более килограмма углекислого газа, а всё человечество ежегодно - около двух миллиардов тонн! При сжигании каменного угля, нефти, газа ежегодно выбрасываются в атмосферу 2 млрд. тонн углекислого газа, один автомобиль выбрасывает 3 тонны СО2.
Большие количества углекислого газа выбрасываются в атмосферу действующими вулканами. Так, например, известен случай, когда от выделившегося при извержении Везувия углекислого газа погибло (были задушены) множество мелких животных.
В некоторых местах земного шара углекислый газ постоянно в больших количествах выделяется из глубины земли. Около двадцати столетий известна человечеству «Собачья пещера» возле Неаполя. В ней тяжёлый углекислый газ стелется по дну пещеры слоем до полуметра. Собаки, попадающие в эту пещеру, задыхаются и погибают, хотя для человека пребывание в пещере безопасно. Отсюда и произошло название пещеры.
Мощные выбросы углекислого газа находятся и в Индонезии. Обширная и глубокая впадина, существующая у подножия одного из вулканов на острове Ява, известна под названием Долины смерти. Дно её усеяно множеством скелетов животных и даже людей, случайно попавших туда и задохнувшихся в атмосфере углекислого газа, наполняющего долину по трещинам земли.
Огромные количества углекислого газа выносятся водными источниками в местностях потухших вулканов. Всемирно известный курорт Кисловодск своим появлением обязан одному из источников «Нарзану». Ежесуточно этот источник выносит около двух с половиной миллионов литров минерализованной воды, содержащей до пяти тонн свободного углекислого газа.
Концентрация углекислого газа в составляет в среднем 0,03 %. Углекислый газ легко пропускает лучи, которые поступают на Землю от Солнца и обогревают её. В то же время он поглощает испускаемые Землёй лучи и является одним из , вследствие чего принимает участие в процессе .
В минувшие геологические эпохи в атмосфере содержалось значительно больше углекислого газа, и средняя годовая температура на Земле была значительно выше, чем сейчас. Вычисления показывают, что при полном удалении углекислого газа из атмосферы, средняя температура земной поверхности понизилась бы на 20º.
Но концентрация углекислого газа в атмосфере практически не изменяется, т.к. большое количество его поглощается растениями и участвует в процессе фотосинтеза.
Содержание этого газа в воздухе выше 3 % оказывает вредное влияние на организм человека. При содержании во вдыхаемом воздухе более 10% углекислого газа наступает остановка дыхания, потеря сознания, человек и другие животные погибают. Но так ли бесполезен для нас углекислый газ? У здорового человека содержание СО2 в крови должно составлять 6-6,5% от объёма всех растворённых там газов. А если это содержание углекислого газа по какой-то причине уменьшается, происходит спазм сосудов. Организм сужает просвет бронхов и кровеносных сосудов, стремясь уменьшить выброс углекислого газа и восстановить нужное его содержание в крови. При этом замедляется транспорт кислорода к клеткам, и, чтобы клетки не испытывали кислородного голодания, сердце увеличивает частоту биений, повышая кровяное давление. Так возникает гипертония, которая может привести к инсульту, т.е. прорыву кровеносных сосудов (чаще в мозгу).
Следовательно, от содержания углекислого газа в крови зависит не только здоровье, но и жизнь.