- Учителю
- Химические элементы в природе и их биологическая роль в организме человека
Химические элементы в природе и их биологическая роль в организме человека
Тема: « Химические элементы в природе и их биологическая роль в организме человека»
Цель данного урока:
Обучающая. Повторение, углубление и обобщение сведений о познаваемости природы химических элементов Периодической системы
Развивающая. Развитие "химического" мышления, умения обобщать и систематизировать полученное знание по курсу неорганической химии.
Воспитывающая. Формирование интереса к предмету, создание положительной психологической атмосферы, воспитание чувства взаимного уважения между собой, максимально раскрыться и показать способностей на уроке.
Форма урока: Беседа с элементами исследовательской и самостоятельной работы обучающихся, работа у доски, индивидуальная, групповая работа.
Наглядность: Периодическая таблица Д.И.Менделеева, Компьютер, Интерактивная доска
Девиз урока: "Повторение - мать учения".
ХОД УРОКА
-
Организационный момент. Подразделяется класс на 3 микрогруппы.
Итак, ребята, мы закончили курс неорганической химии, т.е. подробно разбирали химические элементы металлы и неметаллы, изучали их свойства и в составе неорганических соединений различных классов.
На доске написана тема: « Химические элементы в природе и их биологическая роль в организме человека»
Учитель. Целью сегодняшнего урока является повторение и обобщение знаний по этой теме в занимательной форме.
-
Стратегия «Мозговой штурм».
Вопрос №1.
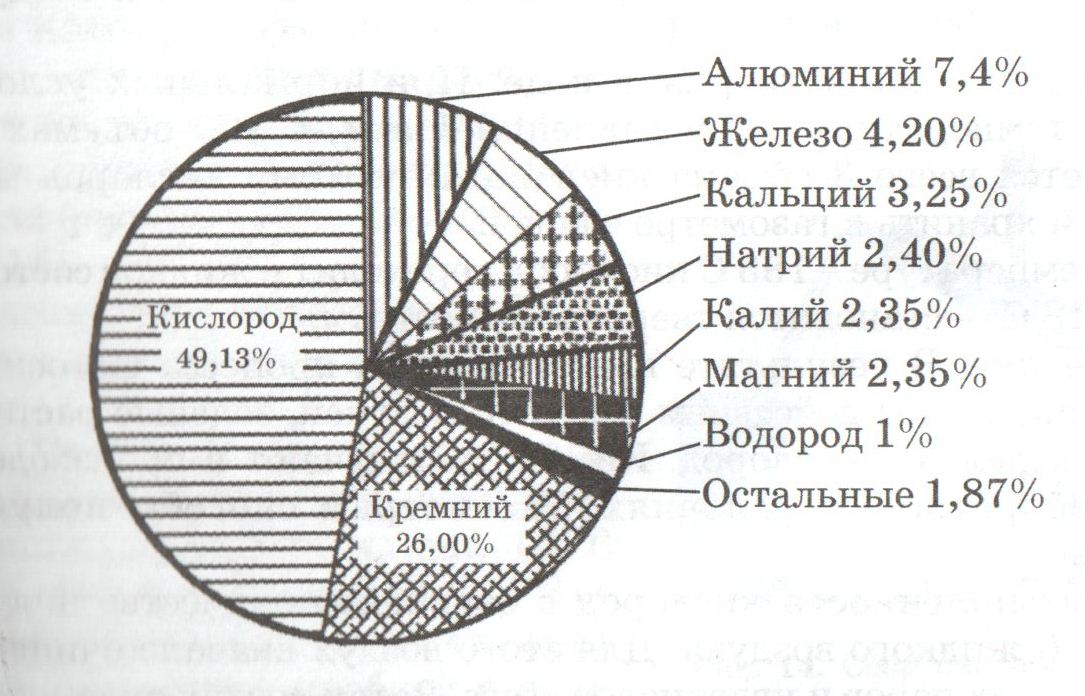
А) Назовите химический элемент, наиболее распространенный в земной коре. (О2, Н2, N2,Р, С,S)
В) В состав каких соединений входит этот элемент?
С) Каково его содержание в природе?
Ответ: Самый распространённый элемент в земной коре - кислород.
Всего по массе кислорода -![]() В атмосфере - 21 % кислорода ( по объему).
В атмосфере - 21 % кислорода ( по объему).
Почти все минералы в земной коре встречаются в виде оксидов и солей.
Например:
![]() -
песок, х.яз.называется оксид кремния и т..д. уч-ся далее должны
назвать эти вещества
-
песок, х.яз.называется оксид кремния и т..д. уч-ся далее должны
назвать эти вещества
![]() -
вода,
-
вода,
![]() -
железная руда,
-
железная руда,
![]() _
мрамор, известняк
_
мрамор, известняк
KMnO4- соль
NaHCO3 - пищевая сода
-
Задача № 2 Вычислите массу и количество вещества кислорода, прореагировавшего с цинком, если образовалось 16 г оксида цинка (II).
-
Вопрос № 2
Как получают кислород в лаборатории и в промышленности?
Напишите уравнения соответствующих реакций.
Чем отличаются эти способы друг от друга?
Ответы: В лаборатории кислород получают из сложных веществ. К таким веществам относяться перманганат калия KMnO4 и бертолетова соль KClO3
KMnO4 =t K2MnO4 + MnO2 + O2 ;
KClO3 =tMnO KCl + O2
В промышленности O2 получают перегонкой жидкого воздуха.
-
Также есть ещё наиболее распространённый химический элемент и наиболее распространённое вещество в нашей природе . Это - … . Уч-ся рассказывает про химический элемент Водород.
"Водород широко распространён в природе, его содержание в земной коре (литосфера и гидросфера) составляет по массе 1%, а по числу атомов 16%. Водород входит в состав самого распространённого вещества на Земле - воды (11,19% водорода по массе), в состав соединений, слагающих угли, нефть, природные газы, глины, а также организмы животных и растений (т. е. в состав белков, нуклеиновых кислот, жиров, углеводов и др.). В свободном состоянии водород встречается крайне редко, в небольших количествах он содержится в вулканических и других природных газах. Ничтожные количества свободного водорода (0,0001% по числу атомов) присутствуют в атмосфере. В околоземном пространстве водород в виде потока протонов образует внутренний ("протонный") радиационный пояс Земли. В космосе является самым распространённым элементом. В виде плазмы он составляет около половины массы Солнца и большинства звёзд, основную часть газов межзвёздной среды и газовых туманностей. Водород присутствует в атмосфере ряда планет и в кометах в виде свободного H2, метана CH4, аммиака NH3, воды H2O, радикалов типа CH, NH, OH, SiH, PH и т. д. В виде потока протонов водород входит в состав корпускулярного излучения Солнца и космических лучей" - БСЭ
В организме человека находятся 81 химический элемент из 92 встречающихся в природе. Человеческий организм - сложная химическая лаборатория. Трудно себе представить, что ежедневно наше самочувствие, настроение и даже аппетит могут зависеть от минеральных веществ. Без них бесполезными оказываются витамины, невозможны синтез и распад белков, жиров и углеводов.
На столах у учеников - таблицы "Биологическая роль химических элементов"
-
Провожу вместе с учащимися анализ таблицы Основу жизни составляют шесть элементов первых трех периодов (H, C, N, О, Р, S), на долю которых приходится 98% массы живого вещества (остальные элементы периодической системы составляют не более 2%).
-
Таблица 1. Суточное поступление химических элементов в организм человекаЖизненно необходимые элементы
-
Таблица 2. Характерные симптомы дефицита химических элементов в организме человека
Пищевые источники макроэлементов
Кальций
1000 мг-2500 мг
Молоко и молочные продукты
Калий
2000 мг-5000 мг
Сухофрукты, бобовые, картофель, дрожжи
Натрий
550 мг-2300 мг
Пищевая соль
Магний
300-350 мг
Продукты из муки грубого помола, орехи, бобовые, зеленые овощи
Фосфор
700 мг-4000 мг
Молоко, молочные продукты, мясо, рыба
Железо
10 мг
15 мг
45 мг
Бобовые, мясо, грибы, продукты из муки грубого помола
7. Ученикам раздаются тексты (см. Приложение 3). Задание: внимательно прочитать текст; выделить элементы, необходимые для жизни, и элементы, опасные для живых организмов и объяснить их роль.
- Элементы-аналоги в природной среде вступают в конкуренцию и могут взаимозаменяться в живых организмах, отрицательно на них влияя. Замена натрия и калия в организмах животных и человека на литий вызывает расстройства нервной системы, так как в этом случае клетки не проводят нервный импульс. Подобные нарушения приводят к шизофрении. Таллий, биологический конкурент калия, заменяет его в стенках клеток, поражает центральную и периферическую нервную систему, желудочно-кишечный тракт и почки. Селен может заменить серу в составе белков. Это единственный элемент, который при высоком содержании в растениях может вызвать внезапную смерть животных и человека, употребивших их в пищу. Кальций при его недостатке в почве заменяется в организме на стронций, который постепенно нарушает нормальную структуру скелета. Особенно опасна замена кальция на стронций-90, который в огромных количествах накапливается в местах ядерных взрывов (при испытании ядерного оружия) или при авариях на АЭС. Этот радионуклид разрушает костный мозг. Кадмий конкурирует с цинком. Этот элемент снижает активность пищеварительных ферментов, нарушает процесс образования гликогена в печени, вызывает деформацию скелета, угнетает рост костей, а также вызывает тяжелые боли в пояснице и в мышцах ног, хрупкость костей (например, перелом ребер при кашле). Другие негативные последствия - рак легких и прямой кишки, нарушение функции поджелудочной железы. Поражение почек, снижение содержания в крови железа, кальция, фосфора. Этот элемент тормозит процессы самоочищения в водных и наземных растениях (отмечается, например, 20-30-кратное увеличение кадмия в листьях табака). Галогены могут очень легко взаимозаменяться в организме. Избыток фтора в окружающей среде (фторированная вода, загрязнение почвы соединениями фтора вокруг предприятия по производству алюминия и другие причины) препятствует поступлению в организм человека йода. В связи с этим возникают заболевания щитовидной железы, эндокринной системы в целом.
-
Имеется большое число химических элементов, особенно среди тяжелых, являющихся ядами для живых организмов. Они оказывают неблагоприятное биологическое воздействие. В табл. 3 приведены эти элементы в соответствии с Периодической системой Д.И. Менделеева.
-
Таблица 3.
Pt
Au
Ba
Hg
Сообщения учащихся, подготовленные заранее. "Биологическая роль химических элементов"
1-й учащийся:
ЗОЛОТО и ГЕРМАНИЙ
Средневековые алхимики считали золото совершенством, а остальные металлы - ошибкой в акте творения и, как известно, прикладывали большие усилия к ликвидации этой ошибки. Идею введения золота в медицинскую практику приписывают Парацельсу, который провозгласил, что целью химии должно быть не превращение всех металлов в золото, а приготовление лекарств. Лекарственные препараты из золота и его соединений пытались применять при многих заболеваниях. Им лечили проказу, волчанку, туберкулез. У людей, чувствительных к золоту, оно могло вызвать нарушение состава крови, реакцию со стороны почек, печени, влиять на настроение, рост зубов, волос. Золото обеспечивает работу нервной системы. Оно содержится в кукурузе. А крепость кровеносных сосудов зависит от германия. Единственный продукт питания, содержащий германий, - чеснок.
2-й учащийся:
МЕДЬ
В человеческом организме наибольшее количество меди содержится в мозге и печени, и одно это обстоятельство указывает на ее важность в жизнедеятельности. Обнаружено, что при болях повышается концентрация меди в крови и спинномозговой жидкости. В Сирии и Египте новорожденным для профилактики рахита и эпилепсии надевают медные браслеты.
3-й учащийся:
АЛЮМИНИЙ
Алюминиевую посуду называют посудой бедняков, так как этот металл способствует развитию старческого атеросклероза. При приготовлении пищи в такой посуде алюминий частично переходит в организм, где и накапливается.
4-й учащийся:
Какой элемент содержится в яблоках? (Железо.)
-
Какова его биологическая роль? (В организме содержится 3 г железа, из них 2 г - в крови. Железо входит в состав гемоглобина. Недостаточное содержание железа приводит к головной боли, быстрой утомляемости.)
Закрепление
І. Составьте кластер «Химические элементы» (Что мы знаем о химических элементах?)
Занимательный тест «Улыбка».
Рисунок, мордашки забавного человечка. Вместо рта у него 15 точек, расположенных в 3 ряда.
(5 вопросов в тесте и 3 варианта ответа)
ІІ. Задание
1) Из предложенного перечня выберите оксид:
а) Na2 О; б) Na(OH); в) H3PO4
2) Вещества, состоящие из атомов Н и кислотных остатков называются:
-
а) основание; б) кислота; в) соль.
3) В растворах щелочей фенолфталеин имеет цвет:
-
а) бесцветный; б) синий; в) малиновый.
4) Из предложенного перечня выберите щелочь:
-
а) гидроксид железа (II); б) гидроксид натрия; в) гидроксид цинка (II).
5) Вещества, состоящие из атомов металлов и кислотных остатков называются:
-
а) соли; б) кислоты; в) основания.
ІІІ. Задание
1) Из предложенного перечня выберите оксид:
-
а) СО2 ; б) Са(ОH)2; в) K2 SО4.
2) Из предложенного перечня выберите щелочь:
-
а) гидроксид железа(III); б) гидроксид бария; в) гидроксид меди (II).
3) В растворах щелочей лакмус имеет цвет:
-
а) бесцветный; б) красный; в) синий.
4) Вещества, состоящие из атомов Н и кислотных остатков называются:
-
а) основания; б) кислоты; в) соли.
5) Вещества, состоящие из атомов металлов и кислотных остатков называются:
-
а) соли; б) кислоты; в) основания.
IV. Рефлексия. У каждого из вас на столе лежит оценочный лист. Быстро подпишите их.
Закончите предложения:
Сегодня на уроке я повторил ___________________________________
Сегодня на уроке я узнал ______________________________________
Сегодня на уроке я научился ___________________________________
</ V. Домашнее задание. Повторить параграфы: …
Определить, о каком простом веществе идет речь:
а) Иду на мелкую монету,
В колокола люблю звенеть,
Мне ставят памятник за это
И знают имя моё - …………(медь)б) Предупреждаю я заранее,
Что не пригоден для дыхания!
А все как будто бы не слышат
И постоянно мною дышат.
Я главный в воздухе, так вот
Легко назвать меня?..................(азот)в) Я- светоносный элемент
Я спичку вам зажгу в момент,
Сгореть смогу и под водой,
Оксид в ней станет кислотой. (фосфор)г) Корабли меня обходят
Знает лоцман наизусть
Если Л на Д заменят
То металлом окажусь. (мель-медь)д) У меня дурная слава
Я известная отрава,
Даже имя говорит,
Что я страшно ядовит! (бром)
-