- Учителю
- Урок-лекция 'Спирты' (10 класс)
Урок-лекция 'Спирты' (10 класс)








 СПИРТЫ
СПИРТЫ
Цели и задачи:
-
Дать учащимся первоначальные понятия о кислородсодержащих веществах.
-
Познакомить учащихся с составом, физическими, химическими свойствами спиртов.
-
Закрепить знания учащихся по гомологии и изомерии.
-
Способствовать формированию представления о физиологической роли спиртов на организм.
-
Продолжить на примере спиртов формирование понятия о химических свойствах, их обусловленности строением вещества и наличием в составе молекулы функциональной группы - ОН.
-
Познакомить учащихся с применением, а также со способами получения спиртов.
-
Продолжить формирование мировоззренческих знаний: умение характеризовать свойства спиртов на основе их состава и строения.
-
Решение задачи на вывод молекулярной формулы органического вещества по продуктам сгорания.
Задача: При сжигании 4,8 г органического вещества образовалось 3,36 л
углекислого газа и 5,4 г воды. Найдите молекулярную формулу
этого углеводорода, если плотность паров этого вещества
по водороду равна 16.
-
Вычисляем молекулярную массу органического вещества, используя относительную плотность его паров по водороду:
Mr=16 · 2 = 32
-
Определяем массу атомов углерода: в 3,36 л СО2 содержится х г С
22,4 л СО2 содержится 12 г С

===+++==== =+==+=
-
Определяем массу атомов водорода: в 5,4 г Н2О содержится у г Н
18 г Н2О содержится 2 г Н
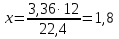
-
Сумма масс углерода и водорода равна массе сожженного вещества: m(С+Н)=1,8+0,6=2,4 г. Следовательно, органическое вещество содержит третий элемент. Это - кислород.
-
Находим соотношение масс: С : Н : О =
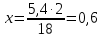 = 0,15 : 0,6 : 0,15 = 1 : 4 : 1
= 0,15 : 0,6 : 0,15 = 1 : 4 : 1
Значит СН4О - это простейшая формула.
Мr (СН4О) = 12+4+16=32
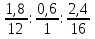 =1
=1
-
Значит, искомая формула СН4О.
Найденная формула состоит из трёх элементов и содержит атом кислорода. Такие вещества относят к классу кислородсодержащих органических соединений - спирты - алканолы. Это и будет новая тема урока.
II.Новая тема.
-
Спирты - производные предельных углеводородов, в молекулах которых один или несколько атомов водорода замещены на один или несколько гидроксильных групп.
R - OH CnH2n+2O CnH2n+1OH
R - функциональная группа - группа атомов, которая обусловливает характерные химические свойства данного класса веществ.
Спирты
одноатомные многоатомные
СН3 - ОН СН2 - СН - СН2
метиловый спирт ǀ ǀ ǀ
ОН ОН ОН
глицерин
-
Гомологический ряд алканолов.
СН3 - ОН метанол, метиловый спирт
С2Н5 - ОН этанол, этиловый спирт
С3Н7 - ОН пропанол, пропиловый спирт
С4Н9 - ОН бутанол, бутиловый спирт и т.д..
3) Изомерия спиртов
1. Изомерия углеродного скелета
СН3 - СН2 - СН2 - СН2 - ОН бутанол-1
СН3 - СН - СН2 - СН2 - ОН 3-метилбутанол-1
‖
СН3
2. Изомерия положения функциональной группы
СН3 - СН2 - СН2 - СН2 - ОН бутанол-1 (первичный спирт)
СН3 - СН - СН2 - СН3 бутанол-2 (вторичный спирт)
‖
ОН
___________________________
СН3
‖
СН3 - С - СН2 - ОН 2,2-диметилбутанол-1 (третичный спирт)
‖
СН3
3. Межклассовая изомерия с простыми эфирами
С2Н6О
алканол простой эфир
СН3 -СН2 - ОН СН3 - О - СН3
этанол диметиловый эфир
-
Химические свойства спиртов
-
Реакции замещения:
а) с активными металлами с образованием алкоголятов
2 R-OH + 2 Me* 2 R-OMe* + H2_
2 С2Н5-OH + 2 Na 2 С2Н5-ONa + H2
этилат натрия
б) этерификация (взаимодействие молекулы спирта с молекулой кислоты)
с образованием сложного эфира
O O
// //
R - C + HO - R1 R - C + H2O
\ \
OH O - R1
сложный эфир
O O
// //
CH3 - C + HO - C2H5 CH3 - C + H2O
\ \
OH O - C2H5
этиловый эфир уксусной кислоты
в) гидрогалогенирование (присоединение галогеноводорода)
с образованием моногалогеналканов
R - OH + HHaI R-HaI + H2O
CH3 - CH2 - OH + HCI CH3 - CH2 - CI + H2O
хлорэтан
-
Реакции отщепления:
а) дегидратация (отщепление молекулы воды)
-
внутримолекулярная с образованием алкенов
R - OH H2O + CnH2n
CH3 - CH2 -OH C2H4 + H2O
этилен
-
межмолекулярная (алкилирование) с образованием простых эфиров
R - OH + HO - R1 R - O - R1 + H2O
простой эфир
CH3 - OH + HO - CH3 CH3 - O - CH3 + H2O
диметиловый эфир
б) дегидрирование (отщепление водорода )
-
первичных спиртов с образованием альдегидов
H H O
| | Cu, t //
H C C O H CH3C + H2
| | \
H H H
этаналь
( ацетальдегид, уксусный альдегид)
-
вторичных спиртов с образованием кетонов
Cu, t
CH3CHCH3 CH3 CCH3 + H2
| ||
OH O
диметилкетон
( ацетон )
-
третичные спирты не дегидрируются.
-
Реакции окисления:
а) горение: R - OH + O2 CO2 + H2O
C3H7OH + 4,5 O2 3 CO2 + 4 H2O
б) окисление оксидом меди (II): качественная реакция на алканолы с образованием
альдегидов
О
t //
CH3 - CH2 - OH + CuO CH3 - C + Cu + H2O
\
Н
этаналь
( ацетальдегид, уксусный альдегид)
-
Получение спиртов.
1. Гидролиз моногалогеналканов водными растворами щелочей:
R - Br + NaOH → R - OH + NaBr
H3PO4, t
2. Гидратация алкенов: H2C=CH2 + HOH CH3 - CH2 - OH
3. Гидрирование альдегидов с образованием первичные спиртов
О
// t, кат.
CH3 - C + H2 CH3 - CH2 - OH
\ этанол
Н
4. Гидрирование кетонов с образованием вторичных спиртов
Ni, t
СН3 - С - СН2 - СН3 + Н2 СН3 - СН - СН2 - СН3
‖‖ ‖
О ОН
5. Спиртовое брожение углеводов (глюкозы)
ферменты
С6Н12О6 2 С2Н5ОН + 2СО2
6. Получение метанола из синтез-газа
Cr2O3 + ZnO, t, p
СО + 2Н2 СН3ОН
6) Применение и значение спиртов
-
Метанол (древесный, метиловый спирт) СН3ОН - прозрачная жидкость со специфическим запахом, напоминающим этиловый спирт. Метиловый спирт - сильный яд. Несколько его граммов, попав в организм, приводят к слепоте, а большие количества - к смерти. Подлежит обязательной маркировке «Метанол - яд».
-
Метанол используют для получения сложных эфиров, которые применяют в пищевой промышленности в качестве ароматизаторов, а также отдушек и растворителей в парфюмерии.
-
Является основой для производства формальдегида, некоторых лекарственных веществ.
-
Служит растворителем лаков и красок.
-
Получают различные органические продукты, в том числе - высокооктановое топливо.
-
Этанол (этиловый спирт) С2Н5ОН - бесцветная жидкость, легко испаряющаяся.
Этиловый спирт - сильный наркотик. Попадая в организм, он быстро всасывается в кровь и приводит организм в возбуждённое состояние, при котором человеку трудно контролировать своё поведение. Употребление спирта часто является основной причиной тяжёлых ДТП, несчастных случаев на производстве и бытовых преступлений. Спирт вызывает тяжёлые заболевания нервной и сердечно-сосудистой систем, а также желудочно-кишечного тракта. Спирт опасен в любой концентрации.
-
Из этанола получают синтетический каучук, уксусную кислоту, красители, эссенции, фотоплёнку, порох, пластмассы.
-
Является хорошим растворителем и антисептиком. Поэтому применяется в медицине, парфюмерии.
-
Применяется в пищевой промышленности.
-
В ряде стран используют в качестве альтернативного топлива для двигателей внутреннего сгорания.
7) Домашнее задание: § 20, 21, с. 88, упр. 14 (б).