- Учителю
- урок на тему: 'Кислоты'
урок на тему: 'Кислоты'
Урок - путешествие по теме: Кислоты.
Цель: сформировать представление о кислотах (состав, классификация, представители), формировать умения составлять формулы химических соединений.
Оборудование: презентация, серная и соляная кислоты, индикатор метилоранж, пробирки, лимон, аскорбиновая кислота, яблоко, таблица: «Изменение окраски индикаторов».
На доске карта путешествия по «стране кислот».
Вступительное слово:
Мы - исследователи кислот -
Так называется этот урок
Он будет совсем необычным у нас
Представим себе, что это - не класс
Отправимся все мы на 40 минут
В страну, где сегодня кислоты нас ждут
Итак, нам предстоит увлекательное путешествие в мир кислот. Но прежде чем отправиться в путь, необходимо проверить, все ли готовы к путешествию и проверить багаж знаний (повторение 3 мин)
ОПРОС. 1.Вспомним, на какие классы классифицируют неорганические вещества? (На оксиды, основания, кислоты, и соли).
2. Назовите, какие из них мы с вами уже изучили? (оксиды и основания).
ПОКАЗЫВАЮ 2-3 карточки с формулами оксидов.
3. Какой класс неорганических соединений я вам показываю сейчас? (Оксиды).
4. На основании чего вы сделали такой вывод? (дают определение оксидам).
5. Прочитайте и назовите каждый оксид.
ПОКАЗЫВАЮ 2-3 карточки с формулами оснований.
6. Формулы, каких веществ я показываю сейчас? (Оснований).
7. Почему эти вещества относятся к основаниям? (Дают определение оснований).
8. Прочитайте и дайте названия этим основаниям.
Можно провести интерактивную игру. При демонстрации формул оснований - ученики встают, оксидов - хлопают в ладоши.
Изучение нового материала.
Демонстрируется 1 слайд презентации. Какие на вкус эти продукты питания. (Кислые).
Слово кислый имеет однокоренное слово - кислота.
Учащиеся формулируют тему урока.
1 станция - историческая. Дежурный по станции рассказывает историю открытия важнейших кислот (первая кислота - уксусная).
Кислоты - прошлое и настоящее. Самая первая кислота, которую научился получать и использовать человек - уксусная. Знакомство кислотами началось в глубокой древности. Азотная кислота, её получение и свойства описывались в трудах врача и алхимика Джабира ибн Хайяна. Химики готовили кислоты при нагревании смеси природной селитры, медного купороса и квасцов, соляную - нагреванием морской соли с глиной. В России купоросное масло (серная), крепкая водка(азотная) и царская водка(смесь азотной и соляной) получали в аптеках. Сохранились записи 1575 года: делал водку крепкую аптекарского приказа ученик Иван Тыю, а на это дело дано пол пуда купороса и 10 фунтов селитры. Сделано всего крепкой водки 6 пудов. А использовали азотную кислоту, или крепкую водку для прижигания бородавок и поражений кожи, разбавленную соляную - для улучшения секреции желудка.
2 станция - дегустационная. Убедитесь, что кислоты - кислые на вкус. Но в кабинете химии нельзя пробовать вещества на вкус. Но сегодня - исключение. Кроме того - вспомните вкус клюквы, щавеля, уксуса. Запишите - (кислоты кислые на вкус, но есть исключения: салициловая - сладкая, никотиновая - горькая.)
Наш поезд отправляется дальше, но красный свет светофора предупреждает, что следующая остановка -
3 станция - Правила техники безопасности (в учебнике - правила работы с кислотами) Внимание! Работать с кислотами необходимо аккуратно, так как можно получить ожог или отравление.
-
При попадании кислоты на кожу надо смыть её струёй воды.
-
Обработать 2% раствором гидрокарбонатом натрия.
4 станция - Информационная. Давайте рассмотрим и проанализируем формулы важнейших кислот. Обратим внимание на состав кислот и сформулируем вместе определение:
Кислоты - это сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка. Как правило, кислотные остатки образуют атомы неметаллов. Обратите внимание, есть кислотные остатки, содержащие кислород, и кислотные остатки без кислорода. Поэтому кислоты классифицируют: 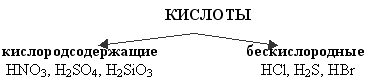
Существует ещё одна классификация кислот: по основности - одноосновные, двухосновные и трехосновные. 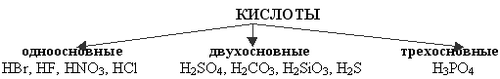
5 станция - Индикаторная. Однажды английский химик Роберт Бойль, изучая свойства соляной кислоты, случайно пролил её. Кислота попала на сине - фиолетовые лепестки фиалок. Спустя некоторое время лепестки стали ярко - красными. Это явление удивило Бойля и он тут же провел серию опытов с разными кислотами и цветами разных растений. Оказалось, что и васильки, и роза и цветки некоторых других растений изменяли окраску при действии кислот. Особенно интересным оказался фиолетовый настой лакмусового лишайника. В растворах кислот он становился красным, а в растворах щелочей - синим. После некоторых раздумий такие вещества Бойль назвал индикаторами, что в переводе с латинского - указатели. Эти вещества стали использовать для распознавания кислот и оснований. Индикаторы помогли Бойлю открыть новую кислоту. Сжигая фосфор и растворяя белый продукт в воде, он получил неизвестную химикам кислоту. По исходному веществу он назвал её фосфорной. На прошлом уроке мы познакомились с индикаторамим (какими?) Фенолфталеиновый - в щелочах малиновый, метилоранж - желтый, лакмусовая бумага - синеет. Давайте попробуем распознать с помощью индикаторов кислоту.
Лабораторный опыт: У вас на столах три пробирки: с водой, кислотой, основанием, а также индикатор метилоранж. Как видно из таблицы - метилоранж в кислотах розовеет. Все выполняют опыт и делают вывод: кислоты проявляют общие свойства, что связано с их строением(наличие атома водорода) Эта скромная бумажка Все покажет без труда Посинеет - в колбе щелочь Покраснеет - кислота.
Итак, наше путешествие по стране кислот подходит к концу и нам пора возвращаться.
Закрепление изученного материала (организовать работу по группам)
1группа. Дан текст, в котором «спрятаны» формулы кислот. Подчеркните их.
H2OSOHBrNa2Co3MgBaH2CO3SO4KOH
H3PO4P2O5CaH2SKPHNO2CS2NH3O3C
HClBaSHKSHH2Na2OH2SiO3NaClH2SO4
2группа. Игра «Третий лишний». В каждом ряду найдите лишнюю формулу, ответ мотивируйте:
![]()
3группа. Ребята решили укомплектовать свою учебную лабораторию оксидами, основаниями и кислотами. Заказ им прислали по почте в виде двух посылок:
1-я посылка: NaOH, CaO, H3PO4, HNO3, Ca(OH)2, Cr2O3
2-я посылка: FeO, H2SO4, KOH, Fe(OH)2, P2O5, HCl,
Распределите полученные вещества по полкам, мотивируйте свою комплектацию
Вопросы для закрепления.
1.Какие вещества называют индикаторами? Кто открыл индикаторы?
2.Какие вещества называют кислотами? С какими кислотами вы познакомились?
3. Какие существуют меры предосторожности при работе с кислотами?
4. Что вы узнали о кислотах на дегустационной станции? Все ли кислоты можно пробовать на вкус? Правильно ли утверждение: вещество можно определить по вкусу: если оно кислое - это кислота.
5. Как называется первая кислота, с которой познакомился человек?
Подведение итогов урока. Выставление оценок. Домашнее задание.