- Учителю
- Урок для учащихся 9 классов В мире электролитической диссоциации
Урок для учащихся 9 классов В мире электролитической диссоциации
 «Рудный қаласының № 10 мектеп - гимназиясы» ММ
«Рудный қаласының № 10 мектеп - гимназиясы» ММ
ГУ «Школа-гимназия №10 города Рудного»
Сабақтың тақырыбы: «Электролитикалық өмірдегі диссоциациясы»
Тема урока: «В мире электролитической диссоциации»
Сынып: 9
Класс: 9
Номинация : Лучшая разработка урока с ИКТ
автордың А.Т.Ж.: Курочка Юлия Васильевна, химия мұғалім,
«Рудный қаласының № 10 мектеп - гимназиясы» ММ
Ф.И.О. авторов: учитель химии, ГУ «Школа-гимназия №10 города Рудного»
Тарасова Александра Витальевна, физика мұғалім,
«Рудный қаласының № 10 мектеп - гимназиясы» ММ
учитель физики, ГУ «Школа-гимназия №10 города Рудного»

г. Рудный
2013г.
ГУ «Школа - гимназия № 10 города Рудного»
Учителя: Курочка Юлия Васильевна
Тарасова Александра Витальевна
БИНАРНЫЙ УРОК ХИМИИ И ФИЗИКИ
9 класс
Тема: «В мире электролитической диссоциации»
Цель: Создать условия для закрепления, повторения и обобщения изученного материала по теме: «Электролитическая диссоциация»; способствовать развитию информационной и коммуникативной компетентностей через разнообразные виды деятельности.
Задачи:
-
Обобщить знания учащихся по теме: «Электролитическая диссоциация».
-
Способствовать дальнейшему:
-
развитию умений учащихся устанавливать причинно-следственные связи;
-
совершенствованию навыков учащихся в составлении РИО;
-
развитию мировоззренческих взглядов, логического мышления, выявлять общее и единичное;
-
развитию умений работать в атмосфере поиска, творчества.
-
Активизировать познавательную деятельность обучающихся на всех этапах урока.
Программное обеспечение: ActiveStudio, Pazlphoto
Оборудование:
-
интерактивная доска, флипчарт урока, GLX-explorer
-
раздаточные материалы: карточки с вопросами «Блиц», 4 комплекта по 28 уравнений;
-
лабораторные ящики с наборами реактивов: растворы гидроксида натрия, сульфата меди, карбаната натрия, азотной кислоты; пробирки,
-
4 листа А3, маркеры
Ход урока:
-
Организационный момент:
Учитель: Здравствуйте, дорогие друзья!
Мы рады видеть вас и хотим, чтобы наш урок прошёл успешно. Успешным он будет, если всем нам будет интересно, а интерес - это в первую очередь наше положительное эмоциональное состояние.
Работать на уроке вы будете в командах (класс делится на 4 команды по 6-7 человек, каждая команда выбирает капитана, придумывает название и девиз). Представьте, пожалуйста, свои команды.
Учитель: Тему, цели и девиз урока вы узнаете, собрав пазлы. (во флипчарте с помощью программы «Pazlphoto»)

Предлагаем первой команде собрать пазлы с загадкой, второй - пазлы с названием темы урока, третьей - пазлы с целями урока, четвертой - с девизом урока. Ваша задача собрать пазлы, как можно быстрее. Победит, та команда, которая затратит меньше времени. К доске приглашаются два представителя команды, остальные члены команды могут подсказывать с места, только в том случае, если участники испытывают затруднение. Победившая команда получает 2 балла.
К доске приглашаются участники первой команды:
Результат:
Жил один кристалл ионный,
Был красивый он и ровный,
Но случилась с ним беда.
Капля на него упала,
И кристалла вмиг не стало:
Вдруг на что-то распластала
Его ловкая вода.
Все семейство удивилось:
«Что с кристаллом приключилось?»
Учитель: Предлагаем ученикам других команд отгадать загадку. За правильный ответ - 0,5 балла.
Ученик: электролитическая диссоциация.
Учитель: К доске приглашаются участники второй команды, которые помогут нам назвать тему урока.
Результат: «В мире электролитической диссоциации».
Затем приглашаются участники третьей команды, которые освещают цели урока.
Результат: Цели урока: повторить и закрепить основные понятия темы «Электролитическая диссоциация», уравнения РИО, качественные реакции на ионы.
Для оглашения девиза урока приглашаются участники четвертой команды.
Результат:
«От знанья в сердце вспыхнет яркий свет, оно для тела - как броня от бед». (Рудаки)
-
Актуализация знаний:
Учитель: Начинаем работу с «Гимнастики для ума» по повторению основных понятий. Каждой команде будет задано по три вопроса. За каждый правильный ответ один балл. Если команда не знает ответа, то право ответа получают команды соперников. Максимальное количество баллов, которые получает каждая команда -3б.
Вопросы: во флипчарте (прием «Звуковая дорожка»)
1. Какие вещества называются электролитами?
2. Почему электролиты проводят электрический ток?
3. Назовите группы веществ которые относятся к электролитам?
4.Какие вещества называются неэлектролитами?
5. Почему неэлектролиты не проводят электрический ток?
6. Назовите группы веществ которые относятся к неэлектролитам?
7. Чем атомы отличаются от ионов?
8 Что такое степень электролитической диссоциации?
9. Какой процесс называется электролитической диссоциацией?
10. Что такое основания с точки зрения теории электролитической диссоциации?
11. Что такое кислоты с точки зрения теории электролитической диссоциации?
12. Что такое соли с точки зрения теории электролитической диссоциации?
Правильные ответы указаны во флипчарте( прием «Скрытый объект»).
Продолжаем работу по отработке теоретических аспектов в блиц-опросе. На столах у вас лежат карточки с вопросами блица. Каждый участник команды пишет на карточке ответ только на один вопрос, который достается ему в порядке очередности и передает следующему участнику. Максимальное количество баллов, которые получает каждая команда -3,5 б. (за каждый правильный ответ-0,5б.)
«Блиц»
* Положительно заряженный
* Отрицательно заряженный электрод
* Направленное движение заряженных частиц
* Положительно заряженные частицы
* Отрицательно заряженные частицы
* Раствор спирта является
* Раствор медного купороса
Проверка правильных ответов во флипчарте с помощью приема «Волшебная колба».
Вывод учителя: в ходе « Блица» и «Гимнастики для ума» мы повторили основные понятия темы, которые помогут вам в дальнейшем.
Учитель: Следующим испытанием для команд будет «Мозговой штурм». На доске вы видите элементы схемы механизма электролитической диссоциации. Ваша задача на листах А-3 за 5 минут изобразить механизм электролитической диссоциации, используя все элементы схемы. Группа, выполнившая работу быстрее других, демонстрирует свой результат и собирает схему во флипчарте (перемещение объкта по флипчарту). Максимальное количество баллов -3б.

Вывод учителя: В споре рождается истина. Работа в команде позволяет вам сплотиться и правильно выполнить любое задание.
Учитель: Переходим от теории к эксперименту - «Теория - основа практики». Во флипчарте внимательно посмотрите видеофрагменты и объясните результаты увиденного с точки зрения физики и химии ( прием « Ссылка на видеофайл»).
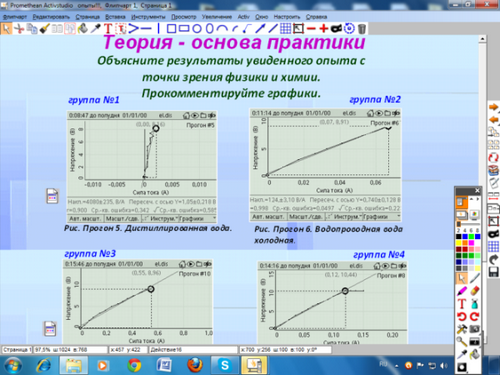
Ученики: участники каждой группы просматривают свой видеофрагмент и комментируют результаты опытов и графики, полученные с помощью GLX-explorer . Максимальное количество баллов -2б.
Учитель: Вы не раз проделывали «чудеса своими руками».Переходим к этапу « И опыт - сын ошибок трудных…». Давайте в очередной раз покажем свои умения.
Напоминаем вам о технике безопасности:
При работе с веществами
Не берите их руками
И не пробуйте на вкус.
Реактивы - не арбуз:
Слезет кожа с языка
И отвалится рука…
Учитель: Вспомним качественные реакции на катионы и анионы. У вас на столах набор реактивов. Вы должны провести качественные реакции с предложенными веществами и составить молекулярные, полные ионные и сокращенные ионные уравнения (РИО).
Ученики: начинают работу по выполнению эксперимента и составляют уравнения реакций;
Учитель: Результаты опытов и составленные уравнения реакций передайте группе соперников для взаимопроверки и оценивания. Максимальное количество баллов -2б.
Во флипчарте ( прием «Перемещение объекта»)
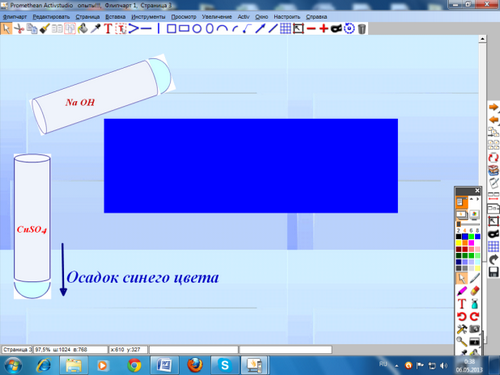
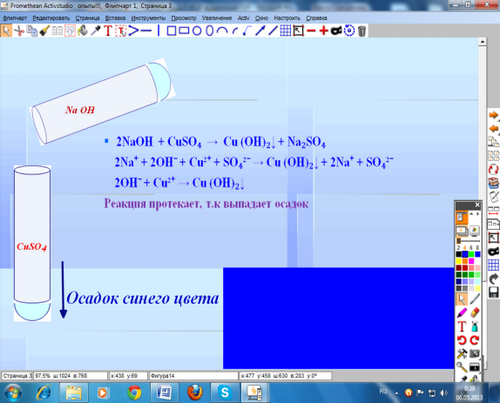
правильные ответы:
имеющаяся соль - сульфат меди (II) будет реагировать с гидроксидом натрия, что приведет к выпадению синего осадка, а карбонат натрия в реакции с азотной кислотой приведет к выделению газа.
-
2NaOH + CuSO₄ → Cu (OH)₂↓ + Na₂SO₄
2Na⁺ + 2OHˉ + Cu²⁺ + SO₄²ˉ → Cu (OH)₂↓ + 2Na⁺ + SO₄²ˉ
2OHˉ + Cu²⁺ → Cu (OH)₂↓
-
Na₂CO₃ + 2HNO₃ → 2NaNO₃+ CO₂↑+H₂O
2Na⁺+ CO₃²ˉ+2H⁺+2NO₃ˉ→ 2Na⁺+ 2NO₃ˉ+CO₂↑+H₂O
CO₃²ˉ+2H⁺→ CO₂↑+H₂
Вывод учителя: Опытным путём мы доказали возможность протекания реакций в растворах электролитов и закрепили умения составлять молекулярные, полные и сокращенные ионные уравнения реакции.
Учитель: Давайте еще раз продемонстрируем умения составлять реакции ионного обмена. В ходе «Вихря РИО» постарайтесь проявить свою сноровку. На столах каждой группы находится комплект карточек из 28 уравнений (на каждой карточке одно уравнение), в которых даны только формулы исходных веществ. Взяв любую карточку, из 28 предложенных, вы должны закончить молекулярное уравнение и составить полное ионное и сокращенное ионное уравнения. После выполнения задания ответ, который у вас получится в виде формулы вещества, доказывающего протекание данной реакции, найдите на доске и закройте карточкой определенного цвета: 1 группа-синим цветом, 2группа- красным, 3группа- желтым, 4 группа-зеленым. (прием «Цветная палитра»)
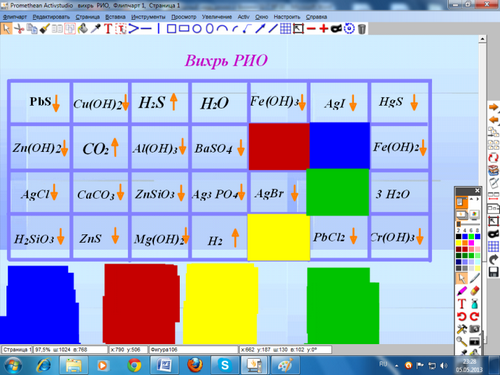
Составленные уравнения сдайте на проверку учителю, указав фамилию. Главное: опередить соперников, выполнив работу быстрее и успеть закрыть как можно больше ответов, так как все задания в каждой группе одинаковые. За каждую закрытую формулу 1 балл. Количество баллов подсчитывается по цветным карточкам.
Вывод учителя: Вы еще раз продемонстрировали свои умения составлять реакции ионного обмена (РИО) и умение работать в команде.
-
Итог урока: « Коротко о главном» (прием «Телеграфная лента»)
Учитель: Вы помните, что сегодня мы пришли на урок с целью повторить, закрепить и обобщить знания по теме «Электролитическая диссоциация». Давайте вспомним, чем мы занимались?
Ученики: Мы повторили основные понятия, совершенствовали навыки в составлении реакций ионного обмены, участвовали в химическом эксперименте, показали умения работать в команде.
-
Домашнее задание: составьте задание, которое может быть оформлено в виде кроссворда, теста или ребуса по теме «Электролитическая диссоциация»
Учитель: Мы считаем, что вы с пользой провели сегодня время.
Еще Б.Шоу сказал: «Единственный путь, ведущий к знанию, - это деятельность», чем мы занимались целый урок.
10