- Учителю
- Информационное сопрождение урока Строение атома
Информационное сопрождение урока Строение атома
5
ИНФОРМАЦИОННОЕ СОПРОВОЖДЕНИЕ
УРОКА:
Этап
Иллюстрации, вопросы, организация деятельности
Предполагаемые ответы
Второй
-
Что можно сказать об атоме?
-
Можно ли таким образом представить атом: в положительно заряженном шаре «плавают» электроны (модель Д.Д.Томсона)?
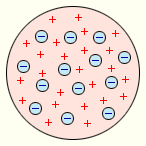
-
Давайте вспомним, как проводился этот эксперимент, какие результаты получены и, какие выводы были сделаны (опыт Э. Резерфорда, 1911 год).
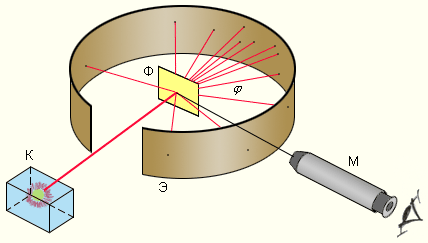
-
Учащимся предлагается объяснить результаты эксперимента, используя модель Томсона.
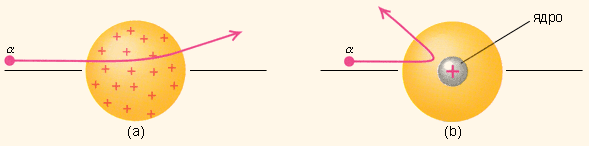
-
Модель, объясняющая результат была предложена Э. Резерфордом, название этой модели - планетарная.
-
Что представляет собой атом?
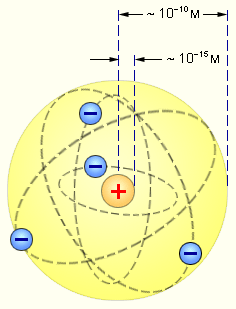
-
Почему атом нейтрален?
-
Как определить заряд ядра?
-
Каков физический смысл порядкового номера элемента в ПСХЭ?
-
Чем определяются химические свойства элемента?
-
Распределение электронов тоже определяется Z, следовательно, именно от Z зависят химические свойства любого элемента.
Атом - микрочастица, являющаяся наименьшей частью химического элемента. Он электри-чески нейтрален.
Данная модель не может объяснить результат опыта Э. Резерфорда.
Учитель напоминает учащимся, какую установку использовал Э. Резерфорд и предлагает обсудить результаты.
Модель Томсона не позволяет объяснить, почему очень малое число частиц отклонилось на углы, большие 900, и что заставило тяжелые частицы так резко изменить направление движения.
В центре находится маленькое и плотное ядро, а снаружи - электроны.
Суммарный заряд электронов равен заряду атомного ядра.
q = Ze, где Z - порядковый номер элемента в ПСХЭ,
е = 1,6 . 10 -19Кл - элементарный заряд, равный заряду электрона.
Он определяет заряд атомного ядра и число электронов, окружающих ядро.
Числом валентных электронов, которые могут принять участие в образовании химических связей.
Третий
-
1896г. - А. Беккерель обнаружил, что уран самопроизвольно испускает излучение, способное проходить через картон и бумагу и действующее на фотопластину.
-
Радиоактивность - самопроизвольное превращение атомного ядра, сопровождающееся испусканием заряженных частиц, нейтронов и фотонов.
-
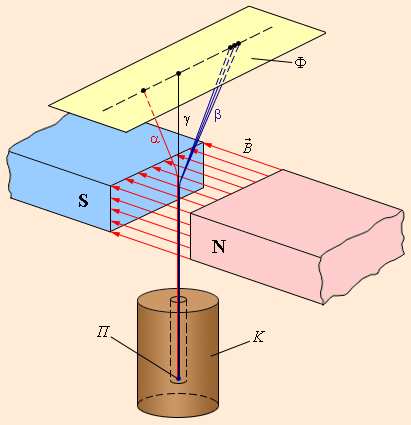
1899г - 1900г. - Э. Резерфорд пропустил это излучение через сильное магнитное поле, выделил три составляющие:
1. положительная,
альфа - частицы, ядра гелия. 2. отрицательная, бета - частицы, быстрые электроны.
3. нейтральная, гамма - излучение,
фотоны (кванты электромагнитного поля).
-
1913г. - Э. Резерфорд предположил, что ядро водорода - протон.
-
Протон - положительная частица, заряд который равен заряду электрона, а масса приблизительно равна атомной единице массы.
-
1 а.е.м.= 1.66 . 10 -27 кг.
-
Если ядро состоит из Z протонов, то как найти его заряд?
-
Чему тогда равна масса ядра (если использовать аналогию в ядром водорода)?
-
На самом деле массы ядер больше, чем суммы масс протонов. Как можно это объяснить?
-
1932г. - Дж. Чедвик обнаружил нейтроны, экспериментально подтвердив гипотезу Э. Резерфорда об их существовании.
-
Нейтрон - частица, не имеющая заряда, масса которой равна
тп = 1.67 . 10 -27кг = 1,0087 а.е.м.
-
Какие частицы входят в состав ядра?
-
Эти частицы называют нуклонами.
-
Дайте определение «нуклонам».
-
Как можно объяснить, что ядро - стабильное образование, ведь в нем плотно упакованы положительные частицы?
-
В ядре нуклоны связаны ядерными силами (сильным взаимодействием).
-
Массовое число A = Z + N.
-
Ядро атома называют нуклидом.
-
Какими числами можно охарактеризовать нуклиды?
-
Педагог предлагает ученикам по предложенным записям определить состав нуклидов:
![]() и т.д.
и т.д.
-
Ученикам предлагается прочитать содержание п.5 на стр. 222 и ответить на вопросы:
-
Что такое изотопы?
-
-
Отличаются ли по свойствам изотопы одного и того же элемента? Почему?
-
Как образовано слово изотоп?
-
Как вы думаете почему?
При анализе иллюстрации учащиеся выдвигают свои предположения, как и почему Э. Резерфорд получил такие результаты:
-отклонение лучей в магнитном поле, говорит о том, этот компонент имеет определенный заряд, положительный или отрицательный.
Заряд ядра равен Ze.
Z атомных единиц массы.
Вероятно, в состав ядра помимо положительных протонов входят еще какие-то нейтральные частицы.
Протоны и нейтроны.
Нуклоны - это частицы, входящие в состав ядра
Вероятно, нельзя взаимодействие между нуклонами объяснить действием кулоновских сил.
A , Z.
A = 238,
Z = 92,
N = 146.
Изотопы - нуклиды, имеющие одинаковое число протонов, но разное число нейтронов.
Так как заряд ядра не меняется, то химические свойства изотопов одного и того же элемента одинаковы.
От греческих слов isos и topos, то есть одинаковое место.
Изотопы занимают одно место в ПСХЭ.
Четвертый
Учащимся предлагается выполнить тестовую работу с целью проверки первичного усвоения материала
Пятый
Домашнее задание п.п.8.1, 8.2, 8.4